
Wetenschap
Wat is het kenmerk van een covalente binding?
Hier zijn enkele kenmerken van een covalente binding:
* Formatie: Covalente bindingen worden gevormd wanneer twee of meer atomen een vergelijkbare elektronegativiteit hebben. Elektronegativiteit is een maatstaf voor het vermogen van een atoom om elektronen aan te trekken. Wanneer twee atomen een vergelijkbare elektronegativiteit hebben, delen ze elektronen gelijkelijk en vormen ze een covalente binding.
* Hechtsterkte: Covalente bindingen zijn sterker dan ionische bindingen, maar niet zo sterk als metaalbindingen. De sterkte van een covalente binding hangt af van de elektronegativiteit van de betrokken atomen en het aantal elektronen dat tussen de atomen wordt gedeeld.
* Polariteit: Covalente bindingen kunnen polair of niet-polair zijn. Een polaire covalente binding is een binding waarbij de elektronen niet gelijkelijk over de atomen worden verdeeld. Dit resulteert in een gedeeltelijke positieve lading op het ene atoom en een gedeeltelijke negatieve lading op het andere atoom.
* Lengte van de obligatie: De lengte van een covalente binding is de afstand tussen de kernen van de twee atomen die bij de binding betrokken zijn. De lengte van de binding hangt af van de grootte van de atomen en het aantal elektronen dat ertussen wordt gedeeld.
* Hefhoek: De bindingshoek is de hoek tussen twee covalente bindingen in een molecuul. De bindingshoek hangt af van de geometrie van het molecuul en het aantal elektronen dat tussen de atomen wordt gedeeld.
Voorbeelden van covalente bindingen:
* Waterstofmolecuul (H2):Het waterstofmolecuul wordt gevormd door de covalente binding van twee waterstofatomen. Elk waterstofatoom deelt één elektron met het andere waterstofatoom en vormt zo een enkele covalente binding.
* Watermolecuul (H2O):Het watermolecuul wordt gevormd door de covalente binding van twee waterstofatomen en één zuurstofatoom. Elk waterstofatoom deelt één elektron met het zuurstofatoom, en het zuurstofatoom deelt twee elektronen met elk waterstofatoom, waardoor in totaal vier covalente bindingen worden gevormd.
* Kooldioxidemolecuul (CO2):Het kooldioxidemolecuul wordt gevormd door de covalente binding van één koolstofatoom en twee zuurstofatomen. Elk zuurstofatoom deelt twee elektronen met het koolstofatoom en vormt in totaal vier covalente bindingen.
 Waarom is de elektrische lading in een atoom nul of neutraal?
Waarom is de elektrische lading in een atoom nul of neutraal?  Wat is de massa koolstof in 350 gram C2H6?
Wat is de massa koolstof in 350 gram C2H6?  Bevroren koper gedraagt zich als edelmetaal in katalyse:studie
Bevroren koper gedraagt zich als edelmetaal in katalyse:studie Wat is er anders aan de oplossing als je een homogeen mengsel en een oplossing vergelijkt?
Wat is er anders aan de oplossing als je een homogeen mengsel en een oplossing vergelijkt?  3D-kweken van hepatocyten op een lever-op-een-chip-apparaat
3D-kweken van hepatocyten op een lever-op-een-chip-apparaat
 Uit onderzoek blijkt dat klimaatverandering 10% heeft toegevoegd aan Ians regenval
Uit onderzoek blijkt dat klimaatverandering 10% heeft toegevoegd aan Ians regenval Egypte zou binnen tien jaar te maken kunnen krijgen met extreme waterschaarste
Egypte zou binnen tien jaar te maken kunnen krijgen met extreme waterschaarste Frankrijk keert het zeereservaat voor autobanden terug - een milieuflop
Frankrijk keert het zeereservaat voor autobanden terug - een milieuflop Een sociaal netwerk voor wereldwijd herstel van ecosystemen
Een sociaal netwerk voor wereldwijd herstel van ecosystemen Hoe oliepalm de vogelhabitat in Mexico beïnvloedt
Hoe oliepalm de vogelhabitat in Mexico beïnvloedt
Hoofdlijnen
- Strategie voor celdeling gedeeld door alle domeinen van het leven
- Hoe 'winnaar- en verliezerseffecten' de sociale rangorde van dieren en mensen beïnvloeden
- Wat is een vetzuur? | Hoe dingen werken
- Wat zijn bycobacteriën?
- Eerder onbekende details van bladluizen tijdens de vlucht om bij te dragen aan een betere gewasveiligheid
- Waarom wiebelen planten? Nieuw onderzoek biedt antwoorden
- Hoe wordt een bij een bijenkoningin?
- Studie volgt hoe aanpassingen aan het leven in een koud klimaat de sociale evolutie van Aziatische colobine-primaten bevorderden
- Eerste wetenschapper die zei dat alle planten uit cellen bestaan?
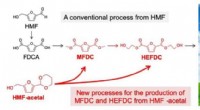
- Groene plastic productie gemakkelijk gemaakt
- Van de natuur afgeleide peptiden als moleculaire hulpmiddelen om cellulaire signalering te bestuderen
- Verdubbeling van de efficiëntie van organische elektronica

- Geavanceerde computers effent de weg naar de toekomst van NMR-spectroscopie

- Nieuwe techniek volgt individuele eiwitbeweging op levende cellen

 Verkeerde uitlijningen in ingekapseld grafeen leiden tot sterke wijziging van elektronische eigenschappen
Verkeerde uitlijningen in ingekapseld grafeen leiden tot sterke wijziging van elektronische eigenschappen NY klaagt Walmart aan, Doelwit voor de verkoop van speelgoed met een hoog loodgehalte
NY klaagt Walmart aan, Doelwit voor de verkoop van speelgoed met een hoog loodgehalte ONS, China bereikt een ZTE-deal van $ 1,4 miljard naarmate er tekenen verschijnen van voortgang van de handelsbesprekingen
ONS, China bereikt een ZTE-deal van $ 1,4 miljard naarmate er tekenen verschijnen van voortgang van de handelsbesprekingen Japanse raket met Mars-sonde VAE klaar voor lancering maandag
Japanse raket met Mars-sonde VAE klaar voor lancering maandag GPS is niet alleen meer voor roadtrips
GPS is niet alleen meer voor roadtrips Facebook lanceert app die gebruikers betaalt voor gegevens over app-gebruik
Facebook lanceert app die gebruikers betaalt voor gegevens over app-gebruik Facebook doodt de democratie met zijn persoonlijkheidsprofileringsgegevens
Facebook doodt de democratie met zijn persoonlijkheidsprofileringsgegevens Wetsvoorstel Maryland streeft naar transparantie in online politieke advertenties
Wetsvoorstel Maryland streeft naar transparantie in online politieke advertenties
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

