
Wetenschap
Waarom is fosforzuur een zwak zuur?
Fosforzuur is een zwak zuur omdat het slechts gedeeltelijk dissocieert in water. Wanneer fosforzuur oplost in water, reageert het met watermoleculen om waterstofionen (H+) en diwaterstoffosfaationen (H2PO4-) te vormen. Sommige fosforzuurmoleculen blijven echter ongedissocieerd in de oplossing.
De mate waarin fosforzuur dissocieert wordt bepaald door de dissociatieconstante, die een maat is voor de sterkte van het zuur. De dissociatieconstante voor fosforzuur is 7,5 x 10-3, wat betekent dat slechts een klein deel van de fosforzuurmoleculen in water dissocieert.
De zwakte van fosforzuur is ook te wijten aan het feit dat de gevormde diwaterstoffosfaationen relatief sterke basen zijn. Dit betekent dat ze kunnen reageren met waterstofionen om niet-gedissocieerde fosforzuurmoleculen te vormen. De combinatie van deze factoren maakt fosforzuur een zwak zuur.
 Nieuw boormateriaal met hoge hardheid gecreëerd door chemische dampafzetting in plasma
Nieuw boormateriaal met hoge hardheid gecreëerd door chemische dampafzetting in plasma Studie onthult precies hoe goedkope brandstofcelkatalysatoren werken
Studie onthult precies hoe goedkope brandstofcelkatalysatoren werken Materiaal voor veiligere voetbalhelmen kan hoofdletsel verminderen
Materiaal voor veiligere voetbalhelmen kan hoofdletsel verminderen Wat zou een voorbeeld van een verbinding zijn?
Wat zou een voorbeeld van een verbinding zijn?  Organische eutectica met kleine moleculen tonen potentieel voor het vervangen van kunststoffen
Organische eutectica met kleine moleculen tonen potentieel voor het vervangen van kunststoffen
 Spinnen:hoe griezelig zijn ze?
Spinnen:hoe griezelig zijn ze?  Opinie:Trumps dreigement op toezeggingen over klimaatverandering zal Afrika hard treffen
Opinie:Trumps dreigement op toezeggingen over klimaatverandering zal Afrika hard treffen NASA ziet een mix van tropische cycloon Ockhi en stofstormen
NASA ziet een mix van tropische cycloon Ockhi en stofstormen Engeland door droogte getroffen zomer 2022 gezamenlijk heetste ooit
Engeland door droogte getroffen zomer 2022 gezamenlijk heetste ooit Historische waterstanden bij reservoirs en dammen in Irak:Ambtenaren
Historische waterstanden bij reservoirs en dammen in Irak:Ambtenaren
Hoofdlijnen
- Controle van celpopulatiegroottes:wanneer is genoeg genoeg?
- Wanneer dupliceren chromosomen tijdens een cellevenscyclus?
- Genetici tonen aan dat COPIA-R7-transposon de immuniteit van zijn gastheer tegen pathogene micro-organismen verbetert
- Nieuw onderzoek met video laat zien hoe vrouwelijke kikkers zich verdedigen tegen ongewenste paring
- Wat maakt ons uniek? Niet zozeer genen als wel omringende sequenties
- Waarom hebben zich zoveel nieuwe ziekten ontwikkeld in de sector salades in zakken?
- Onderzoekers vinden dat diffusie een ongebruikelijke signaalrol speelt in Drosophila-embryo's
- Onderzoek laat zien hoe vistuig een langzame dood van walvissen kan veroorzaken
- Uit onderzoek blijkt dat troebel water ervoor kan zorgen dat Afrikaanse vissen grotere ogen ontwikkelen
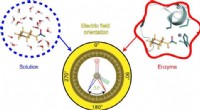
- Elektrische velden in kaart brengen om te helpen ontrafelen hoe enzymen werken
- Lassen met stamcellen voor chirurgische lijmen van de volgende generatie
- Consumenten, quats en COVID-19:zijn desinfecterende producten veilig?

- Onderzoekers ontdekken een nieuw anorganisch materiaal met de laagste thermische geleidbaarheid ooit gerapporteerd

- Hoe bouwen bacteriën natuurlijke producten op?
 Nieuw virtueel laboratorium voor het samenvoegen van neutronensterren
Nieuw virtueel laboratorium voor het samenvoegen van neutronensterren Astronomen laten zien hoe superreuzen herhaaldelijk afkoelen en opwarmen
Astronomen laten zien hoe superreuzen herhaaldelijk afkoelen en opwarmen Problemen oplossen met een analoge multimeter
Problemen oplossen met een analoge multimeter Onderzoekers voorspellen falen in ongeordende materialen
Onderzoekers voorspellen falen in ongeordende materialen Radiorelikwie gedetecteerd in een samensmeltend cluster van sterrenstelsels
Radiorelikwie gedetecteerd in een samensmeltend cluster van sterrenstelsels Wat gebeurt er aan de bewegende rand van een scheur?
Wat gebeurt er aan de bewegende rand van een scheur? Hoe kinderen te leren waar eten vandaan komt - laat ze tuinieren
Hoe kinderen te leren waar eten vandaan komt - laat ze tuinieren Canadese ijskappen verdwijnen, bevestiging van de wetenschappelijke voorspelling van 2017
Canadese ijskappen verdwijnen, bevestiging van de wetenschappelijke voorspelling van 2017
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

