
Wetenschap
Is het waarschijnlijker dat een diatomisch molecuul bij elkaar wordt gehouden door een covalente binding of door een ionisch molecuul? En waarom?
Bovendien moet de elektronegativiteit van de twee atomen in een diatomisch molecuul vergelijkbaar zijn om een covalente binding te kunnen vormen. Elektronegativiteit is een maatstaf voor hoe sterk een atoom elektronen aantrekt. Als de elektronegativiteit van de twee atomen te verschillend is, zal het ene atoom de elektronen sterker aantrekken dan het andere, en dit zal resulteren in een ionische binding.
Het diatomische molecuul waterstofchloride (HCl) wordt bijvoorbeeld bij elkaar gehouden door een covalente binding omdat de elektronegativiteit van waterstof en chloor vergelijkbaar is. Daarentegen wordt de ionische verbinding natriumchloride (NaCl) bij elkaar gehouden door een ionische binding omdat de elektronegativiteit van natrium en chloor heel verschillend is.
 Waarom moet de oplossing verzadigd zijn als de oplosbaarheid ervan wordt bepaald?
Waarom moet de oplossing verzadigd zijn als de oplosbaarheid ervan wordt bepaald?  Waarom gedragen boorverbindingen zich als Lewis-zuren?
Waarom gedragen boorverbindingen zich als Lewis-zuren?  Uit onderzoek blijkt dat interstitiële Cu de defectdichtheid in de matrix vermindert en het donorachtige effect onderdrukt
Uit onderzoek blijkt dat interstitiële Cu de defectdichtheid in de matrix vermindert en het donorachtige effect onderdrukt  Elektronenkristallografie bleek net zo goed te werken als röntgenkristallografie alleen op kleinere kristallen
Elektronenkristallografie bleek net zo goed te werken als röntgenkristallografie alleen op kleinere kristallen Nieuw polymeer verbetert het vermogen van tribo-elektrische nanogeneratoren
Nieuw polymeer verbetert het vermogen van tribo-elektrische nanogeneratoren
 Waarom vrouwelijke waterbuffels hoorns hebben, maar impala's niet?
Waarom vrouwelijke waterbuffels hoorns hebben, maar impala's niet?  NASA vindt overblijfselen van tropische cycloon Iris
NASA vindt overblijfselen van tropische cycloon Iris De verhuizing van Australië om koolstof in de bodem op te slaan is een probleem bij het aanpakken van klimaatverandering
De verhuizing van Australië om koolstof in de bodem op te slaan is een probleem bij het aanpakken van klimaatverandering De meest voorkomende oceaanplanten
De meest voorkomende oceaanplanten  Opwarming van de aarde - zorgwekkende lessen uit het verleden
Opwarming van de aarde - zorgwekkende lessen uit het verleden
Hoofdlijnen
- Supercoiling duwt moleculaire handboeien langs chromatinevezels
- Beschrijf de functies van celdeling in zowel eencellige als meercellige organismen?
- Wetenschappers gebruiken een supercomputer om te leren hoe cicadevleugels bacteriën doden
- Team ontwikkelt technologie voor de productie van bioplastics uit landbouw- en voedselbijproducten
- Vergelijking voor glucosemetabolisme
- Vertonen organismen die zijn geproduceerd als resultaat van binaire splijting een grote genetische variatie?
- Hoe plantensensoren ziekteverwekkers detecteren
- Flavonoïden van sorghumplanten doden vallegerwormplaag op maïs, kunnen gewas beschermen
- Monster ontdekt in het Canadese Noordpoolgebied
- Door machinaal leren ondersteund moleculair ontwerp voor hoogwaardige organische fotovoltaïsche materialen
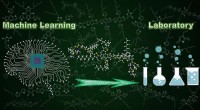
- Grote stappen voor het vastleggen van koolstof met behulp van aarde-overvloedige elementen als fotokatalytisch systeem
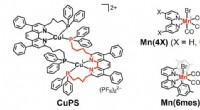
- Het vinden van vezelig eiwit kan leiden tot verbeterde bioprinting, tissue engineering
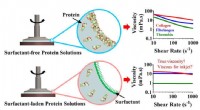
- Kleine medicijnafgiftecapsules kunnen getransplanteerde insulineproducerende cellen ondersteunen
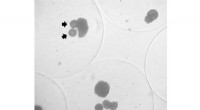
- Traditionele eutectische legering biedt nieuwe hoop voor metaal-zuurstofbatterijen met hoge energiedichtheid

 Betaald verlof kan de mama-kloof vergroten, maar de tijd met kinderen vergroten
Betaald verlof kan de mama-kloof vergroten, maar de tijd met kinderen vergroten Een reizende golf van opwinding staat bekend als?
Een reizende golf van opwinding staat bekend als?  Sinds 1982 gemiddeld twee weken minder sneeuw in berggebieden
Sinds 1982 gemiddeld twee weken minder sneeuw in berggebieden Nieuwe studie presenteert methode om cyberaanvallen op GPS-apparaten te stoppen
Nieuwe studie presenteert methode om cyberaanvallen op GPS-apparaten te stoppen Maakt het gebrek aan slaap je dik?
Maakt het gebrek aan slaap je dik?  Dodelijke bosbrand omsingelt Turkse elektriciteitscentrale
Dodelijke bosbrand omsingelt Turkse elektriciteitscentrale Grafeenvlokken voor toekomstige transistors
Grafeenvlokken voor toekomstige transistors Studie analyseert wat Amerikaanse burgers ertoe brengt interventie in het buitenland te steunen
Studie analyseert wat Amerikaanse burgers ertoe brengt interventie in het buitenland te steunen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

