
Wetenschap
Lost zout of suiker sneller op in verschillende vloeistoffen?
Temperatuur: Over het algemeen versnelt het verhogen van de temperatuur van de vloeistof het oplossingsproces van zowel zout als suiker. Hogere temperaturen verhogen de kinetische energie van oplosmiddelmoleculen, wat leidt tot een snellere beweging en een groter vermogen om de opgeloste deeltjes uit elkaar te halen en te omringen, waardoor de oplossnelheid wordt verhoogd.
Hoeveelheid opgeloste stof: De oplossnelheid neemt af naarmate de hoeveelheid opgeloste stof in de vloeistof toeneemt. Wanneer er meer opgeloste stof is om op te lossen, moeten de oplosmiddelmoleculen harder werken om de opgeloste deeltjes uit elkaar te halen en te scheiden, wat leidt tot een langzamer oplossingsproces.
Oppervlakte van de opgeloste stof: Hoe groter het oppervlak van de opgeloste stof dat aan het oplosmiddel wordt blootgesteld, hoe sneller de oplossnelheid. Als je bijvoorbeeld zout of suiker in kleinere deeltjes maalt, zorgt het grotere oppervlak ervoor dat meer oplosmiddelmoleculen in contact komen met de opgeloste stof, waardoor een snellere oplossing mogelijk wordt.
Aard van de vloeistof: Verschillende vloeistoffen hebben verschillende mogelijkheden om zout of suiker op te lossen. Water is bijvoorbeeld een universeel oplosmiddel en kan zowel zout als suiker effectief oplossen. Aan de andere kant lossen niet-polaire oplosmiddelen zoals olie of benzine zout of suiker niet goed op. De chemische eigenschappen en moleculaire structuur van de vloeistof spelen een belangrijke rol bij het bepalen van de oplossnelheid.
Over het algemeen lost zout sneller op in water dan suiker, omdat het wordt afgebroken tot kleinere ionen (natrium en chloride) die gemakkelijker worden opgelost door watermoleculen. Aan de andere kant bestaan suikermoleculen uit grotere en complexe structuren die meer tijd en energie van watermoleculen nodig hebben om uiteen te vallen en op te lossen.
Het is belangrijk op te merken dat de exacte oplossnelheden ook afhangen van de specifieke gebruikte vloeistof, evenals van de betrokken zout- of suikerconcentraties.
 Zeer selectief adsorberend materiaal trekt ongewenste stoffen aan om bioproductie ten goede te komen
Zeer selectief adsorberend materiaal trekt ongewenste stoffen aan om bioproductie ten goede te komen Biologische medicijnen maken met spinnenzijde-eiwit
Biologische medicijnen maken met spinnenzijde-eiwit Geminiaturiseerde massaspectrometer voor verkenning van Mars heeft een enorm potentieel
Geminiaturiseerde massaspectrometer voor verkenning van Mars heeft een enorm potentieel Wat is de dichtheid van alliminium?
Wat is de dichtheid van alliminium?  Naar een beter begrip van structuur-metabolismerelaties in humaan aldehydeoxidase (update)
Naar een beter begrip van structuur-metabolismerelaties in humaan aldehydeoxidase (update)
 Pronken:Wilde chimpansees laten voorwerpen aan anderen zien, simpelweg om de aandacht te delen
Pronken:Wilde chimpansees laten voorwerpen aan anderen zien, simpelweg om de aandacht te delen  Bosbranden scheuren door het wijnland van Californië, duizenden vluchten van huis
Bosbranden scheuren door het wijnland van Californië, duizenden vluchten van huis Nieuwe Chinese duikboot bereikt diepste oceaangeul
Nieuwe Chinese duikboot bereikt diepste oceaangeul Boven en buiten megathrusts - aftappende porievloeistoffen dempen aardbevingstrillingen
Boven en buiten megathrusts - aftappende porievloeistoffen dempen aardbevingstrillingen Een duurzaamheidsindicator om de fietsvriendelijkheid van Amerikaanse steden te vergelijken
Een duurzaamheidsindicator om de fietsvriendelijkheid van Amerikaanse steden te vergelijken
Hoofdlijnen
- Wetenschappers leren meer over hoe motoren de wegen van onze cellen manoeuvreren
- Hoe chromosoomuiteinden de cellulaire veroudering beïnvloeden
- Gered Irrawaddy dolfijnkalf sterft ondanks wekenlange zorg
- Onderzoekers identificeren combinatie van factoren voor biologische cacaoopbrengst
- Biologen kijken naar het verleden voor vroege genetische ontwikkeling van kleine spinnen- en insectenogen
- De evolutie van slijm:hoe komen we aan al dit slijm?
- Waar en waarom mensen schaatsen maakten van dierlijke botten
- NASA helpt tijgers, jaguars en olifanten te beschermen – zo doe je dat
- De nadelen van gelelektroforese
- Nieuw metamateriaal biedt herprogrammeerbare eigenschappen

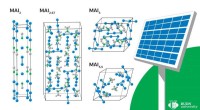
- Chemicus ontwikkelt techniek om zonnecellen te verbeteren
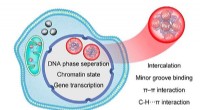
- Moleculair mechanisme van door rutheniumcomplex geïnduceerde DNA-fasescheiding onthuld
- Een moleculaire snaartelefoon aan het werk
- Onderzoekers bouwen robotwetenschapper die al een nieuwe katalysator heeft ontdekt

 Europa wankelt van de ergste overstromingen in jaren terwijl het dodental 120 . overschrijdt
Europa wankelt van de ergste overstromingen in jaren terwijl het dodental 120 . overschrijdt Klimaatverandering bestrijden in de schaduw van de Mount Everest
Klimaatverandering bestrijden in de schaduw van de Mount Everest Libanon laat oude tanks zinken om onderwaterduikpark te creëren
Libanon laat oude tanks zinken om onderwaterduikpark te creëren Een primeur:onderzoekers kwantificeren fotostroomverlies in deeltjesinterface
Een primeur:onderzoekers kwantificeren fotostroomverlies in deeltjesinterface Onderzoekers onthullen een veel rijker beeld van het verleden met nieuwe DNA-hersteltechniek
Onderzoekers onthullen een veel rijker beeld van het verleden met nieuwe DNA-hersteltechniek Welke ionen helpen de pH van speeksel te reguleren?
Welke ionen helpen de pH van speeksel te reguleren?  Geweld tegen Aziatische Amerikanen neemt toe maar racisme is niet nieuw
Geweld tegen Aziatische Amerikanen neemt toe maar racisme is niet nieuw Wat is de juiste uitspraak over bryofyten? A hebben gespecialiseerde weefsels die water geleiden. B. Opgenomen door osmose. C. Zijn niet erg afhankelijk van de D-plantengroep bestaande uit algen en mossen.
Wat is de juiste uitspraak over bryofyten? A hebben gespecialiseerde weefsels die water geleiden. B. Opgenomen door osmose. C. Zijn niet erg afhankelijk van de D-plantengroep bestaande uit algen en mossen.
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

