
Wetenschap
Is het delen van elektronen in polaire covalente bindingen gelijk?
In een polaire covalente binding zal het atoom met de grootste elektronegativiteit de elektronen sterker aantrekken. Dit zal een gedeeltelijke positieve lading creëren op het atoom met de lagere elektronegativiteit en een gedeeltelijke negatieve lading op het atoom met de hogere elektronegativiteit.
Het verschil in elektronegativiteit tussen de twee atomen bepaalt de polariteit van de binding. Hoe groter het verschil in elektronegativiteit, hoe polairder de binding zal zijn.
Polaire covalente bindingen worden in veel moleculen aangetroffen, waaronder water, ammoniak en koolstofdioxide. De polariteit van deze bindingen is belangrijk voor het begrijpen van de eigenschappen van de moleculen. De polariteit van watermoleculen is bijvoorbeeld verantwoordelijk voor de hoge oppervlaktespanning en het vermogen om veel stoffen op te lossen.
 Redactioneel:Vijf jaar na de Overeenkomst van Parijs, de wereld doet nog steeds niet genoeg om klimaatverandering tegen te gaan
Redactioneel:Vijf jaar na de Overeenkomst van Parijs, de wereld doet nog steeds niet genoeg om klimaatverandering tegen te gaan Overmatig gebruik van fosfaatmeststoffen kan microbiële functies verminderen die essentieel zijn voor de gezondheid van gewassen
Overmatig gebruik van fosfaatmeststoffen kan microbiële functies verminderen die essentieel zijn voor de gezondheid van gewassen Geüpgraded waterrisicofilter kan de reactie van bedrijven op waterrisico's helpen transformeren
Geüpgraded waterrisicofilter kan de reactie van bedrijven op waterrisico's helpen transformeren Van New York tot Chili, loodbesmettingsproject ontwikkelt burgerwetenschap
Van New York tot Chili, loodbesmettingsproject ontwikkelt burgerwetenschap Hoe draagt het openbaar vervoer bij aan het milieu?
Hoe draagt het openbaar vervoer bij aan het milieu?
Hoofdlijnen
- Waarom gebruikte je RNA in plaats van DNA om eiwitten te maken?
- Veranderingen in mariene ecosystemen blijven onopgemerkt
- Doorbraak in het begrijpen hoe dodelijke pneumokokken de immuunafweer vermijden
- Een RNA TREAT voor Halloween
- Hoe sperma het genoom van vader uitpakt, zodat het kan samensmelten met dat van moeder
- Hoe langzame spiervezels hun buren overtuigen om zich bij hen aan te sluiten
- Wat heeft Mathias Scheiden bijgedragen aan het onderzoek naar cellen?
- Verschil tussen een eencellige protoctist en bacterie?
- Zooplankton Vs. fytoplankton
- Zijde kan de gevoeligheid verbeteren, flexibiliteit van draagbare lichaamssensoren

- Zijn groene huishoudelijke consumentenproducten minder giftig dan traditionele producten?

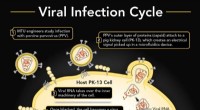
- Microfluidics helpt ingenieurs om virale infectie in realtime te bekijken
- Onderzoekers gebruiken microgolven om tekenen van uitdroging te meten

- Verbetering van de waarneming van eiwitbinding

 Afbeelding:Saturnus binnenstebuiten ringen
Afbeelding:Saturnus binnenstebuiten ringen College.xxx? Scholen kopen pornodomeinen om ze schoon te houden
College.xxx? Scholen kopen pornodomeinen om ze schoon te houden  Een remedie voor koolmonoxidevergiftiging ontgrendelen
Een remedie voor koolmonoxidevergiftiging ontgrendelen Persoonlijkheids- en stemmingswisselingen bij bacteriën
Persoonlijkheids- en stemmingswisselingen bij bacteriën in eerste, SpaceX lanceert gerecyclede raket en ruimteschip (update)
in eerste, SpaceX lanceert gerecyclede raket en ruimteschip (update) Gemodificeerd enzym kan de productie van ethanol van de tweede generatie verhogen
Gemodificeerd enzym kan de productie van ethanol van de tweede generatie verhogen Hoe geodetische koepels werken
Hoe geodetische koepels werken  Slakkenhuizen laten zien dat het hoogbouwplateau veel lager is dan vroeger
Slakkenhuizen laten zien dat het hoogbouwplateau veel lager is dan vroeger
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

