
Wetenschap
Waarom is de netto ionische vergelijking voor fluorwaterstofzuur en kaliumhydroxide dit HF OH- opbrengst H2O vloeistof F- aq niet H waarom f in hf een toeschouwerion andere reacties?
HF(aq) + KOH(aq) → H2O(l) + KF(aq)
Bij deze reactie doneert HF een proton (H+) aan OH- om water (H2O) te vormen. Het fluoride-ion (F-) uit HF en het kaliumion (K+) uit KOH zijn toeschouwerionen, wat betekent dat ze niet deelnemen aan de reactie en onveranderd blijven.
Bij andere reacties gedraagt HF zich mogelijk niet als toeschouwerion. Bij reacties met sterke basen zoals natriumhydroxide (NaOH) kan HF bijvoorbeeld een verdere reactie ondergaan om het hexafluorsilicaation (SiF6 ^ 2-) te vormen. Dit komt omdat het fluoride-ion een zwakke base is en kan reageren met het hydroxide-ion om het stabielere hexafluorsilicaation te vormen.
Daarom hangt het gedrag van HF als toeschouwerion of reactant af van de specifieke reactieomstandigheden en de sterkte van de base waarmee het reageert.
 De reactiviteit van zwarte fosfor reguleren door middel van beschermende chemie
De reactiviteit van zwarte fosfor reguleren door middel van beschermende chemie Wetenschappers ontdekken materiaal dat ideaal is voor slimme fotovoltaïsche ramen
Wetenschappers ontdekken materiaal dat ideaal is voor slimme fotovoltaïsche ramen Video:Waarom stinkende kazen stinken
Video:Waarom stinkende kazen stinken Onderzoekers vereenvoudigen de constructie van kleine structuren druppel voor druppel
Onderzoekers vereenvoudigen de constructie van kleine structuren druppel voor druppel Wat is de partiële stikstofdruk in lucht bij atmosferische druk (1 atm)?
Wat is de partiële stikstofdruk in lucht bij atmosferische druk (1 atm)?
Hoofdlijnen
- Is de tweekamerige geest geëvolueerd om het moderne menselijke bewustzijn te creëren?
- Waarom zijn er geen hyena's in Europa?
- Wat doodt zeeotters? Wetenschappers lokaliseren parasietstam
- Wat is de belangrijkste primaire producent in het mariene ecosysteem?
- Middeleeuwse kist levert fascinerend skelet op
- Het geheim van betere koffie? De vogels en de bijen
- Hoe voorkom je virusuitbraken? Door de diergezondheid te beschermen
- Nieuwe hulpbron legt de innerlijke werking van sorghumplantencellen bloot voor het ontwerpen van betere grondstoffen voor bio-energie
- Wat is een subarachnoïdale bloeding?
- Materialen die opengaan in de hitte van het moment
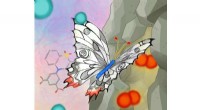
- Fullerenen overbruggen geleidende kloof in organische fotovoltaïsche energie
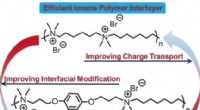
- Wetenschappers lossen een duurzaamheidsprobleem op in brandstofcellen voor waterstofauto's
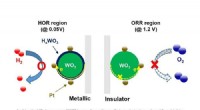
- Precies afstemmen op de dynamiek van upconversion-luminescentie
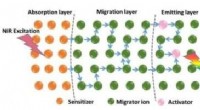
- Nieuwe aanpak voor fotosynthetische productie van koolstofneutrale biobrandstof uit groene algen

 Curtiss Gouden Flyer
Curtiss Gouden Flyer  Poeder, geen gas:een veiliger, effectievere manier om een ster op aarde te creëren
Poeder, geen gas:een veiliger, effectievere manier om een ster op aarde te creëren Hoeveel is 1,09 gram?
Hoeveel is 1,09 gram?  Waarom smelten de gletsjers in het zuidoosten van Tibet zo snel?
Waarom smelten de gletsjers in het zuidoosten van Tibet zo snel?  N-gedoteerde koolstof-ingekapselde overgangsmetaalkatalysatoren om de prestaties van zink-luchtbatterijen te optimaliseren
N-gedoteerde koolstof-ingekapselde overgangsmetaalkatalysatoren om de prestaties van zink-luchtbatterijen te optimaliseren Wat is de basis voor het benoemen van elementen?
Wat is de basis voor het benoemen van elementen?  Volkswagen besteedt 44 miljard euro aan elektrisch offensief
Volkswagen besteedt 44 miljard euro aan elektrisch offensief Hoe experts de ecologische voetafdruk van de Olympische Spelen in Parijs berekenen:83 flessen wijn per persoon
Hoe experts de ecologische voetafdruk van de Olympische Spelen in Parijs berekenen:83 flessen wijn per persoon
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

