
Wetenschap
Welke primaire standaard wordt gebruikt om tegen zoutzuur te titreren?
Na2CO3(aq) + 2HCl(aq) → 2NaCl(aq) + H2O(l) + CO2(g)
Omdat natriumcarbonaat een primaire standaard is, wordt het veel gebruikt voor de nauwkeurige bepaling van de concentratie van HCl-oplossingen. Om de titratie uit te voeren, wordt een bekende massa natriumcarbonaat nauwkeurig afgewogen en opgelost in water. De resulterende oplossing wordt vervolgens langzaam onder voortdurend roeren aan de HCl-oplossing toegevoegd totdat het eindpunt is bereikt.
Het eindpunt van de titratie wordt bepaald met behulp van een indicator, die van kleur verandert als reactie op de pH-verandering. Een veelgebruikte indicator voor de titratie van HCl met natriumcarbonaat is methyloranje, dat van rood naar geel verandert naarmate de pH van de oplossing stijgt. Het equivalentiepunt wordt bereikt wanneer de toegevoegde hoeveelheid natriumcarbonaat stoichiometrisch equivalent is aan de hoeveelheid HCl die in de oplossing aanwezig is.
Door zorgvuldig het volume HCl te registreren dat nodig is om het equivalentiepunt te bereiken, kan de exacte concentratie van de HCl-oplossing nauwkeurig worden berekend. Deze titratiemethode is betrouwbaar, nauwkeurig en kan nauwkeurige resultaten opleveren voor het bepalen van de concentratie van HCl-oplossingen in verschillende analytische en laboratoriumomgevingen.
 Wetenschappers onderzoeken 3D-geprinte legeringen met hoge entropie
Wetenschappers onderzoeken 3D-geprinte legeringen met hoge entropie Wat is het product van een magnesium- en zoutzuurreactie?
Wat is het product van een magnesium- en zoutzuurreactie?  Wanneer een glas water in de zon wordt gelaten, verdwijnt de chemische verandering geleidelijk?
Wanneer een glas water in de zon wordt gelaten, verdwijnt de chemische verandering geleidelijk?  Zullen cyborgs gemaakt worden van melanine? Pigmentdoorbraak maakt biocompatibele elektronica mogelijk
Zullen cyborgs gemaakt worden van melanine? Pigmentdoorbraak maakt biocompatibele elektronica mogelijk Hoe een Desiccant
Hoe een Desiccant
 Succes in de Amazone:minder ontbossing
Succes in de Amazone:minder ontbossing NASA-NOAA-satelliet toont windschering die een veranderende tyfoon Bualoi . beïnvloedt
NASA-NOAA-satelliet toont windschering die een veranderende tyfoon Bualoi . beïnvloedt Copernicus Sentinel-5P ozon verhoogt dagelijkse voorspellingen
Copernicus Sentinel-5P ozon verhoogt dagelijkse voorspellingen Het mobiliseren van wereldwijd kapitaal in de nasleep van een ramp is essentieel voor economisch herstel
Het mobiliseren van wereldwijd kapitaal in de nasleep van een ramp is essentieel voor economisch herstel Plattelandsbewoners in Alaska hebben moeite om toegang te krijgen tot water en dit te betalen
Plattelandsbewoners in Alaska hebben moeite om toegang te krijgen tot water en dit te betalen
Hoofdlijnen
- Hoe de anatomie van een rundvleeshart en een menselijk hart te vergelijken
- Honden kunnen ruiken als ze gestrest zijn, suggereert onderzoek
- Hoe zijn dieren en planten vergelijkbaar?
- Wat zijn de kenmerken die alle bacteriën gemeenschappelijk hebben?
- Waarom zijn de cilia en het slijmvlies belangrijk in het ademhalingssysteem?
- Wat is een homoloog allel?
- Hoe wordt rijst genetisch gemodificeerd?
- Het leefgebied van de panda krimpt, steeds meer gefragmenteerd worden
- Studie decodeert dimerisatie en herkenning van antidepressiva op de noradrenalinetransporteur
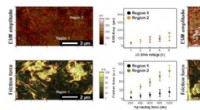
- Visualisatie van functionele componenten om optimale composietelektroden te karakteriseren
- Onderzoekers creëren sterke, snel, waterdichte lijm

- Deponeren van ijzersoorten in ZSM-5 om cyclohexaan te oxideren tot cyclohexanon

- Hoe probiotische bifidobacteriën patiënten met coeliakie kunnen helpen?

- Adsorberend materiaal filtert giftig chroom, arseen uit watervoorraden

 Waarom de stinkende durian echt 'koning van alle vruchten' is
Waarom de stinkende durian echt 'koning van alle vruchten' is  Hoe ruimteliften zullen werken
Hoe ruimteliften zullen werken  PPPL-fysici bouwen diagnose die de plasmasnelheid in realtime meet
PPPL-fysici bouwen diagnose die de plasmasnelheid in realtime meet Waarom het bedrijfsmodel van socialemediagiganten als Facebook onverenigbaar is met mensenrechten
Waarom het bedrijfsmodel van socialemediagiganten als Facebook onverenigbaar is met mensenrechten Bio-geïnspireerd gelmateriaal kan ingenieurs helpen de bewegingen van zachte robots te beheersen
Bio-geïnspireerd gelmateriaal kan ingenieurs helpen de bewegingen van zachte robots te beheersen Wat betekent generatietijd in de microbiologie?
Wat betekent generatietijd in de microbiologie?  Onderzoekers ontwikkelen een methode voor het vergelijken van biologische oppervlakken tussen soorten
Onderzoekers ontwikkelen een methode voor het vergelijken van biologische oppervlakken tussen soorten De rol van algen in het ecosysteem
De rol van algen in het ecosysteem
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

