
Wetenschap
Wat gebeurt er als een zilveren lepel ondergedompeld wordt gehouden in een waterige kopersulfaatoplossing?
Wanneer een zilveren lepel wordt ondergedompeld in een waterige kopersulfaatoplossing, vindt er een verdringingsreactie plaats. Omdat koper reactiever is dan zilver, verdringt het zilver uit de zoutoplossing en wordt het op het oppervlak van de lepel afgezet. Als gevolg hiervan wordt de zilveren lepel bedekt met een laagje koper en begint de blauwe kleur van de kopersulfaatoplossing te vervagen. De chemische reactie die plaatsvindt is:
$$CuSO_4(aq) + 2Ag(s) → 2AgNO_3(aq) + Cu(s)$$
Bij deze reactie vervangen koperatomen de zilveratomen in de kopersulfaatoplossing, waardoor zilvernitraat ontstaat. De koperatomen worden vervolgens op het oppervlak van de zilveren lepel afgezet.
 Een nieuwe manier om hout transparant te maken, sterker en lichter dan glas
Een nieuwe manier om hout transparant te maken, sterker en lichter dan glas Onderzoekers observeren een zeer opgewonden rondzwervende energiebaan in chemische reacties
Onderzoekers observeren een zeer opgewonden rondzwervende energiebaan in chemische reacties  Wat is de chemische formule van het Hinsberg-reagens?
Wat is de chemische formule van het Hinsberg-reagens?  Bij elke chemische reactie zijn de hoeveelheden die behouden blijven:
Bij elke chemische reactie zijn de hoeveelheden die behouden blijven: Wat is de formule van zinkhydroxide?
Wat is de formule van zinkhydroxide?
 Dood graag? De race om natuurfoto’s op sociale media kan ecosystemen verwoesten of tot snelle uitsterving leiden
Dood graag? De race om natuurfoto’s op sociale media kan ecosystemen verwoesten of tot snelle uitsterving leiden  Britten hopen duurzame gewoonten te behouden na COVID-19-lockdown, onderzoek suggereert:
Britten hopen duurzame gewoonten te behouden na COVID-19-lockdown, onderzoek suggereert: Met unieke gegevens, onderzoekers volgen het effect van het Braziliaanse sojamoratorium op een oprukkende landbouwgrens
Met unieke gegevens, onderzoekers volgen het effect van het Braziliaanse sojamoratorium op een oprukkende landbouwgrens Virtuele realiteit zou kunnen dienen als krachtig hulpmiddel voor milieueducatie
Virtuele realiteit zou kunnen dienen als krachtig hulpmiddel voor milieueducatie Krijgen de leerlingen voldoende lucht?
Krijgen de leerlingen voldoende lucht?
Hoofdlijnen
- Hoe Candida albicans zuurstofgebrek exploiteert om ziekten te veroorzaken
- Deal verbiedt val in Colorado, bureau zegt dat het toch niet wordt gebruikt (update)
- Het ruimen van controverses nu de Franse wolvenpopulatie in 2023 afneemt
- Wat is TA Cloning?
- Het orgaansysteem dat ondersteuning en bescherming biedt voor lichaamsdelen is het endocriene of circulatoire skeletale ademhalingssysteem?
- Genregulatie, en niet alleen genen, is wat mensen onderscheidt
- Nieuwe hypothese legt uit hoe menselijke voorouders vuur in hun voordeel gebruikten
- Waarom hebben plantencellen zowel celwanden als celmembranen?
- We weten nu hoe insecten en bacteriën ijs beheersen
- Birnessietstudie biedt inzichten voor elektrochemie, energie opslag

- Wetenschappers ontwikkelen strategie om afzonderlijke atomen te stabiliseren met ionische vloeistof als elektronische stabilisator
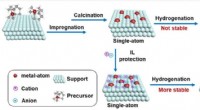
- Op zoek naar de chemie van het leven

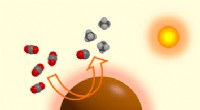
- Elementair boor is een effectieve fotothermokatalysator voor de omzetting van kooldioxide
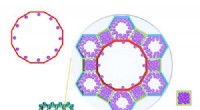
- Realtime analyse van MOF-adsorptiegedrag
 Apollo-rotsmonsters leggen sleutelmomenten vast in de vroege geschiedenis van de manen, studie vinden
Apollo-rotsmonsters leggen sleutelmomenten vast in de vroege geschiedenis van de manen, studie vinden Hoe te meten Vierkante centimeters
Hoe te meten Vierkante centimeters Nieuw onderzoek naar rookpluimen van megabranden maakt duidelijk wat ze bevatten, hoe ze bewegen en wat hun potentiële gevolgen zijn
Nieuw onderzoek naar rookpluimen van megabranden maakt duidelijk wat ze bevatten, hoe ze bewegen en wat hun potentiële gevolgen zijn  Wetenschappers catalogiseren bijna 100 stoffige bolletjes in de Krabnevel
Wetenschappers catalogiseren bijna 100 stoffige bolletjes in de Krabnevel 5 fonkelende sterrenstelsels helpen ons het mysterie van de ontbrekende materie in de Melkweg te ontrafelen
5 fonkelende sterrenstelsels helpen ons het mysterie van de ontbrekende materie in de Melkweg te ontrafelen Inheemse bomen gedijen goed in teakplantages en kunnen het Panamakanaal beschermen
Inheemse bomen gedijen goed in teakplantages en kunnen het Panamakanaal beschermen Het aanpakken van klimaatmigratie binnen de grenzen helpt landen bij het plannen, effecten verzachten
Het aanpakken van klimaatmigratie binnen de grenzen helpt landen bij het plannen, effecten verzachten De kwaliteitsscores van docenten veranderen afhankelijk van de leerlingen, school, studie vondsten
De kwaliteitsscores van docenten veranderen afhankelijk van de leerlingen, school, studie vondsten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

