
Wetenschap
Wat is de PH-waarde van KHCO3?
De pH-waarde van KHCO3 (kaliumbicarbonaat) is afhankelijk van de concentratie van de oplossing. KHCO3 is een zwakke base en wanneer het in water wordt opgelost, ondergaat het een gedeeltelijke dissociatie, waarbij waterstofionen (H+) en bicarbonaationen (HCO3-) vrijkomen. De pH-waarde is een maatstaf voor de concentratie waterstofionen in een oplossing en varieert van 0 tot 14. Een pH-waarde van 7 wordt als neutraal beschouwd, terwijl waarden onder de 7 een zure oplossing aangeven en waarden boven de 7 een basische oplossing.
Voor een 0,1 M oplossing van KHCO3 ligt de pH-waarde doorgaans rond de 8,3–8,4. Dit geeft aan dat de oplossing enigszins basisch is. De exacte pH-waarde kan variëren afhankelijk van de temperatuur en andere factoren. Het is belangrijk op te merken dat de pH-waarde van een oplossing ook kan worden beïnvloed door de aanwezigheid van andere stoffen, zoals zuren of basen.
 De bossen in Ghana worden weggevaagd:wat zit hierachter en waarom pogingen om dit te stoppen niet werken?
De bossen in Ghana worden weggevaagd:wat zit hierachter en waarom pogingen om dit te stoppen niet werken?  Boomsoorten die essentieel zijn voor het herstel van verstoorde tropische bossen
Boomsoorten die essentieel zijn voor het herstel van verstoorde tropische bossen Europese industriële luchtvervuiling kost honderden miljarden:rapport
Europese industriële luchtvervuiling kost honderden miljarden:rapport ‘Er wordt te veel geld uitgegeven aan gevangenissen en politiewerk’:wat Aboriginal-gemeenschappen ons vertelden over de financiering van herinvestering in gerechtigheid
‘Er wordt te veel geld uitgegeven aan gevangenissen en politiewerk’:wat Aboriginal-gemeenschappen ons vertelden over de financiering van herinvestering in gerechtigheid  Terwijl China zijn spieren spant op Antarctica, wetenschap is het beste diplomatieke instrument op het bevroren continent
Terwijl China zijn spieren spant op Antarctica, wetenschap is het beste diplomatieke instrument op het bevroren continent
Hoofdlijnen
- Met uitsterven bedreigde mus in Centraal-Florida die in het wild waarschijnlijk niet zal overleven
- Het echte verschil tussen plantaardige en dierlijke cellen
- Wanneer wordt het inwendige van de cel als isotoon met de omringende vloeistof beschouwd?
- Wat is belangrijk aan laboratoriumapparatuur?
- Bestaat er een wetenschappelijke formule voor grappig?
- Nieuw inzicht in hoe planten cellulose maken
- Hoe seizoensallergieën uw huisdier beïnvloeden
- Wat zijn drie fysieke eigenschappen van een banaan?
- Zijn dieren kwetsbaar voor COVID-19?
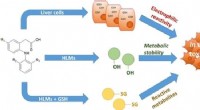
- Subtiele veranderingen in de chemische structuur kunnen de toxiciteit van geneesmiddelen beïnvloeden
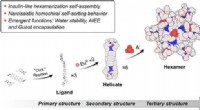
- Hexamere lanthanide-organische capsules met tertiaire structuur, opkomende functies
- Licht pincet kan bewegen, smelten, en verstrooi mysterieuze biologische ijsbergen

- Eencellige test kan precies onthullen hoe medicijnen kankercellen doden

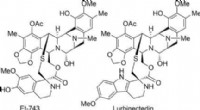
- Totale synthese van mariene antitumormiddelen trabectedine en lurbinectedine
 Wat als koeien niet bestonden?
Wat als koeien niet bestonden?  Mogelijk betaalt u te veel voor advertenties op Google, Bing
Mogelijk betaalt u te veel voor advertenties op Google, Bing De verschillen tussen mannelijke en vrouwelijke spinnen
De verschillen tussen mannelijke en vrouwelijke spinnen Een slimme chemo-enzymatische methode detecteert en verwijdert gevaarlijke fenolen
Een slimme chemo-enzymatische methode detecteert en verwijdert gevaarlijke fenolen Ruimtetelescoop detecteert water in een aantal asteroïden
Ruimtetelescoop detecteert water in een aantal asteroïden Studie suggereert oplossingen voor strafrechtelijke betrokkenheid bij mensen die dakloos zijn, ernstige psychische aandoening
Studie suggereert oplossingen voor strafrechtelijke betrokkenheid bij mensen die dakloos zijn, ernstige psychische aandoening Hoe zullen vracht- en toeleveringsketens er over 20 jaar uitzien? Experts denken na over de scenario's
Hoe zullen vracht- en toeleveringsketens er over 20 jaar uitzien? Experts denken na over de scenario's Koude stofkernen in de centrale zone van de Melkweg
Koude stofkernen in de centrale zone van de Melkweg
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

