
Wetenschap
Ladingsverandering:hoe elektrische krachten variëren in colloïden
De elektrische kracht tussen twee geladen deeltjes wordt gegeven door de wet van Coulomb:
```
F =k * q₁ * q₂ / r²
```
waar:
* F is de elektrische kracht in Newton (N)
* k is de elektrostatische constante (8,988 × 10^9 N m²/C²)
* q₁ en q₂ zijn de ladingen van de twee deeltjes in coulombs (C)
* r is de afstand tussen de twee deeltjes in meters (m)
De elektrische kracht tussen twee colloïdale deeltjes is omgekeerd evenredig met het kwadraat van de afstand ertussen. Dit betekent dat hoe dichter de deeltjes bij elkaar zijn, hoe sterker de elektrische kracht zal zijn.
De elektrische kracht tussen twee geladen deeltjes kan aantrekkelijk of afstotend zijn. Als de deeltjes tegengestelde ladingen hebben, zal de kracht aantrekkelijk zijn. Als de deeltjes dezelfde lading hebben, zal de kracht afstotend zijn.
De elektrische kracht tussen colloïdale deeltjes is een van de factoren die de stabiliteit van een colloïdale dispersie bepaalt. Als de elektrische krachten tussen de deeltjes sterk genoeg zijn, zullen de deeltjes verspreid worden en niet uit de oplossing bezinken. Als de elektrische krachten zwak zijn, zullen de deeltjes aggregeren en uit de oplossing bezinken.
De lading van een colloïdaal deeltje kan worden beïnvloed door een aantal factoren, waaronder de pH van de oplossing, de ionsterkte van de oplossing en de aanwezigheid van oppervlakteactieve stoffen. Door deze factoren te beheersen is het mogelijk de elektrische krachten tussen colloïdale deeltjes en de stabiliteit van colloïdale dispersies te beheersen.
 Onthulling wat de kristalgroei regelt
Onthulling wat de kristalgroei regelt Nieuw groen oplosmiddel kan onze lucht helpen zuiveren
Nieuw groen oplosmiddel kan onze lucht helpen zuiveren Wetenschappers isoleren kankerstamcellen met behulp van nieuwe methode
Wetenschappers isoleren kankerstamcellen met behulp van nieuwe methode Wetenschappers analyseren structuur, mechanisme van faageiwit dat elektronen steelt
Wetenschappers analyseren structuur, mechanisme van faageiwit dat elektronen steelt De C-H-bindingen in koolwaterstoffen verbreken om complexe organische moleculen te synthetiseren
De C-H-bindingen in koolwaterstoffen verbreken om complexe organische moleculen te synthetiseren
 Klimaatverandering brengt de beschikbaarheid van essentiële hernieuwbare energiebronnen in gevaar, zo blijkt uit onderzoek
Klimaatverandering brengt de beschikbaarheid van essentiële hernieuwbare energiebronnen in gevaar, zo blijkt uit onderzoek Hoe kan de oceaan ons schone energie geven?
Hoe kan de oceaan ons schone energie geven?  Hoe vogelkoppels met meerdere soorten zich gedragen als K-pop-groepen
Hoe vogelkoppels met meerdere soorten zich gedragen als K-pop-groepen  Stijgende temperaturen kunnen gewasvoeding beschermen als klimaatveranderingen
Stijgende temperaturen kunnen gewasvoeding beschermen als klimaatveranderingen Define Chemical Pollution
Define Chemical Pollution
Hoofdlijnen
- Hoe fluctuerende zuurstofniveaus de evolutie van dieren kunnen hebben versneld
- Wanneer afscheid nemen? Enquête werpt licht op moeilijke beslissingen voor hondenbezitters
- Spechten vertonen tekenen van mogelijke hersenbeschadiging, maar dat is misschien geen slechte zaak
- In Ethiopië identificeren wetenschappers een fossiele otter ter grootte van een leeuw
- Bijen zijn verbazingwekkend goed in het nemen van beslissingen – en ons computermodel legt uit hoe dat mogelijk is
- Wat zijn enkele veel voorkomende toepassingen van gist?
- Het geheim van de winterslaap van schildpadden is de billenademhaling
- Tabaksplanten als levensredders
- Wat gebeurt er als een kind wordt geboren met een extra chromosoom in het 23e paar?
- Doorbraak metaalionen leidt tot nieuwe biomaterialen

- Een licht schijnen op de vreemde wereld van diwaterstoffosfaatanionen
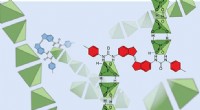
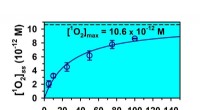
- Geabsorbeerde fotonen door 2-oxocarbonzuren omzetten in zeer reactieve singlet-zuurstof
- Forensisch chemicus stelt zweetteststrip voor als vervanging voor ademanalyse

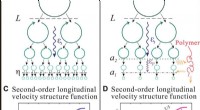
- Experimentele observatie van de schaal van het elastische bereik in turbulente stroming met polymeeradditieven
 Optische telescopen verkrijgen langetermijnmonitoringsresultaten van fluxvariabiliteit in blazars
Optische telescopen verkrijgen langetermijnmonitoringsresultaten van fluxvariabiliteit in blazars Subductie kan minder water recyclen dan gedacht
Subductie kan minder water recyclen dan gedacht Studie neemt bezorgdheid over radioactiviteit in migrerende zeevruchten weg
Studie neemt bezorgdheid over radioactiviteit in migrerende zeevruchten weg Wetenschappers maken verbluffende 3D-akoestische hologrammen
Wetenschappers maken verbluffende 3D-akoestische hologrammen  Wat de watercrisis van Flint zou kunnen betekenen voor de rest van het land
Wat de watercrisis van Flint zou kunnen betekenen voor de rest van het land  MAXI J1348-630 is een zwart gat X-ray binaire, observaties suggereren:
MAXI J1348-630 is een zwart gat X-ray binaire, observaties suggereren: Menselijk gedrag modelleren met Airbnb
Menselijk gedrag modelleren met Airbnb Alle factoren van een getal snel en gemakkelijk vinden
Alle factoren van een getal snel en gemakkelijk vinden
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

