
Wetenschap
Heeft deze chemische reactie de bouwstenen van het leven op aarde gecreëerd?

Hoe begon het leven? Hoe creëerden chemische reacties op de vroege aarde complexe, zichzelf replicerende structuren die zich ontwikkelden tot levende wezens zoals wij die kennen?
Volgens één denkrichting bestond er vóór het huidige tijdperk van op DNA gebaseerd leven een soort molecuul dat RNA (of ribonucleïnezuur) werd genoemd.
RNA – dat vandaag de dag nog steeds een cruciaal onderdeel van het leven is – kan zichzelf repliceren en andere chemische reacties katalyseren.
Maar RNA-moleculen zelf zijn gemaakt van kleinere componenten die ribonucleotiden worden genoemd. Hoe zouden deze bouwstenen zich op de vroege aarde hebben gevormd en vervolgens zijn samengevoegd tot RNA?
Chemici zoals ik proberen de keten van reacties na te bootsen die nodig is om RNA te vormen aan het begin van het leven, maar dat is een uitdagende taak. We weten dat welke chemische reactie dan ook die ribonucleotiden veroorzaakte, moet kunnen plaatsvinden in de rommelige, gecompliceerde omgeving die miljarden jaren geleden op onze planeet werd aangetroffen.
Ik heb onderzocht of "autokatalytische" reacties een rol kunnen hebben gespeeld. Dit zijn reacties die chemicaliën produceren die ervoor zorgen dat dezelfde reactie opnieuw plaatsvindt, wat betekent dat ze zichzelf in een breed scala van omstandigheden in stand kunnen houden.
In ons nieuwste werk gepubliceerd in Chemical Science hebben mijn collega's en ik autokatalyse geïntegreerd in een bekende chemische route voor het produceren van de bouwstenen van ribonucleotiden, wat plausibel had kunnen gebeuren met de eenvoudige moleculen en complexe omstandigheden die op de vroege aarde werden aangetroffen.
De formose-reactie
Autokatalytische reacties spelen een cruciale rol in de biologie, van het reguleren van onze hartslag tot het vormen van patronen op schelpen. In feite is de replicatie van het leven zelf, waarbij één cel voedingsstoffen en energie uit de omgeving opneemt om twee cellen te produceren, een bijzonder ingewikkeld voorbeeld van autokatalyse.
Een chemische reactie genaamd de formose-reactie, voor het eerst ontdekt in 1861, is een van de beste voorbeelden van een autokatalytische reactie die op de vroege aarde had kunnen plaatsvinden.
In wezen begint de formose-reactie met één molecuul van een eenvoudige verbinding genaamd glycolaldehyde (gemaakt van waterstof, koolstof en zuurstof) en eindigt met twee. Het mechanisme is afhankelijk van een constante aanvoer van een andere eenvoudige verbinding, formaldehyde genaamd.
Een reactie tussen glycolaldehyde en formaldehyde maakt een groter molecuul, waarbij fragmenten worden afgesplitst die terugvloeien naar de reactie en deze gaande houden. Zodra het formaldehyde echter op is, stopt de reactie en beginnen de producten af te breken van complexe suikermoleculen tot teer.
De formose-reactie deelt enkele gemeenschappelijke ingrediënten met een bekende chemische route om ribonucleotiden te maken, bekend als de Powner-Sutherland-route. Tot nu toe heeft echter niemand geprobeerd de twee met elkaar in verband te brengen – met goede reden.
De formele reactie staat erom bekend dat ze 'niet-selectief' is. Dit betekent dat het veel nutteloze moleculen produceert naast de eigenlijke producten die je wilt.
Een autokatalytische wending in de route naar ribonucleotiden
In onze studie probeerden we een ander eenvoudig molecuul, cyanamide genaamd, aan de formose-reactie toe te voegen. Dit maakt het mogelijk dat sommige van de moleculen die tijdens de reactie worden gemaakt, worden "overgeheveld" om ribonucleotiden te produceren.
De reactie produceert nog steeds geen grote hoeveelheid ribonucleotide-bouwstenen. De producten die wel geproduceerd worden, zijn echter stabieler en zullen minder snel verslechteren.
Wat interessant is aan onze studie is de integratie van de formosereactie en de productie van ribonucleotiden. In eerdere onderzoeken is elk afzonderlijk onderzocht, wat weerspiegelt hoe scheikundigen gewoonlijk denken over het maken van moleculen.
Over het algemeen hebben scheikundigen de neiging complexiteit te vermijden om de kwantiteit en zuiverheid van een product te maximaliseren. Deze reductionistische benadering kan ons er echter van weerhouden dynamische interacties tussen verschillende chemische routes te onderzoeken.
Deze interacties, die overal in de echte wereld buiten het laboratorium plaatsvinden, vormen misschien wel de brug tussen chemie en biologie.
Industriële toepassingen
Autokatalyse kent ook industriële toepassingen. Wanneer je cyanamide aan de formose-reactie toevoegt, is een ander product een verbinding genaamd 2-aminooxazol, die wordt gebruikt in scheikundig onderzoek en de productie van veel farmaceutische producten.
Bij de conventionele productie van 2-aminooxazool wordt vaak gebruik gemaakt van cyanamide en glycolaldehyde, waarvan de laatste duur is. Als het kan worden gemaakt met behulp van de formose-reactie, is er slechts een kleine hoeveelheid glycolaldehyde nodig om de reactie op gang te brengen, waardoor de kosten worden verlaagd.
Ons laboratorium optimaliseert momenteel deze procedure in de hoop dat we de autokatalytische reactie kunnen manipuleren om gewone chemische reacties goedkoper en efficiënter te maken, en hun farmaceutische producten toegankelijker. Misschien zal het niet zo'n groot probleem zijn als het creëren van leven zelf, maar we denken dat het nog steeds de moeite waard kan zijn.
Meer informatie: Quoc Phuong Tran et al., Op weg naar een prebiotische synthese van chemoton-nucleotideprecursoren, aangedreven door de autokatalytische formose-reactie, Chemische Wetenschap (2023). DOI:10.1039/D3SC03185C
Journaalinformatie: Chemische Wetenschap
Aangeboden door The Conversation
Dit artikel is opnieuw gepubliceerd vanuit The Conversation onder een Creative Commons-licentie. Lees het originele artikel. 
 Enzym ontdekt in de darm kan leiden tot nieuwe biomarker voor ziekten
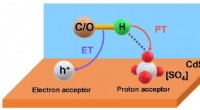
Enzym ontdekt in de darm kan leiden tot nieuwe biomarker voor ziekten Mechanisme van zuurstofactivering op bariumbevattende perovskietmaterialen
Mechanisme van zuurstofactivering op bariumbevattende perovskietmaterialen Theoretische opbrengst berekenen
Theoretische opbrengst berekenen Slimme truc maakt 20 keer snellere beeldvorming mogelijk met elektronenmicroscopie
Slimme truc maakt 20 keer snellere beeldvorming mogelijk met elektronenmicroscopie Klik... Resistente bacteriën op heterdaad betrapt
Klik... Resistente bacteriën op heterdaad betrapt
 Microscopische defecten in het ijs beïnvloeden de manier waarop enorme gletsjers stromen, zo blijkt uit onderzoek
Microscopische defecten in het ijs beïnvloeden de manier waarop enorme gletsjers stromen, zo blijkt uit onderzoek  Als mensen inkrimpen tot tiny houses, ze nemen een milieuvriendelijkere levensstijl aan
Als mensen inkrimpen tot tiny houses, ze nemen een milieuvriendelijkere levensstijl aan Waterstof is een van de toekomstige bestuurders van stookolie en milieuactivisten kunnen beide steunen
Waterstof is een van de toekomstige bestuurders van stookolie en milieuactivisten kunnen beide steunen Een Bobcat ontwijken
Een Bobcat ontwijken Vijf doden en drie vermisten na Franse weekendstormen
Vijf doden en drie vermisten na Franse weekendstormen
Hoofdlijnen
- Voor melkveehouders, waar blijft de tijd?
- Studie suggereert nieuw mechanisme voor lipidetransporter
- Parasitaire worm speelt waarschijnlijk een rol bij de achteruitgang van elandpopulaties
- Een spinnenzijde-geluidssysteem:webben passen bij de akoestische deeltjessnelheid voor geluidsdetectie over lange afstanden
- Sommige planten kunnen de toxische effecten van metalen kortsluiten. Nu proberen wetenschappers hun kracht te benutten
- Onderzoek toont aan dat plantengroeiregulatoren gunstig kunnen zijn voor de vestiging van uien, productie
- Welke soorten moleculen katalyseren RNA-splitsing?
- Wetenschappers winnen de World Food Prize voor hun werk aan de Global Seed Vault
- Studie koppelt koudwaterschok aan catastrofale instorting van koraal in de oostelijke Stille Oceaan
- Voor fotokatalysatoren, de tand des tijds doorstaan betekent een perfecte partner vinden

- Wetenschapper lost een van de heilige gralen van de fysische chemie op na 17 jaar onderzoek

- Nieuwe methode stimuleert de vorming van syngas uit biopolyolen
- Nieuwe chemie voor het regelen van het vloeistofvolume in volumetrische additieve productie
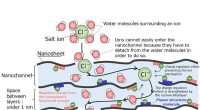
- Zeer functioneel membraan ontwikkeld voor de productie van zoetwater uit zeewater
 Welke celwanden zijn samengesteld uit chitine?
Welke celwanden zijn samengesteld uit chitine?  Air France zegt de capaciteit de komende twee maanden tussen 70 en 90% te verminderen
Air France zegt de capaciteit de komende twee maanden tussen 70 en 90% te verminderen Venezolaanse communicatiesatelliet buiten dienst
Venezolaanse communicatiesatelliet buiten dienst Nederlander zwemt epische schaatsbaan bedreigd door klimaatverandering
Nederlander zwemt epische schaatsbaan bedreigd door klimaatverandering Regelvolgende moleculen bieden de eerste directe bevestiging van een theorie van een halve eeuw oud
Regelvolgende moleculen bieden de eerste directe bevestiging van een theorie van een halve eeuw oud De maan helpt de geheimen van het universum te onthullen
De maan helpt de geheimen van het universum te onthullen Smeltende permafrost verhoogt het broeikasgas uit Arctische meren
Smeltende permafrost verhoogt het broeikasgas uit Arctische meren Geïntegreerde sensor kan de behandeling van hersenaneurysma's volgen
Geïntegreerde sensor kan de behandeling van hersenaneurysma's volgen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

