
Wetenschap
Licht gebruiken om medicijnen en plastics efficiënter te produceren
Iedereen die op conventionele wijze medicijnen, kunststoffen of kunstmest wil produceren, heeft warmte nodig voor chemische reacties – maar dat geldt niet voor de fotochemie, waar licht de energie levert. Ook het proces om tot het gewenste product te komen kent vaak minder tussenstappen.
Onderzoekers van de Universiteit van Basel gaan nu een stap verder en laten zien hoe de energie-efficiëntie van fotochemische reacties tienvoudig kan worden verhoogd. Duurzamere en kosteneffectievere toepassingen liggen nu verleidelijk dichtbij.
Industriële chemische reacties vinden meestal plaats in verschillende fasen tussen verschillende tussenproducten. Fotochemie maakt sluiproutes mogelijk, waardoor er minder tussenstappen nodig zijn. Met fotochemie kun je ook met minder gevaarlijke stoffen werken dan in de conventionele chemie, omdat licht een reactie teweegbrengt in stoffen die niet goed reageren onder hitte. Tot nu toe zijn er echter nog niet veel industriële toepassingen voor fotochemie geweest, deels omdat het leveren van energie met licht vaak inefficiënt is of ongewenste bijproducten creëert.
De onderzoeksgroep onder leiding van professor Oliver Wenger aan de Universiteit van Basel beschrijft nu een fundamenteel principe dat een onverwacht sterke impact heeft op de energie-efficiëntie van fotochemie en de snelheid van fotochemische reacties kan verhogen. Hun resultaten worden gepubliceerd in Nature Chemistry .
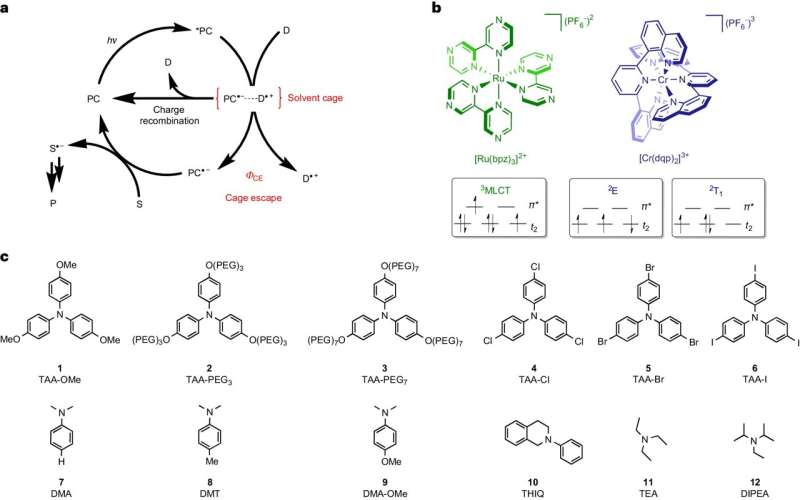
Bij dit soort reacties bevinden de uitgangsmoleculen zich in een vloeibare oplossing. Als ze energie ontvangen in de vorm van licht, kunnen ze elektronen met elkaar uitwisselen en radicalen vormen. Deze extreem reactieve moleculen komen altijd in paren voor en blijven omgeven door oplosmiddel, dat de paren radicalen als een soort kooi omsluit.
Om ervoor te zorgen dat de radicalen kunnen blijven reageren op de gewenste doelproducten, moeten ze uit deze kooi ‘uitbreken’ en daarbuiten een reactiepartner vinden. Het team rond Wenger en zijn postdoc Dr. Cui Wang identificeerde dit uitbraakproces als een beslissende stap die de energie-efficiëntie en de snelheid van fotochemische reacties beperkt.
Radicalen breken los
Zolang de radicalen paarsgewijs in de oplosmiddelkooi blijven, kunnen ze spontaan weer met elkaar reageren tot de uitgangsmaterialen. Deze omgekeerde reactie verspilt energie omdat alleen het reeds geabsorbeerde licht wordt gebruikt om terug te keren naar het startpunt.
Het Bazelse team kon deze omgekeerde reactie vertragen en de radicalen daardoor meer tijd geven om de kooi te verlaten. Hoe langer de ongewenste omgekeerde reactie werd, des te meer radicalen konden uitbreken en des te energiezuiniger en sneller de gewenste doelproducten zich ontwikkelden.
Wang, die nu de functie van assistent-professor bekleedt aan de Universiteit van Osnabrück, gebruikte in haar onderzoek twee specifieke kleurstoffen, die beide licht absorberen en de energie ervan gedurende een korte periode opslaan voordat ze deze gebruiken om radicalenparen te vormen. Eén van de twee onderzochte kleurstoffen was echter in staat aanzienlijk meer energie op te slaan dan de andere en deze over te dragen aan de radicalen.
Dankzij de extra energie konden de radicalen de oplosmiddelkooi tot tien keer efficiënter verlaten. Bijgevolg worden de doelproducten geproduceerd met een tot tien keer hogere energie-efficiëntie. "Dit directe verband tussen de radicalen die uit de oplosmiddelkooi breken en de efficiënte vorming van de doelproducten is verbazingwekkend duidelijk", aldus Wang.
De belangrijkste bevinding is dat bepaalde kleurstoffen meer radicalen kunnen afgeven dan andere, afhankelijk van de hoeveelheid geabsorbeerd licht. "De keuze van de kleurstof kan worden gebruikt om de energie-efficiëntie van fotochemische reacties te vergroten", aldus Wenger. Op zijn beurt stelt hij dat energie-efficiëntie ook een doorslaggevend criterium is voor het industriële gebruik van fotochemie.