
Wetenschap
Gesimuleerde chemie:nieuw AI-platform ontwerpt de kankermedicijnen van morgen
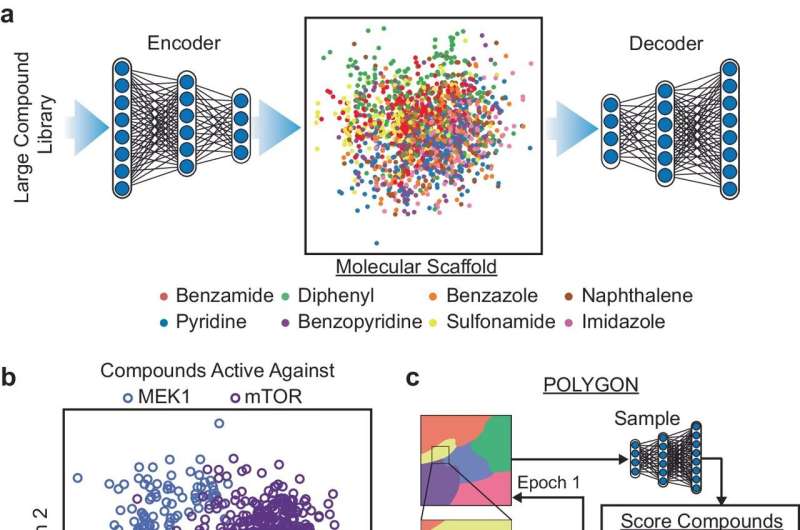
Wetenschappers van UC San Diego hebben een machine learning-algoritme ontwikkeld om de tijdrovende chemie te simuleren die betrokken is bij de vroegste fasen van de ontdekking van geneesmiddelen. Dit zou het proces aanzienlijk kunnen stroomlijnen en deuren kunnen openen voor nog nooit eerder vertoonde behandelingen.
Het identificeren van kandidaat-geneesmiddelen voor verdere optimalisatie omvat doorgaans duizenden individuele experimenten, maar het nieuwe kunstmatige intelligentieplatform (AI) zou potentieel in een fractie van de tijd dezelfde resultaten kunnen opleveren. De onderzoekers gebruikten de nieuwe tool, beschreven in Nature Communications , om 32 nieuwe kandidaat-medicijnen tegen kanker te synthetiseren.
De technologie maakt deel uit van een nieuwe maar groeiende trend in de farmaceutische wetenschap waarbij AI wordt gebruikt om de ontdekking en ontwikkeling van geneesmiddelen te verbeteren.
“Een paar jaar geleden was AI een vies woord in de farmaceutische industrie, maar nu is de trend absoluut het tegenovergestelde:biotech-startups vinden het moeilijk om geld in te zamelen zonder AI in hun bedrijfsplan aan te pakken”, zegt senior auteur Trey Ideker, professor. in de afdeling Geneeskunde van de UC San Diego School of Medicine en adjunct-professor bio-ingenieur en computerwetenschappen aan de UC San Diego Jacobs School of Engineering.
"AI-gestuurde ontdekking van geneesmiddelen is een zeer actief gebied in de industrie geworden, maar in tegenstelling tot de methoden die in bedrijven worden ontwikkeld, maken we onze technologie open source en toegankelijk voor iedereen die deze wil gebruiken."
Het nieuwe platform, genaamd POLYGON, is uniek onder de AI-tools voor het ontdekken van geneesmiddelen, omdat het moleculen met meerdere doelwitten kan identificeren, terwijl bestaande protocollen voor het ontdekken van geneesmiddelen momenteel prioriteit geven aan therapieën met één doel. Multi-target medicijnen zijn van groot belang voor artsen en wetenschappers vanwege hun potentieel om dezelfde voordelen te bieden als combinatietherapie, waarbij verschillende medicijnen samen worden gebruikt om kanker te behandelen, maar met minder bijwerkingen.
"Het kost vele jaren en miljoenen dollars om een nieuw medicijn te vinden en te ontwikkelen, vooral als het gaat om een medicijn met meerdere doelwitten", zegt Ideker. "De zeldzame paar multi-target medicijnen die we hebben, zijn grotendeels bij toeval ontdekt, maar deze nieuwe technologie zou kunnen helpen het toeval uit de weg te ruimen en een nieuwe generatie precisiegeneeskunde op gang te brengen."
De onderzoekers trainden POLYGON op een database van meer dan een miljoen bekende bioactieve moleculen die gedetailleerde informatie bevatten over hun chemische eigenschappen en bekende interacties met eiwitdoelen. Door te leren van patronen uit de database kan POLYGON originele chemische formules genereren voor nieuwe kandidaat-geneesmiddelen die waarschijnlijk bepaalde eigenschappen hebben, zoals het vermogen om specifieke eiwitten te remmen.
"Net zoals AI nu erg goed is in het genereren van originele tekeningen en afbeeldingen, zoals het maken van afbeeldingen van menselijke gezichten op basis van gewenste eigenschappen zoals leeftijd of geslacht, kan POLYGON originele moleculaire verbindingen genereren op basis van gewenste chemische eigenschappen", aldus Ideker.
"In dit geval vertellen we de AI niet hoe oud we willen dat ons gezicht eruitziet, maar vertellen we hoe we willen dat ons toekomstige medicijn interageert met ziekte-eiwitten."
Om POLYGON op de proef te stellen, gebruikten de onderzoekers het om honderden kandidaat-geneesmiddelen te genereren die zich richten op verschillende paren kankergerelateerde eiwitten.
Hiervan synthetiseerden de onderzoekers 32 moleculen die de sterkst voorspelde interacties hadden met de MEK1- en mTOR-eiwitten, een paar cellulaire signaaleiwitten die een veelbelovend doelwit zijn voor kankercombinatietherapie. Deze twee eiwitten zijn wat wetenschappers synthetisch dodelijk noemen, wat betekent dat het remmen van beide eiwitten samen genoeg is om kankercellen te doden, zelfs als het remmen van één alleen dat niet is.
De onderzoekers ontdekten dat de medicijnen die ze synthetiseerden een significante activiteit hadden tegen MEK1 en mTOR, maar weinig off-target-reacties hadden met andere eiwitten. Dit suggereert dat een of meer van de door POLYGON geïdentificeerde geneesmiddelen mogelijk beide eiwitten kunnen targeten als kankerbehandeling, wat een lijst met keuzes oplevert die door menselijke chemici kan worden verfijnd.
"Als je eenmaal de kandidaat-geneesmiddelen hebt, moet je nog steeds alle andere chemie uitvoeren die nodig is om die opties te verfijnen tot één enkele, effectieve behandeling", aldus Ideker. "We kunnen en mogen niet proberen de menselijke expertise uit de pijplijn voor het ontdekken van geneesmiddelen te elimineren, maar wat we wel kunnen doen is een paar stappen van het proces inkorten."
Ondanks deze voorzichtigheid zijn de onderzoekers optimistisch dat de mogelijkheden van AI voor de ontdekking van geneesmiddelen nog maar net worden onderzocht.
"Het zal heel spannend zijn om te zien hoe dit concept zich de komende tien jaar zal ontwikkelen, zowel in de academische wereld als in de particuliere sector", aldus Ideker. "De mogelijkheden zijn vrijwel eindeloos."