
Wetenschap
Door de natuur geïnspireerde proteïne kan helpen bij de plasticplaag
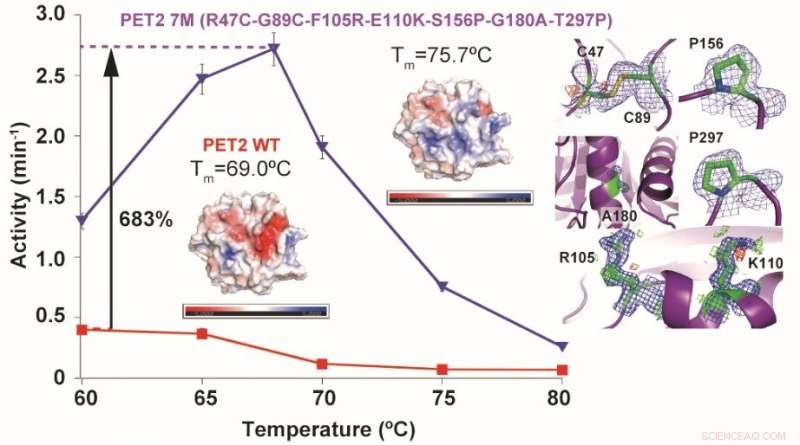
Mutaties van een PET-hydrolyserend enzym PET2 resulteerden in een 6,7 graden C toename in thermische stabiliteit en een 6,8-voudige toename in PET-hydrolytische activiteit. t m staat voor smelt (denaturatie) temperatuur en kleuren op enzymstructuren tonen hun oppervlakteladingen (blauw:positief, rood:negatief). Krediet:NINS/IMS
Goedkoop om te produceren en lang te degraderen, plastic was ooit een fabricagewonder. Nutsvoorzieningen, plastic is een milieuplaag, verstopping van stortplaatsen en verstikking van waterwegen. Een in Japan gevestigd onderzoeksteam is teruggekeerd naar de natuur om een aanpak te ontwikkelen om de hardnekkige stof af te breken. Vergelijkbaar met hoe een eiwit zich bindt aan cellulose in planten of aan chitine in schaaldieren om ontbinding te initiëren, een gemanipuleerd eiwit is op weg om zich te binden aan plastic deeltjes in een poging ze efficiënter af te breken.
Ze publiceerden hun resultaten op 29 juni in ACS Katalyse .
"Polyethyleentereftalaat (PET) wordt in de moderne samenleving in grote hoeveelheden geproduceerd en gebruikt vanwege de lage kosten en het gemak van verwerking, " zei papier auteur Ryota Iino, hoogleraar van het Instituut voor Moleculaire Wetenschappen (IMS) in de National Institutes of Natural Sciences (NINS). "Echter, in recente jaren, vanuit het perspectief van het realiseren van een duurzame samenleving, de volledige recycling van PET in de industrie en de verwijdering van PET uit de natuurlijke omgeving zijn mondiale vraagstukken geworden. Om deze problemen op te lossen, het is erg belangrijk om te begrijpen hoe PET efficiënt kan worden afgebroken."
De onderzoekers onderzochten en ontwikkelden een enzym dat was gekloond uit een bibliotheek van genetisch materiaal dat uit de natuur was verzameld. Dit enzym, PET2 genaamd, bleek de afbraak van PET te vergemakkelijken door de reactie tussen de chemische componenten van PET en water te versnellen.
Met behulp van beeldvormingsanalyse met één molecuul, het team ontdekte dat de manier waarop het enzym zich aan het oppervlak van PET bindt, de afbraaksnelheid feitelijk beperkt.
"We hebben ook onthuld dat door positieve ladingen op het oppervlak van PET-afbrekend enzym te introduceren, de bindingssnelheid aan het PET-oppervlak kan worden verhoogd, ' zei Iino.
De positieve ladingen reageren gunstig op het PET-oppervlak, dus meer van het enzym kan het PET binden en effectiever afbreken. De onderzoekers ontdekten ook dat, hoewel ontwikkeld PET2 een hoge thermische stabiliteit en hoogste activiteit vertoonde bij 68 graden Celsius - iets lager dan de meeste huishoudelijke keukenovens kunnen gaan - het effectiever kan zijn bij hogere temperaturen waar de moleculaire bindingen van PET flexibeler en breekbaarder worden.
"Ons uiteindelijke doel is om een bacterie te maken die PET in de omgeving kan waarnemen, ga er naar toe, en degraderen, " zei Iino. Zo'n bacterie zou dan het gedegradeerde PET kunnen omzetten in energie die nuttig is voor andere organismen, effectief optreden als een geautomatiseerd recyclingcentrum voor plastic. "In de natuur, chitine en cellulose worden op deze manier gerecycled."
Iino is ook verbonden aan de School of Physical Sciences van The Graduate University for Advanced Studies (SOKENDAI). Andere bijdragers zijn onder meer Akihiko Nakamura, Vakgroep Toegepaste Levenswetenschappen, Faculteit Landbouw, Shizuoka-universiteit, en het Shizuoka Instituut voor de Studie van Mariene Biologie en Chemie; en Naoya Kobayashi en Nobuyasu Koga, Exploratory Research Centre on Life and Living Systems (ExCELLS), NINS. Koga is ook aangesloten bij IMS, NINS, en SOKENDAI.
Het toonaangevende initiatief voor excellente jonge onderzoekers, het ministerie van Onderwijs, Cultuur, Sport, Wetenschap, en technologie van Japan, Stichting Sumitomo, en het ExCELLS Special Collaboration Program ondersteunde dit onderzoek.
 Nieuwe techniek maakt snelle screening op nieuwe typen zonnecellen mogelijk
Nieuwe techniek maakt snelle screening op nieuwe typen zonnecellen mogelijk Wetenschappers onderzoeken elektronische eigenschappen van vloeibare elektrolyten voor energietechnologieën
Wetenschappers onderzoeken elektronische eigenschappen van vloeibare elektrolyten voor energietechnologieën Verschil tussen Atomen & Ionen
Verschil tussen Atomen & Ionen  Zuivere brandstof uit zonlicht halen
Zuivere brandstof uit zonlicht halen Galvaniseren:de geboorte van een enkele kern vastgelegd in de camera
Galvaniseren:de geboorte van een enkele kern vastgelegd in de camera
 Microvervuiling die China en Zuid-Azië teistert:studie
Microvervuiling die China en Zuid-Azië teistert:studie Honderden vluchten vertraagd door mist die Noord-India overspoelt
Honderden vluchten vertraagd door mist die Noord-India overspoelt Luchtradar onthult grondwater onder gletsjer
Luchtradar onthult grondwater onder gletsjer Wetenschappers vinden geoxideerd ijzer diep in het binnenste van de aarde (update)
Wetenschappers vinden geoxideerd ijzer diep in het binnenste van de aarde (update) Dieren in het regenwoud die strijden om hetzelfde voedsel
Dieren in het regenwoud die strijden om hetzelfde voedsel
Hoofdlijnen
- Antibioticaresistentie:onderzoekers slagen erin resistentiegenen te blokkeren
- Wanneer treedt melkzuurfermentatie op?
- Zijn mannelijke Y-chromosomen korter dan X-chromosomen?
- Epigenetica: definitie, hoe het werkt, voorbeelden
- De zeeschildpad die weigerde te worden geslagen door de storm
- Team onthult hoge prevalentie van bacteriën die gen mcr-1 dragen in ecosysteem
- Hoe soorten versteend hout te identificeren
- De illegale schildpaddenhandel - waarom wetenschappers geheimen bewaren
- Welke soorten organische moleculen vormen een celmembraan?
- De kracht van zwavel ontsluiten in toekomstig medicijnontwerp

- Milieuvriendelijke productie van geneesmiddelen Nobelprijswinnaars meest trotse prestatie

- Waarom scheren zelfs de scherpste scheermessen dof maakt

- Koelgordijn gemaakt van een poreus drielaags membraan - alternatief voor elektrisch aangedreven airconditioning

- Nieuw polymeer kan de prestaties van organische en perovskiet-zonnecellen verbeteren

 NASA zet eerste stappen in de richting van supersnel internet in de ruimte
NASA zet eerste stappen in de richting van supersnel internet in de ruimte Hogere temperaturen kunnen koraalriffen helpen beschermen
Hogere temperaturen kunnen koraalriffen helpen beschermen LEGO-techniek onthult de fysica van DNA-transport door nanoporiën
LEGO-techniek onthult de fysica van DNA-transport door nanoporiën Astronomen vinden regelmatige ritmes tussen pulserende sterren
Astronomen vinden regelmatige ritmes tussen pulserende sterren Grafeen op boornitride kan leiden tot doorbraak in microchiptechnologie
Grafeen op boornitride kan leiden tot doorbraak in microchiptechnologie Zelfrijdende auto's dwingen steden om slim te worden
Zelfrijdende auto's dwingen steden om slim te worden Blauwe wervelvlamstructuur onthuld met supercomputers
Blauwe wervelvlamstructuur onthuld met supercomputers Nieuw nanodeeltje ontwikkeld voor intraveneuze kankerimmunotherapie
Nieuw nanodeeltje ontwikkeld voor intraveneuze kankerimmunotherapie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

