
Wetenschap
Onderzoekers identificeren post-translationele vorming van gespannen cyclofanen in bacteriën
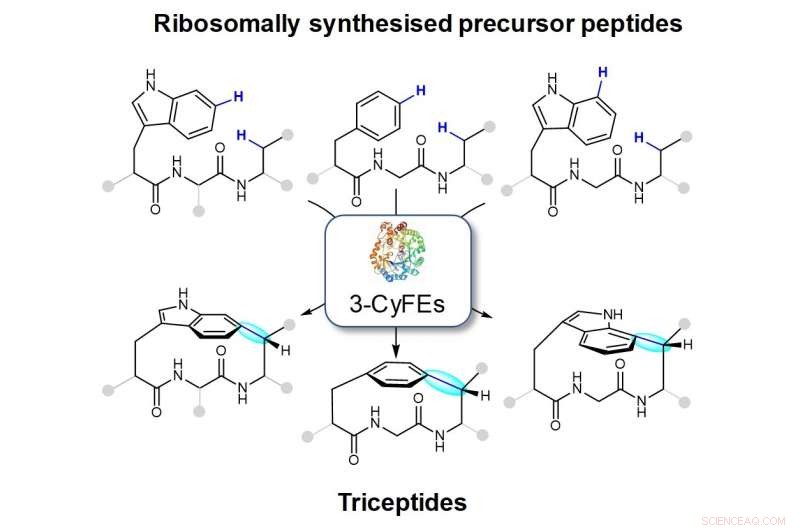
Figuur toont macrocycli die worden gecreëerd door de cyclofaanvormende enzymen met drie resten (3-CyFE's). De nieuwe binding wordt weergegeven in blauw en gemarkeerd in cyaan. De familie van natuurlijke producten die worden geproduceerd door 3-CyFE's wordt triceptiden genoemd.
NUS-onderzoekers hebben post-translationele modificerende enzymen in bacteriën geïdentificeerd die een nieuwe familie van cyclische peptiden voor nieuwe therapieën kunnen creëren.
Cyclische peptiden zijn een bekende klasse van moleculen die een reeks biologische activiteiten bezitten, waaronder antibacteriële, immunosuppressieve en kankerbestrijdende eigenschappen. De uitdaging om nieuwe soorten cyclische peptiden te creëren, ligt in de ontdekking van nieuwe katalytische reacties door chemische synthese of door het gebruik van enzymen. Een strategie om dit te bereiken omvat de vorming van koolstof-koolstof (C-C) bindingen. Echter, C-C bindingsvormende reacties bij niet-geactiveerde koolstof-waterstof (C-H) bindingen zijn moeilijk omdat deze posities inert zijn, en de selectiviteit is niet gemakkelijk te controleren. Door deze barrières te overwinnen, kan op een efficiënte en voorspelbare manier een nieuwe reeks cyclische peptiden worden gecreëerd.
Het onderzoeksteam onder leiding van prof. Brandon Morinaka van de afdeling Farmacie, NUS heeft reacties gevonden die worden gekatalyseerd door een reeks post-translationele modificerende enzymen van verschillende bacteriën die mogelijk kunnen worden gebruikt om belangrijke medicijnmoleculen te ontwikkelen. Deze enzymen kunnen de vorming van een C(aryl)-C( sp 3 ) binding tussen de zijketens van twee aminozuren. Deze moleculaire rangschikking is het bepalende kenmerk voor een klasse van natuurlijke producten die triceptiden worden genoemd (drie residuen in cyclofaanpeptiden) (zie afbeelding). De ringsluitingsreactie resulteert in de vorming van gespannen peptidecyclofanen. Hoewel deze enzymen worden gecodeerd in enkele honderden bacteriële genomen, hun functie en hun eindproducten zijn grotendeels onbekend gebleven.
Deze enzymen bieden een nieuwe strategie voor de modificatie van peptiden en kunnen worden toegepast om therapeutische peptiden te genereren die een unieke binding aan moleculaire doelen vertonen. De cyclisatie van peptiden is een algemene strategie die in de natuur en de synthetische chemie wordt gebruikt om afbraak door spijsverteringsenzymen te voorkomen. Het voorkomen van afbraak is een essentiële eigenschap die geneesmiddelen nodig hebben om hun doel te bereiken en vormt een hindernis voor het gebruik van peptiden als geneesmiddelen.
Deze enzymen zijn in staat om de ringen in verschillende patronen met verschillende aminozuren te installeren. Dit betekent dat de breedte van producten potentieel groot is en kan worden toegepast op verschillende doelen bij het ontdekken van geneesmiddelen. Diverse bacteriën uit een reeks microbiomen bleken te coderen voor de cyclofaanvormende enzymen. De diversiteit van producten wijst erop dat peptide-cyclofanen vaker voorkomen dan voorheen bekend was en mogelijk een algemeen gebruik of een algemene functie zou kunnen verlenen in deze klasse van natuurlijke producten.
Het team is van plan om extra natuurlijke triceptideproducten te produceren en het enzymmechanisme te begrijpen. Hun langetermijndoelen zijn het genereren van een breed scala aan peptide-cyclofaanproducten die kunnen worden gebruikt als startpunt voor het aanpakken van ziekten van belang.
Prof Morinaka zei:"Post-translationele cyclofaanvormende enzymen bieden een nieuwe methode voor het creëren van diverse cyclische peptiden die nieuwe kansen bieden in peptide-engineering en medicijnontdekking."
 De vorm in water:eerste nanoschaalmetingen van het vouwen van biomoleculen in vloeistof
De vorm in water:eerste nanoschaalmetingen van het vouwen van biomoleculen in vloeistof Superflexibele aerogels zijn zeer efficiënte absorptiemiddelen, thermische isolatoren, en druksensoren
Superflexibele aerogels zijn zeer efficiënte absorptiemiddelen, thermische isolatoren, en druksensoren Samenwerking zorgt voor doorbraak in duurzame elektronicaproductie
Samenwerking zorgt voor doorbraak in duurzame elektronicaproductie Nieuw elektrodemateriaal ontwikkeld om de laadcapaciteit van lithiumbatterijen te vergroten
Nieuw elektrodemateriaal ontwikkeld om de laadcapaciteit van lithiumbatterijen te vergroten Wat is de vergelijking tussen atomen en moleculen?
Wat is de vergelijking tussen atomen en moleculen?
Hoofdlijnen
- Genomische studie onderzoekt de evolutie van zachte killer-bijen in Puerto Rico
- Wat is TA Cloning?
- Delen van een dierencel voor kinderen
- Anti-verouderingsbehandelingen - de wetenschap van het leven langer
- Wat is er nodig voor de glycolyse?
- Pas op voor de huisdieren bij het hanteren van de Halloween-snoepvangst
- Eiwit-overexpressieprotocol
- Tekenen kunnen helpen, kunnen geschiedenisliefhebbers helpen om meer buff te krijgen
- Wat zijn de functies van Triglyceride Phospholipid & Sterol?
- Een nieuwe microscoop onthult het wonder van moleculaire zuurstof

- Onderzoekers stellen een eenstapsstrategie voor om op grafeen gebaseerde composietfaseveranderingsmaterialen te synthetiseren
- Onderzoekers maken 's werelds snelste moleculaire shuttle
- Welke fundamentele wet wordt aangetoond in evenwichtsvergelijkingen?

- Een nieuwe methode kan tomaten veiliger maken om te eten

 De verbranding van kolen in Siberië leidde 250 miljoen jaar geleden tot klimaatverandering
De verbranding van kolen in Siberië leidde 250 miljoen jaar geleden tot klimaatverandering Communicatie verstoren bij infectieuze bacteriën
Communicatie verstoren bij infectieuze bacteriën Wetenschappelijke evaluatie van neushoorndiëten verbetert dierentuin
Wetenschappelijke evaluatie van neushoorndiëten verbetert dierentuin Hyundai pronkt met wandelend autoproject
Hyundai pronkt met wandelend autoproject Een type semi-transparant polymeer dat bij kamertemperatuur kan worden hersteld met een kleine druk
Een type semi-transparant polymeer dat bij kamertemperatuur kan worden hersteld met een kleine druk Berkeley-onderzoekers verlichten witte OLED's
Berkeley-onderzoekers verlichten witte OLED's De nadelen van Recycled Plastics
De nadelen van Recycled Plastics Tarantula's inspireren nieuwe structurele kleuren met de grootste kijkhoek
Tarantula's inspireren nieuwe structurele kleuren met de grootste kijkhoek
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway | Italian |

-
Wetenschap © https://nl.scienceaq.com

