
Wetenschap
High-tech gel helpt bij het afleveren van medicijnen
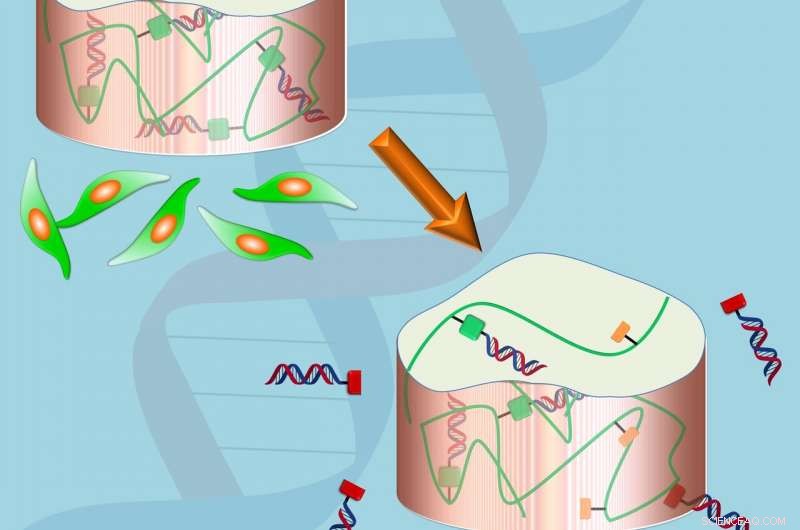
Gel helpt bij het afleveren van medicijnen. Krediet:Eben Alsberg
Geneesmiddelen die de vorming van ongewenste of schadelijke eiwitten helpen voorkomen, worden momenteel ontwikkeld om een aantal ziekten te behandelen, waaronder kanker. De medicijnen zijn gebaseerd op klein interfererend RNA, of siRNA, dat zijn stukjes nucleïnezuur die werken door de productie van eiwitten te verstoren. Maar om deze medicijnen op het juiste doelwit te krijgen, zoals een tumor, blijft een uitdaging omdat siRNA's snel in het lichaam kunnen worden afgebroken, waardoor systemische toediening inefficiënt wordt. Ze kunnen ook wat moeite hebben om cellen binnen te gaan waar ze hun werk doen.
Eben Alsberg, de Richard en Loan Hill hoogleraar bio-engineering en orthopedie aan de Universiteit van Illinois in Chicago, en collega's rapporteren over een op hydrogel gebaseerde drager die siRNA's rechtstreeks kan afleveren waar ze nodig zijn. Ze rapporteren hun bevindingen in wetenschappelijke vooruitgang .
Andere onderzoekers hebben enig succes gehad bij het koppelen van de siRNA-moleculen aan andere materialen om nanodeeltjes te vormen die de afbraak van siRNA helpen voorkomen en de medicijnen helpen cellen binnen te dringen. Maar systemisch afgeleverde medicijnen met nanodeeltjes hebben de neiging om de beoogde cellen laag te bereiken, meerdere doses nodig hebben om het gewenste effect te hebben, wat het risico op negatieve bijwerkingen verhoogt.
Biologisch compatibele hydrogels zijn gebruikt om biologische geneesmiddelen of medicijnen rechtstreeks naar specifieke gebieden in het lichaam te brengen. Een hydrogelplug of -vel met geneesmiddel kan direct op de plaats worden geplaatst waar het medicijn nodig is, bijvoorbeeld in een gewricht of bij een breuk in het bot, of zelfs geïnjecteerd.
Maar een probleem was dat medicijnen die in hydrogels zijn geladen, vaak snel naar de omliggende cellen en weefsels diffunderen. het verstrekken van een eerste uitbarsting van drugs en niet veel meer. De afgifte kan worden vertraagd door de porositeit van de hydrogel te veranderen, de afbraaksnelheid en door te sleutelen aan de affiniteit van het medicijn voor de hydrogel.
Alsberg samen met Matthew Levy, universitair hoofddocent biochemie aan het Albert Einstein College of Medicine, en hun collega's ontwikkelden een unieke hydrogelstrategie die meer controle mogelijk maakt over de afgifte van siRNA's in de loop van de tijd. Door het siRNA chemisch te koppelen aan de hydrogel via een linker die in het lichaam kan worden afgebroken, ze kunnen de afgifte van het medicijn beheersen. Wanneer de hydrogel in een op water gebaseerde omgeving wordt geplaatst, zoals een biologisch organisme, water breekt de linker tussen het siRNA en de hydrogel, het medicijn vrijgeven. In dit soort systeem, afgifte van het geneesmiddel wordt verlengd in vergelijking met wanneer het siRNA alleen fysiek in de hydrogel wordt opgesloten.
"Misschien kunnen we deze technologie in de toekomst gebruiken om bijvoorbeeld, de productie te voorkomen van bepaalde eiwitten waarvan bekend is dat ze bepaalde ziekten bevorderen, of om stamcellen te helpen transformeren in cellen die nodig zijn om beschadigd weefsel zoals bot of kraakbeen te herstellen, ', aldus Alsberg.
 De kloof tussen weer en klimaat overbruggen
De kloof tussen weer en klimaat overbruggen Hoe veranderingen veroorzaakt door het coronavirus de klimaatverandering kunnen helpen aanpakken
Hoe veranderingen veroorzaakt door het coronavirus de klimaatverandering kunnen helpen aanpakken Verbetering van overstromingsprojecties, voorspellingen en bescherming in Venetië
Verbetering van overstromingsprojecties, voorspellingen en bescherming in Venetië Hoe maak je een Dolphin Habitat in een schoenendoos voor school
Hoe maak je een Dolphin Habitat in een schoenendoos voor school  Wereldwijd kankerrisico door verbranding van organisch materiaal komt van niet-gereguleerde chemicaliën
Wereldwijd kankerrisico door verbranding van organisch materiaal komt van niet-gereguleerde chemicaliën
Hoofdlijnen
- Zooplankton Vs. fytoplankton
- Met uitsterven bedreigde mus in Centraal-Florida die in het wild waarschijnlijk niet zal overleven
- Hoe het Human Microbiome-project werkt
- Vijf soorten genverbindingsmechanismen
- Wetenschappers rapporteren chemische basis van de celdelingstimer, een mogelijk doelwit tegen kanker
- Onderzoekers onthullen hoe stamcellen beslissingen nemen
- Soorten forensische tests
- Wetenschappers presenteren een nieuwe methode om elk eiwit in elk soort cel direct en snel te vernietigen
- Nieuwe software kan binnen enkele minuten iemands identiteit verifiëren aan de hand van hun DNA
- Hoe Vmax Lineweaver

- Zullen de futures-superbatterijen van zeewater worden gemaakt?
- Wetenschappers ontdekken dat hydratatie de sleutel is tot het verbeteren van de prestaties van katalysatoren voor industrieel gebruik
- Er komt iets slecht (ruikend) op deze manier - de wetenschap van stoffen en geuren

- Onderzoek onthult het eerste niet-centrosymmetrische fluoroxosilicofosfaat met Si-F-bindingen
 In een recensie van 100 best verkochte prentenboeken, vrouwelijke hoofdrolspelers zijn grotendeels onzichtbaar
In een recensie van 100 best verkochte prentenboeken, vrouwelijke hoofdrolspelers zijn grotendeels onzichtbaar Wetenschappers vinden een effectieve manier om brandstof voor waterstofmotoren te verkrijgen
Wetenschappers vinden een effectieve manier om brandstof voor waterstofmotoren te verkrijgen Wetenschapper leidt internationaal team om 60 jaar oud mysterie van magnetische zonnegolven te ontrafelen
Wetenschapper leidt internationaal team om 60 jaar oud mysterie van magnetische zonnegolven te ontrafelen Ouders, seksuele voorlichting begint thuis
Ouders, seksuele voorlichting begint thuis Golffysica als een analoog terugkerend neuraal netwerk
Golffysica als een analoog terugkerend neuraal netwerk Wat is het smeltpunt van tin?
Wat is het smeltpunt van tin?  Bestaat er zoiets als een objectief slecht nummer?
Bestaat er zoiets als een objectief slecht nummer? Onderzoekers vinden waarde in ongebruikelijk type plantmateriaal
Onderzoekers vinden waarde in ongebruikelijk type plantmateriaal
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- Italian | Portuguese | German | Dutch | Danish | French | Spanish | Swedish | Norway |

-
Wetenschap © https://nl.scienceaq.com

