
Wetenschap
Slimmere medicijnafgifte dankzij controle over inkapseling
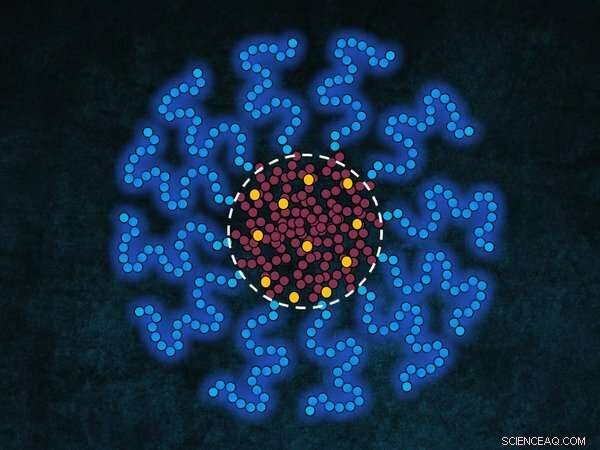
Schematische afbeelding van een micel - bestaande uit een hydrofiele schaal (blauwe staarten) en een hydrofobe kern (rode staarten) - die medicijnmoleculen inkapselen (geel). De geneesmiddelmoleculen verzamelen zich meestal op het grensvlak tussen kern en schil (gestippelde witte lijn) van de micel als de concentratie van het geneesmiddel lager is dan de oplosbaarheid in water van het oplosmiddel, terwijl als de concentratie boven de oplosbaarheid ligt, ze zich in de kern verzamelen. Krediet:Alessandro Ianori
Onderzoekers van de Technische Universiteit Eindhoven en de Universiteit Utrecht hebben de parameters ontdekt die de inkapseling van medicijnen bepalen. Dit geeft meer controle over de langzame en gestage afgifte van geneesmiddelen bij patiënten. Bovendien, het ontwerpen van inkapseling voor nieuwe medicijnen zal nu veel minder experimenten vereisen, wat zorgt voor een snellere en goedkopere ontwikkeling van medicijnen. De onderzoekers geloven dat dit werk een aanzienlijke impact zal hebben op het biomedische veld en het ontwerpen van toekomstige medicijnen.
Veel medicijnen zijn hydrofoob - ze lossen niet goed op in water - wat de toediening van medicijnen bij patiënten problematisch maakt. Een mogelijke oplossing is om de medicijnen in te kapselen in kleine verpakkingen die van binnen hydrofoob (waterafstotend) en van buiten hydrofiel (wateroplosbaar) zijn. De medicijnen hopen zich op in de binnenkant van deze verpakkingen en het transport van het medicijn door het lichaam van de patiënt wordt veel gemakkelijker. De verpakkingen bestaan vaak uit bijbehorende oppervlakteactieve stoffen, die farmaceutisch zijn goedgekeurd. Wanneer opgelost in water, een fysiologische oplossing, of bloed, deze moleculen oriënteren hun hydrofobe deel naar de binnenkern (met affiniteit voor de onoplosbare geneesmiddelen) en hun hydrofiele kant naar buiten, het vormen van een bolvormig 'pakket', een micel genoemd.
De verblijfplaats in een micel
Drugs op deze manier door het lichaam vervoeren is al decennia mogelijk, maar nu pas begrijpen onderzoekers welke factoren precies bepalen waar de medicijnen in de micel zich verzamelen. Deze ruimtelijke verdeling kan de afgiftesnelheid van de medicijnen in een patiënt dramatisch beïnvloeden. Sommige geneesmiddelen concentreren zich in het midden van de hydrofobe kern van de micel en komen langzaam vrij, hetgeen wenselijk is voor de medicijnopname van een patiënt. Andere geneesmiddelen verzamelen zich bij de kern-schil-interface van de micel en komen meestal snel vrij. Daarom, het regelen van de locatie van de medicijnen in de micel-inkapseling regelt de afgiftesnelheid van de medicijnen.
Een kleurstof gebruiken om drugs te volgen
Om te onderzoeken waar onoplosbare medicijnen zich verzamelen, de onderzoekers gebruikten Nile Red, een kleurstofmolecuul dat lijkt op de grootte en oplosbaarheid van typische medicijnen. De kleurstof heeft een heel slimme eigenschap:het absorbeert niet alleen een bepaalde kleur licht, maar ook die kleur is afhankelijk van de omgeving. Als de kleurstof is opgelost in zuiver water, het absorbeert licht van een andere kleur dan wanneer er ook wat alcohol in het water is opgelost. Het veranderen van de water/alcohol-verhouding is een slimme manier om een goed oplosmiddel of een slecht oplosmiddel voor de kleurstof te simuleren. Dit is analoog aan het werken met een in water oplosbaar medicijn of een onoplosbaar medicijn. Door de lichtabsorptie te meten, de onderzoekers konden bepalen hoeveel kleurstof zich in de kern van de micel verzamelde en hoeveel bij de kern-schaal-interface.
Experimenten gecombineerd met computersimulaties
Om hun bevindingen te bevestigen, de onderzoekers deden computersimulaties om de locaties van de opgeloste medicijnen en de vorm van de blokcopolymeermicel te bepalen. De berekeningen onthullen de rangschikking van de componenten binnen en buiten de micel, waardoor de voorkeursregio's van het medicijn kunnen worden beoordeeld.
Uit de experimenten en berekeningen werd geconcludeerd dat het voorkeursgebied van het geneesmiddel binnen de blokcopolymeermicellen voornamelijk wordt bepaald door de concentratie en de oplosbaarheid van de geneesmiddelmoleculen in het omringende medium (water/fysiologisch medium/bloed). Als de concentratie van het medicijn lager is dan de oplosbaarheid in water van het oplosmiddel, verzamelen de medicijnmoleculen zich op het kern-schil-interface van de micel, terwijl als de concentratie boven de oplosbaarheid ligt, ze zich in de kern verzamelen.
Minder proefondervindelijk experimenteren
Het huidige onderzoek naar inkapseling van geneesmiddelen wordt gedomineerd door trial-and-error-experimenten. De resultaten die in dit onderzoek worden gerapporteerd, maken de ontwikkeling van smartdrugs eenvoudiger en goedkoper. Dit zal de bijwerkingen van therapie helpen verminderen en het creëren van gepersonaliseerde therapeutische behandelingen vergemakkelijken waarbij de afgifte van het medicijn wordt aangepast aan de individuele behoeften van de patiënt.
 Onderzoekers krijgen een glimp op nanoschaal van spleet- en putcorrosie terwijl het gebeurt
Onderzoekers krijgen een glimp op nanoschaal van spleet- en putcorrosie terwijl het gebeurt Nieuwe vondst legers verlaagt onbedoelde ontploffing van voorraden
Nieuwe vondst legers verlaagt onbedoelde ontploffing van voorraden Nieuwe materialen en processen om pathogene micro-organismen uit water te verwijderen
Nieuwe materialen en processen om pathogene micro-organismen uit water te verwijderen Dynamisch 3D-printproces met lichtgestuurde draai
Dynamisch 3D-printproces met lichtgestuurde draai Wetenschappers ontwikkelen supersnel opladen, kaliumbatterijen met hoge capaciteit
Wetenschappers ontwikkelen supersnel opladen, kaliumbatterijen met hoge capaciteit
 NASA-infraroodbeelden geven aan dat Cristobals zware regen kan maken
NASA-infraroodbeelden geven aan dat Cristobals zware regen kan maken Goed nieuws:habitats die bescherming verdienen in Duitsland worden beschermd
Goed nieuws:habitats die bescherming verdienen in Duitsland worden beschermd Hoe maak je een 3D Food Web Model
Hoe maak je een 3D Food Web Model Studie van Europese historische gegevens suggereert dat het aandeel NO2 in de NOx-emissies kleiner is dan gedacht
Studie van Europese historische gegevens suggereert dat het aandeel NO2 in de NOx-emissies kleiner is dan gedacht Een Otter-schoenendoos maken Habitat
Een Otter-schoenendoos maken Habitat
Hoofdlijnen
- Grafische Australische video van Japanse walvisvangst vrijgegeven
- Wetenschappers ontdekken dat schorpioenen zich richten op hun gif
- Dit is waarom Fortnite zo verslavend is
- Telofase: wat gebeurt er in deze fase van mitose en meiose?
- Hoe worden genen aan- en uitgezet?
- Door schadesporen in kaart te brengen, kunnen onderzoekers het water volgen in Photosystem II
- Onderzoekers observeren enzymen die cellulose afbreken om de productie van biobrandstoffen te ondersteunen
- Florida probeert het tij te keren bij de invasie van leguaan
- Het verschil tussen een sporofyt en gametofyt
- Een glowstick die kanker opspoort?
- Ultrasone techniek onthult de identiteit van grafiet

- Metaalzepen kritisch in snelheid van bederf van olieverfschilderijen

- Hit-to-lead-onderzoeken naar een nieuwe reeks kleine molecuulremmers van DHODH

- Organotinvergiftiging kan zwaarlijvigheid veroorzaken, medici zeggen:
 Raciale micro-agressies dragen bij aan ongelijkheden in STEM-onderwijs
Raciale micro-agressies dragen bij aan ongelijkheden in STEM-onderwijs Nieuwe methoden ontwikkelen om nanodeeltjes in voedsel te detecteren
Nieuwe methoden ontwikkelen om nanodeeltjes in voedsel te detecteren Hoe een justitie-weegschaal te maken
Hoe een justitie-weegschaal te maken Australië verandert van verdediging in aanval in natuurbrandgevecht
Australië verandert van verdediging in aanval in natuurbrandgevecht Grote investeerder biedt ongeveer $ 6,5 miljard voor athenahealth
Grote investeerder biedt ongeveer $ 6,5 miljard voor athenahealth Toekomstige gevolgen van El Nino, La Nina zal waarschijnlijk intensiveren
Toekomstige gevolgen van El Nino, La Nina zal waarschijnlijk intensiveren De effecten van zoutconcentratie op bacteriegroei
De effecten van zoutconcentratie op bacteriegroei Succesvolle test brengt militair een stap dichter bij elektromagnetische railkanonnen
Succesvolle test brengt militair een stap dichter bij elektromagnetische railkanonnen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

