
Wetenschap
Van goot naar darm:hoe antimicrobieel resistente microben van de omgeving naar de mens reizen
Er zijn talloze manieren waarop antibioticaresistente microben het menselijk lichaam kunnen binnendringen. Credit:Biorender, auteur verstrekt
Van keelpijn tot koorts en levensbedreigende infecties, de meeste mensen hebben regelmatig antibiotica gebruikt. Recente rapporten tonen aan dat de wereldwijde COVID-19-pandemie het gebruik van antibiotica heeft doen toenemen.
Sommige microben kunnen van nature resistent zijn tegen bepaalde antimicrobiële stoffen. In andere gevallen bevordert oneigenlijk gebruik van antimicrobiële stoffen de wijziging van microbiële genen (genen zijn eenheden van DNA), waardoor de microben resistent worden tegen antimicrobiële stoffen. De man achter de ontdekking van antibiotica, Alexander Fleming, gaf een anticiperende waarschuwing over dit onderwerp in zijn Nobellezing van 1945:
"Meneer X heeft keelpijn. Hij koopt wat penicilline en geeft zichzelf niet genoeg om de streptokokken (bacteriën waarvan bekend is dat ze keelpijn en amandelen veroorzaken) te doden, maar genoeg om ze te leren penicilline te weerstaan. Vervolgens infecteert hij zijn vrouw. Mevrouw X. X krijgt longontsteking en wordt behandeld met penicilline. Omdat de streptokokken nu resistent zijn tegen penicilline, mislukt de behandeling. Mevrouw X sterft. Wie is er primair verantwoordelijk voor de dood van mevrouw X?"
Deze situatie wordt antimicrobiële resistentie genoemd en de genen die resistentie verlenen, worden antimicrobiële resistentiegenen (ARG's) genoemd.
Antimicrobiële resistentiegenen
Wereldwijd nemen gezondheidsproblemen als gevolg van antimicrobiële resistentie toe. Een van de belangrijkste redenen is de mobiliteit van ARG's. De resistentiegenen kunnen worden overgedragen van de ene generatie microben naar de volgende door reproductie, en kunnen ook worden overgedragen door horizontale genoverdracht (niet-seksuele overdracht van genetisch materiaal tussen verschillende microben).
Dit houdt in dat antimicrobiële resistentiegenen, ongeacht hun oorsprong, kunnen worden overgedragen van omgevingsbronnen naar de menselijke darm en vice versa.
Als milieu-ingenieurs richt ons onderzoek aan de McGill University zich op het ontwikkelen van hulpmiddelen voor het bewaken van de beweging van antimicrobiële resistentiegenen in afvalwater en het begrijpen van de impact van ARG-overdracht op menselijke darmmicroben. Afgezien van de overdracht van mens op mens van resistente microben zoals beschreven door Fleming, zijn er verschillende andere manieren waarop deze microben het menselijk lichaam kunnen binnendringen.
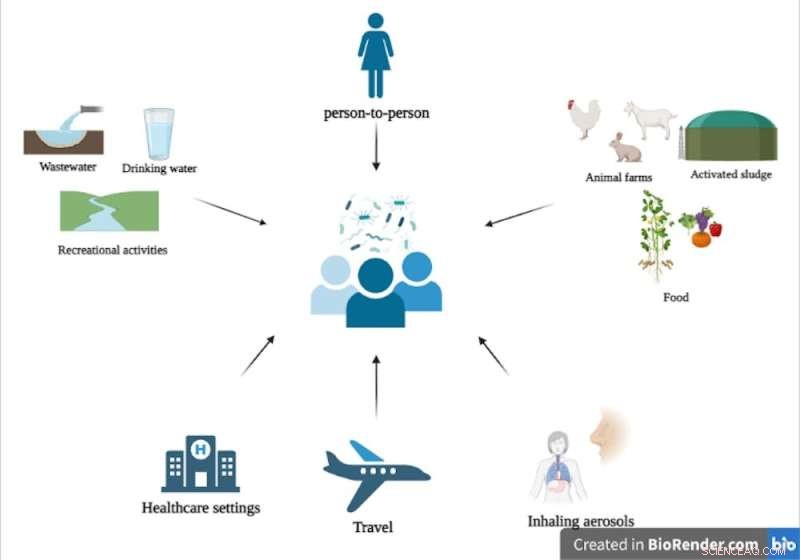
Verschillende routes van overdracht van genen voor antimicrobiële resistentie van de omgeving naar de menselijke darm. Krediet:BioRender.com, auteur verstrekt
Afvalwater
Afvalwater is een gootsteen voor menselijke activiteiten en bevat resistentiegenen van menselijke uitwerpselen, boerderijen, huishoudens en ziekenhuizen. Gezuiverd afvalwater komt vaak terecht in oppervlaktewateren zoals rivieren, die worden gebruikt voor recreatieve activiteiten zoals sport, vissen en zwemmen. Uit een dwarsdoorsnede-onderzoek bleek dat de darm van surfers drie tot vier keer meer kans heeft om te worden gekoloniseerd door multiresistente microben in vergelijking met de darm van niet-surfers.
Daarnaast wordt drinkwater gewonnen uit gezuiverd oppervlakte- of grondwater. Onderzoek heeft aangetoond dat drinkwaterbiofilms (aggregatie van microben die op oppervlakken leven) antimicrobiële resistentiegenen kunnen overbrengen naar de muizendarm, wat aangeeft dat ze ook kunnen worden overgedragen naar de menselijke darm.
Eten
Om de productiviteit van dieren te verhogen, worden op boerderijen vaak antimicrobiële middelen toegepast, wat kan leiden tot de selectie en ontwikkeling van resistentiegenen. De toepassing van dierlijke mest en slib (bijproduct van afvalwaterzuivering) in de landbouw kan de overdracht van antimicrobiële resistentiegenen naar voedselgewassen bemiddelen. Er zijn verschillende ARG's gevonden die vanuit de bodem naar eetbare delen van planten, zoals tomaten, sla en tuinbonen, reizen.
Lucht
Inhaleerbare genen voor antimicrobiële resistentie vormen een steeds groter wordende stille bedreiging voor de gezondheid. Recente rapporten van ziekenhuismonsters hebben aangetoond dat de dagelijkse menselijke blootstelling aan resistente bacteriën in spuitbussen 10 keer hoger is dan die in drinkwater.
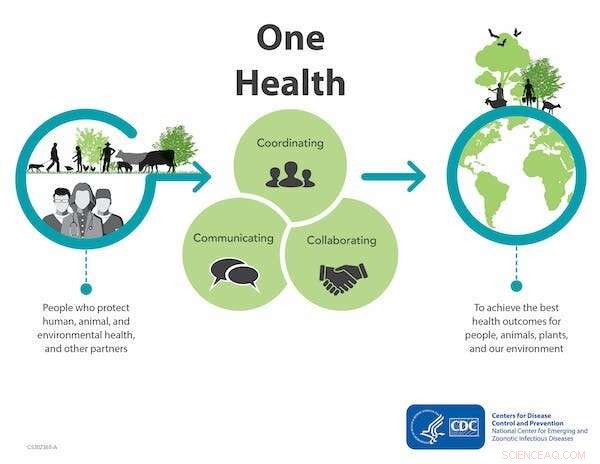
One Health-benadering om antimicrobiële resistentie te bestrijden. Krediet:centra voor ziektebestrijding en -preventie
Gezondheidszorg
Gezondheidszorginstellingen zijn een van de meest prominente locaties voor het oplopen van multiresistente infecties vanwege de aanwezigheid van opportunistische pathogenen die immunologisch gecompromitteerde patiënten infecteren. De aanwezigheid van antimicrobiële stoffen helpt verder bij de ontwikkeling en selectie van resistente microben, die vervolgens van de ene patiënt op de andere kunnen worden overgedragen door interpersoonlijk contact of via gemeenschappelijke oppervlakken zoals deurgrepen, bedrails of kluisjes.
Reizen
Internationale reizigers die naar ontwikkelingslanden reisden, bleken multiresistente bacteriën te krijgen. Ze kunnen deze microben hebben verkregen via besmet voedsel en water, vanwege slechte hygiënepraktijken of vanwege een verschillend antimicrobieel gebruiksbeleid in verschillende landen.
Een One Health-benadering
Het is duidelijk dat antimicrobieel resistente microben ons omringen, en het is normaal dat we ons zorgen maken. Maar wat nog belangrijker is om te herkennen, zijn de kleine stappen die we allemaal nog kunnen nemen. Dit houdt onder meer in dat patiënten worden behandeld met het juiste antibioticum in de juiste dosis.
On a global level, understanding the transmission routes for resistant microbes is a part of a One Health approach. The holistic concept of One Health acknowledges that the health of humans is interconnected to the health of animals and our surrounding environment. This enables bringing together resources and policies to monitor and tackle antimicrobial resistance.
Indeed, resistant microbes are running a marathon with antimicrobials, and we need to take measures to slow down their pace. In the long run, this would ensure that the antimicrobials would continue to support human survival. + Verder verkennen
Modeling antimicrobial use and resistance in Canadian turkey flocks
Dit artikel is opnieuw gepubliceerd vanuit The Conversation onder een Creative Commons-licentie. Lees het originele artikel. 
 De aardbeving van 4 juli zal de Big One niet vertragen. En het zou de aardbevingsspanning kunnen hebben verergerd
De aardbeving van 4 juli zal de Big One niet vertragen. En het zou de aardbevingsspanning kunnen hebben verergerd China zegt dat het zijn CO2-reductiedoel vroegtijdig heeft bereikt
China zegt dat het zijn CO2-reductiedoel vroegtijdig heeft bereikt Onderzoekers identificeren 15 twisters die prairies raken op Canada Day
Onderzoekers identificeren 15 twisters die prairies raken op Canada Day NASA-ogen intensiveren tropische cycloon Frances
NASA-ogen intensiveren tropische cycloon Frances Lichtere bestrating maakt steden echt cool als het goed wordt gedaan
Lichtere bestrating maakt steden echt cool als het goed wordt gedaan
Hoofdlijnen
- Verdrietig en verontrustend:enorme aantallen vogeldoden in Australische hittegolven onthullen dat er een groot verlies op komst is
- Hoe ziet een menselijke cel eruit?
- Scholieren reageren vooral op één of twee buren tegelijk
- Dode vissen en depressies aan de oevers van de Oder
- Honden kunnen dementie krijgen, maar veel wandelen kan het risico verlagen
- Diepe wortels in planten aangedreven door bodemhydrologie
- Een bouwsteen voor leverfitness op oudere leeftijd
- Van druppel tot ontdekking
- Waarom neemt het DNA-gehalte toe tijdens interfase?
- Computersimulaties onthullen wortels van resistentie tegen geneesmiddelen
- Koraalgenoom onthult cysteïneverrassing

- Naar huis vliegen? IJstijd heeft de vogeltrek mogelijk afgeremd

- Vogels leren van elkaars walging, waardoor insecten felle kleuren kunnen ontwikkelen

- 2 kiwivogels zijn zeldzaam lichtpuntje in grimmig uitstervingsrapport

 Wat eet muggenlarven?
Wat eet muggenlarven?  Mongoolse microfossielen wijzen op de opkomst van dieren op aarde
Mongoolse microfossielen wijzen op de opkomst van dieren op aarde Supernovarest N132D in detail onderzocht
Supernovarest N132D in detail onderzocht Om de toekomst van orkanen te begrijpen, kijk naar het verleden
Om de toekomst van orkanen te begrijpen, kijk naar het verleden Wat is de basis voor uitzonderingen op het Aufbau-principe?
Wat is de basis voor uitzonderingen op het Aufbau-principe?  Hoe bewegen oceaanstromingen?
Hoe bewegen oceaanstromingen?  DNA-nanorobots richten zich op HER2-positieve borstkankercellen
DNA-nanorobots richten zich op HER2-positieve borstkankercellen Rusland worstelt met het opruimen van gemorste brandstof in de Arctische rivier
Rusland worstelt met het opruimen van gemorste brandstof in de Arctische rivier
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

