
Wetenschap
Het vastleggen van extracellulaire blaasjes:een nieuwe technologie voor het isoleren van ziektemarkers
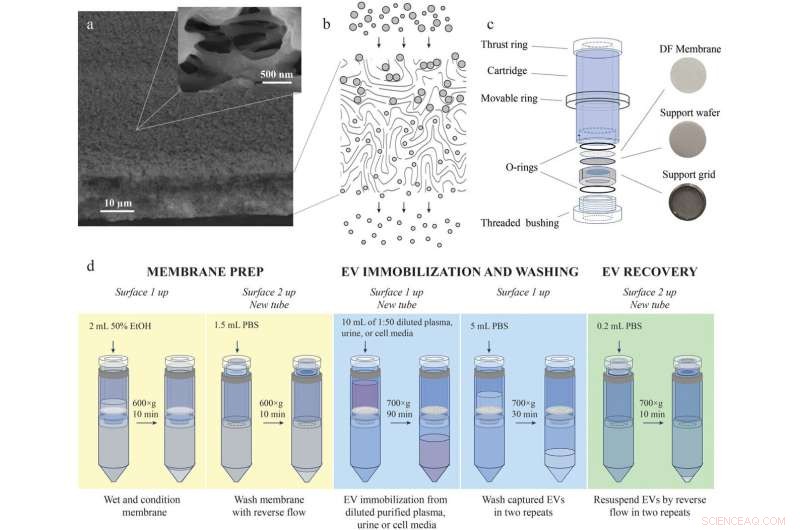
Dieptefiltratiemedium, cartridge en het protocol voor DF-isolatie van EV's uit bloedplasma, urine en celkweekmedia. (a) SEM-beeld van het dieptefiltratiemembraan met de rand en het ingangsoppervlak (oppervlak 1). Hogere vergroting (inzet) van inlaatporiën in Surface 1 toont openingen die veel groter zijn dan de grootte van EV's. Dientengevolge sleept de stroom blaasjes in de poriën totdat ze geïmmobiliseerd raken in de diepte van het filter. (b) Illustratie van het dieptefiltratieproces met twee populaties deeltjes van verschillende groottes. Grotere deeltjes worden vastgehouden in het volume van het filtratiemedium, terwijl kleinere deeltjes worden geëlueerd. (c) DF-patroon. Foto's van het membraan en zijn drager (poreuze wafel en roestvrijstalen rooster waarop het rust) worden rechts getoond. (d) Samenvatting van de werkstroom voor dieptefiltratie om EV's te isoleren van bloedplasma, urine en celkweekmedia. Krediet:Journal of Extracellulaire Vesicles (2022). DOI:10.1002/jev2.12256
Biofysici van Skoltech, MIPT en hun collega's van het bedrijf Prostagnost hebben een nieuwe technologie ontwikkeld voor het isoleren van extracellulaire blaasjes (EV) uit biologische vloeistoffen. Het bestuderen van blaasjes is essentieel voor de diagnose en behandeling van verschillende ziekten, waaronder kanker. De nieuwe techniek overtreft niet alleen methoden die tot nu toe bekend zijn in zuiverheid en opbrengst van EV's, maar is ook eenvoudig, snel, goedkoop en kan draaien op standaard laboratoriumhardware. Het onderzoek is gepubliceerd in het Journal of Extracellular Vesicles .
Onze lichaamscellen "communiceren" met elkaar door signaalmoleculen af te geven aan de bloedstroom. Om ervoor te zorgen dat de moleculen het doelwit veilig bereiken, zijn ze ingekapseld in kleine blaasjes van nanoformaat, EV's, die als een afgiftesysteem werken. EV's van gezonde en zieke cellen hebben een verschillende inhoud, wat de basis vormt voor de diagnose. Blaasjes die worden uitgescheiden door ongezonde cellen bevatten een hele reeks moleculen die dienen als een biomarker voor een ziekte. Het bestuderen van de biomarkers helpt zowel om een ziekte te diagnosticeren als om de behandeling te volgen door veranderingen te analyseren in het aantal EV's dat de geselecteerde markers bevat.
De vraag rijst echter hoe deze minuscule dragers te isoleren. Uit de grote hoeveelheid moleculen in biologische vloeistoffen moeten alleen EV's worden geselecteerd om de eiwitmoleculen die ze bevatten te identificeren, wat biomarkers kunnen zijn voor een ziekte of een teken van een goede gezondheid. Afhankelijk van welke nucleïnezuren, zoals mRNA of DNA, of eiwitten in of op het oppervlak van een EV worden aangetroffen, wordt een conclusie getrokken over de vooruitzichten van de patiënt. Daarom is het belangrijk dat deze onderzoeken snel, efficiënt en tegen lage kosten worden uitgevoerd.
Vasiliy Chernyshev, hoofdauteur en onderzoekswetenschapper bij het MIPT Laboratory for the Development of Innovative Drugs and Agricultural Biotechnology en het Skoltech BioPhotonics Lab, zegt dat "momenteel verschillende algemeen erkende methoden bestaan voor het isoleren van blaasjes, maar deze zijn ofwel te omslachtig of vereisen gespecialiseerde apparatuur, zoals een ultracentrifuge. Niet elke kliniek kan dit betalen en bovendien heeft deze methode een vrij lage isolatie-efficiëntie."
Het team heeft een filtratieapparaat ontwikkeld, een speciale membraansamenstelling en -ontwerp en een stapsgewijze isolatieprocedure. De oplossing maakt snelle en efficiënte EV-isolatie mogelijk en zorgt tegelijkertijd voor een hoge zuiverheid, wat erg belangrijk is voor zowel diagnostiek als EV-onderzoek. Het apparaat is volledig gemaakt van Russische componenten tegen minimale kosten.
Vasiliy Chernyshev voegt eraan toe dat "in het EV-isolatieapparaat dat we samen met het bedrijf Prostagnost hebben ontwikkeld, de scheiding diep in het membraan plaatsvindt met een specifiek porieontwerp. In tegenstelling tot conventionele filtratie, vangen we het product op in het filter en winnen we het terug met de omgekeerde stroom."
"Met deze nieuwe techniek kunnen we EV's van verschillende groottes, inclusief exosomen, effectief isoleren van vrijwel elke biologische vloeistof, zoals bloed, plasma en urine, en EV's met een hoge zuiverheid verkrijgen die vrij zijn van extracellulaire deeltjes of moleculen. Maar het allerbelangrijkste:alles wat we nodig hebben voor de taak is een gewone laboratoriumcentrifuge en specifieke membranen en reageerbuizen die toegankelijk zijn voor elk Russisch klinisch laboratorium."
Sergey Leonov, hoofd van het MIPT-laboratorium voor de ontwikkeling van innovatieve geneesmiddelen en landbouwbiotechnologie, merkt op dat "ons team veel moeite heeft gedaan om de zuiverheid van de exosomen te beschrijven en te bewijzen - membraanblaasjes met een grootte van 40 tot 100 nm. belangrijk voor zowel diagnostiek als proteomics."
"Er is een grote behoefte aan zulke eenvoudige, snelle en effectieve methoden voor wetenschappelijk en medisch EV-onderzoek. We hebben een lokaal ontwikkelde unieke technologie voorgesteld die kan uitgroeien tot een bruikbare routine voor conventionele oncologische praktijken. Dit onderzoek is een perfect voorbeeld van MIPT's inter -institutionele, industriële en internationale samenwerkingen die helpen om met succes om te gaan met importvervangingstaken en om innovatieve Russische oplossingen op de markt te brengen die hun internationale analogen ruimschoots overtreffen." + Verder verkennen
Nanomembraansysteem kan helpen bij het diagnosticeren van ziekten door biomarkers in tranen te isoleren
 Nieuw-Zeelands White Island zal waarschijnlijk opnieuw uitbarsten, maar een nieuw waarschuwingssysteem kan urenlang waarschuwen en levens redden
Nieuw-Zeelands White Island zal waarschijnlijk opnieuw uitbarsten, maar een nieuw waarschuwingssysteem kan urenlang waarschuwen en levens redden Verkenning van de oceaan onthult een van Cuba's verborgen natuurlijke schatten
Verkenning van de oceaan onthult een van Cuba's verborgen natuurlijke schatten Welke soorten vlooien leven in Florida?
Welke soorten vlooien leven in Florida?  Mānoa:Herstel van hybride bos komt ten goede aan gemeenschappen en verhoogt de veerkracht
Mānoa:Herstel van hybride bos komt ten goede aan gemeenschappen en verhoogt de veerkracht Studie identificeert kantelpunt voor herstel van oester
Studie identificeert kantelpunt voor herstel van oester
Hoofdlijnen
- Hoe natuurlijke selectie werkt
- Mitosis vs Meiosis: Wat zijn de overeenkomsten en verschillen?
- Intelligente microscopen voor het detecteren van zeldzame biologische gebeurtenissen
- The Differences Between Kinetochore & Nonkinetochore
- Helder en fotostabiel groen fluorescerend eiwit afgeleid van Japanse kwallen
- Wat zijn energiegerelateerde organellen?
- Wat zit er in je tarwe? Wetenschappers voegen het genoom van de meest voorkomende broodtarwe samen
- Hoeveel Valence-elektronen heeft natrium?
- Klimaatverandering bedreigt landbouwhuisdieren:Italiaanse onderzoekers gebruiken genomica om ze te redden
- Termieten spelen mogelijk een grotere rol in toekomstige ecosystemen
- Vleugelafdrukken kunnen individuele vleermuizen net zo effectief identificeren als vingerafdrukken mensen identificeren
- Nanoplastics kunnen zich in de voedselketen verplaatsen van planten tot insecten en van insecten tot vissen

- Insecten plagen met bitterzoete smaak om gewassen te beschermen

- Geliefde hondenrassen zullen net zo vaak bijten als verboden hondenrassen. Hier leest u hoe u ze kunt stoppen

 NASA's GPM analyseert de regenval van de Atlantische tropische storm Ernestos
NASA's GPM analyseert de regenval van de Atlantische tropische storm Ernestos Silicadeeltjes kunnen leiden tot nieuwe behandelingen voor obesitas en diabetes
Silicadeeltjes kunnen leiden tot nieuwe behandelingen voor obesitas en diabetes Nieuw materiaal doodt E. coli-bacteriën in 30 seconden
Nieuw materiaal doodt E. coli-bacteriën in 30 seconden Wat is het verschil tussen eindige wiskunde en pre-calculus?
Wat is het verschil tussen eindige wiskunde en pre-calculus?  Vrees dat overstromingswater het Barrier Reef zou kunnen verstikken
Vrees dat overstromingswater het Barrier Reef zou kunnen verstikken Studie onthult unieke fysieke, chemische eigenschappen van cicadevleugels
Studie onthult unieke fysieke, chemische eigenschappen van cicadevleugels Wat zijn de functies van een levercel?
Wat zijn de functies van een levercel?  Mysterieuze kosmische explosie verrast astronomen die het verre röntgenuniversum bestuderen
Mysterieuze kosmische explosie verrast astronomen die het verre röntgenuniversum bestuderen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

