Wetenschap
Wat zijn de verschillende soorten modellen van atomen?
Een atoom is het kleinste deel van de elementen waaruit alles op aarde bestaat. Deeltjes van energie vormen een atoom en alleen kernreacties kunnen een atoom verder splitsen. In de afgelopen decennia is een verscheidenheid aan verschillende modellen gebruikt om te speculeren over hoe een atoom werkt en welke deeltjes het bevat.
TL; DR (te lang; niet gelezen)
er waren een paar primitieve modellen voor atomen, je zult hoogstwaarschijnlijk de Bohr en Electron Cloud-modellen in de klas tegenkomen.
Model van biljartbal
In het begin van de 19e eeuw, John Dalton stelde voor dat atomen waren als kleine, harde biljartballen. Zijn kijk op volledig solide atomen lijkt nu een heel fundamenteel idee, maar in 1803 was het baanbrekend. De experts van de Colorado State University zeggen dat deze theorie een belangrijke bijdrage levert aan de chemie. Hij stelde ook voor dat alle atomen van één element identiek zijn, en dat elk element een ander type atoom had.
Plum Pudding-model
J.J. Thompson's Plum Pudding Model introduceerde het idee van positieve en negatieve ladingen in atomen. Volgens Visionlearning gebruikte hij kathodestraalbuizen en positief geladen platen om het bestaan van negatieve deeltjes met de naam elektronen aan te tonen. Hij veronderstelde dat een atoom leek op een pruimenpudding, of een bol gevuld met positief geladen vloeistof en gestippeld met negatieve elektronen.
Zonnestelselmodel
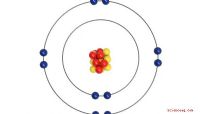
Het planetaire of zonnestelselmodel werd ontwikkeld door Niels Bohr , zeggen de experts van de Universiteit van Tennessee. Ondanks de onnauwkeurigheden en het feit dat het in 1915 is ontwikkeld, is het het meest voorkomende model dat kinderen tegenwoordig krijgen. Het Bohr-model toont een groep neutronen en protonen geclusterd in het midden om de kern te vertegenwoordigen. Overstekbare ringen, bezaaid met elektronen, omringen de kern.
Elektronwolkenmodel
Het elektronenwolkmodel is het meest recente beschikbare atomische model en werd ontwikkeld in de jaren 20 van de vorige eeuw. Op de website van de Colorado State University staat dat Erwin Schrodinger en Werner Heisenburg de specifieke ringen van het Bohr-model hebben veranderd in wolken die de kern omringen. Elke wolk bevat een bepaald aantal elektronen, maar dit model geeft het beste weer hoe moeilijk het is om vast te stellen waar elk elektron zich in relatie tot de kern bevindt.
Hoofdlijnen
- Wat is het Malthusiaanse uitgangspunt?
- Wat doet acetonalcohol met een gramkleuring?
- Is de tweekamerige geest geëvolueerd om het moderne menselijke bewustzijn te creëren?
- Hoe BRCA-genen werken
- Waarom creëren Britse wetenschappers een hybride mens-varken?
- Wat onderscheidt mensen van chimpansees en andere apen?
- Oncogene: wat is het? & Hoe beïnvloedt het de celcyclus?
- Hoe zijn cellen, weefsels en organen aan elkaar gerelateerd?
- Wat gebeurt er met de nucleaire envelop tijdens cytokinese?
Cytokinese is de verdeling van één cel in twee en is de laatste stap na de mitotische celcyclus in vier stadia. Tijdens cytokinese blijft de nucleaire envelop, of kernmembraan, die het gen
 Wetenschapsproject voor de effecten die dranken hebben op de tanden
Wetenschapsproject voor de effecten die dranken hebben op de tanden Homemade Oil Press
Homemade Oil Press Overeenkomsten van Snakes & Lizards
Overeenkomsten van Snakes & Lizards De voor- en nadelen van OTEC
De voor- en nadelen van OTEC  10 zwarte wetenschappers die je moet kennen
10 zwarte wetenschappers die je moet kennen  Verschillende soorten Wild Blue Jay Birds
Verschillende soorten Wild Blue Jay Birds  Negatieve breuken optellen en aftrekken
Negatieve breuken optellen en aftrekken  Soorten scheepsdieselmotoren
Soorten scheepsdieselmotoren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com