
Wetenschap
Nanotechnologie voor genoombewerking in meerdere spieren tegelijk
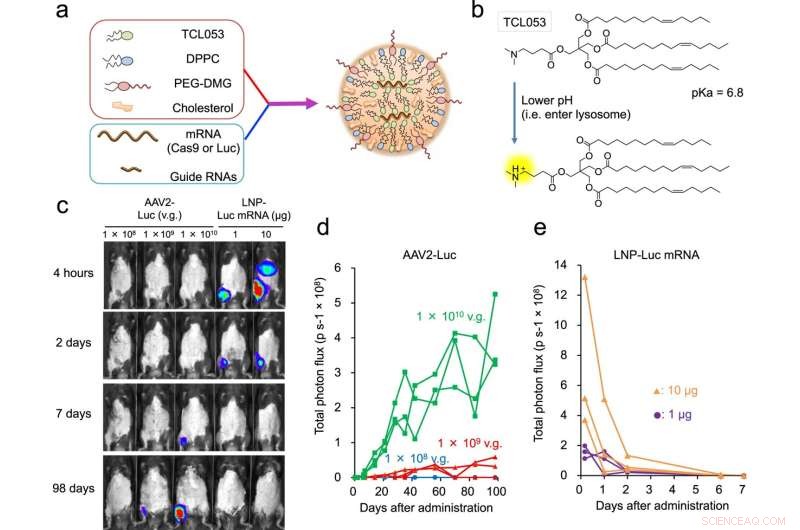
Fig. 1:LNP-gemedieerde Luc-mRNA- of CRISPR-Cas9-mRNA / sgRNA-afgifte in spierweefsel. een schematische illustratie van LNP-CRISPR. Ofwel Luc-mRNA of Cas9-mRNA/sgRNA is ingekapseld in LNP dat bestaat uit TCL053, DPPC (Dipalmitoylfosfatidylcholine), PEG-DMG (Polyethyleenglycol-dimyristoylglycerol) en cholesterol. b Chemische structuur van het nieuw gesynthetiseerde ioniseerbare lipide, TCL053. c Representatieve bioluminescentiebeelden van C57BL/6J-muizen na de intramusculaire injectie van AAV2-Luc (1 × 108, 1 × 109 of 1 × 1010 v.g., vectorgenomen) of LNP-Luc-mRNA (1 of 10 μg mRNA). d, e Kwantificering van het bioluminescentiesignaal in skeletspieren van C57BL/6J-muizen behandeld met AAV2-Luc (d) of LNP-Luc-mRNA (e). Dezelfde muizen (n = 3 muizen per groep) werden in de loop van de tijd herhaaldelijk onderzocht. Totale fluxgegevens (p s−1, fotonen per seconde) worden uitgezet als een enkele lijn per muis. Krediet:DOI:10.1038/s41467-021-26714-w
Veel hardnekkige ziekten zijn het gevolg van een genetische mutatie. Genome editing technologie belooft de mutatie te corrigeren en daarmee nieuwe behandelingen voor patiënten. Het blijft echter een grote uitdaging om de technologie bij de cellen te krijgen die de correctie nodig hebben. Een nieuwe studie onder leiding van CiRA Junior Associate Professor Akitsu Hotta en in samenwerking met Takeda Pharmaceutical Company Limited als onderdeel van het T-CiRA Joint Research Program rapporteert hoe lipidenanodeeltjes een effectief middel zijn voor de levering om Duchenne-spierdystrofie (DMD) bij muizen te behandelen .
De Nobelprijs voor scheikunde van vorig jaar voor de ontdekkers van CRISPR-Cas9 bevestigde de impact van genome editing-technologie. Hoewel CRISPR-Cas9 kan worden toegepast op landbouw en veeteelt voor voedzamer voedsel en robuustere gewassen, gaat de meeste media-aandacht uit naar het medische potentieel ervan. DMD is slechts een van de vele ziekten die onderzoekers voorzien in een behandeling met CRISPR-Cas9.
"Oligonucleotide-medicijnen zijn nu beschikbaar voor DMD, maar hun effecten zijn van voorbijgaande aard, dus de patiënt moet wekelijkse behandelingen ondergaan. Aan de andere kant zijn de CRISPR-Cas9-effecten langdurig", zei Hotta.
DMD resulteert in progressieve spieratrofie door het hele lichaam. Patiënten beginnen normaal gesproken symptomen te vertonen, zoals gemakkelijk vallen en niet kunnen rennen voordat ze naar school gaan, en dragen vaak beademingsapparatuur voordat ze volwassen zijn.
Voor een ziekte als DMD is het noodzakelijk om een breed scala aan skeletspieren aan te pakken, wat betekent dat meerdere injecties belangrijk zijn. Momenteel onderzochte toedieningssystemen maken gebruik van niet-pathogene virussen om CRISPR-Cas9 af te leveren, maar deze virussen induceren immuunreacties en de productie van antilichamen, die meerdere injecties verbieden.
Lipide nanodeeltjes kunnen deze reacties voorkomen. Zoals hun naam al doet vermoeden, zijn lipidenanodeeltjes kleine deeltjes met een diameter van minder dan 0,1 µm en bestaan ze uit lipiden die hun eigenschappen veranderen als reactie op zuurgraad. Door deze functie kunnen ze buiten de cel intact blijven, maar eenmaal binnen scheuren ze om hun inhoud vrij te geven, zoals CRISPR-Cas9, dat vervolgens vrij is om de genmutatie te corrigeren. Lipide-nanodeeltjes worden gebruikt voor COVID-19-vaccins, maar hun nut voor genome editing-therapie wordt nog onderzocht. Als onderdeel van het T-CiRA Joint Research Program heeft Hotta lipide-nanodeeltjes ontwikkeld die genome editing-technologie aan de cel kunnen leveren.
Na experimenten met verschillende formuleringen, rapporteert de studie een nieuw lipidenanodeeltje dat CRISPR-Cas9 inkapselt en zich richt op spiercellen in muizen.
In tegenstelling tot oligonucleotide-geneesmiddelen, waarvan de effecten bij muizen na de behandeling voortdurend afnamen en na een paar maanden verdwenen, toont de studie aan dat de levering van CRISPR-Cas9 met het nieuwe lipide-nanodeeltje een constant effect in de spieren had dat langer dan een jaar aanhield.
Bovendien waren de effecten duidelijk, zelfs bij toediening van de deeltjes met meerdere intramusculaire injecties, terwijl de op virus gebaseerde toediening geen effect had na de tweede injectie. Bovendien hadden intraveneus geperfuseerde lipidenanodeeltjes in de ledematen therapeutisch voordeel voor meerdere spierweefsels.
Als toevoeging aan de veiligheid merkte Hotta op:"CRISPR-Cas9 verdween binnen een paar dagen uit het lichaam. Dat betekent dat het risico van off-target genoombewerking minimaal is, maar de therapeutische effecten houden lang aan." + Verder verkennen
CRISPR/Cas9-genbewerking verhoogt de effectiviteit van ultrasone kankertherapie
 Nieuwe monsterhouder voor eiwitkristallografie
Nieuwe monsterhouder voor eiwitkristallografie Veelzijdige ontwerpoptimalisatie voor superomnifobe oppervlakken
Veelzijdige ontwerpoptimalisatie voor superomnifobe oppervlakken Met koper gedoteerd zinksulfide verandert omkeerbaar van kleur wanneer het wordt verlicht en kan worden gebruikt in slimme adaptieve vensters
Met koper gedoteerd zinksulfide verandert omkeerbaar van kleur wanneer het wordt verlicht en kan worden gebruikt in slimme adaptieve vensters Selectief kooldioxide omzetten in methaan of ethaan
Selectief kooldioxide omzetten in methaan of ethaan Ontdekking binnen het celcyclusproces om inzicht te krijgen in cellulaire ziekten
Ontdekking binnen het celcyclusproces om inzicht te krijgen in cellulaire ziekten
 Hoe maak je een druivengelei en oranje feeder van een hanger om Orioles aan te trekken
Hoe maak je een druivengelei en oranje feeder van een hanger om Orioles aan te trekken
Maak een jelly and orange feeder voor je achtertuin om ervoor te zorgen dat orioles verschijnen in je favoriete buitenruimte. Een kleine kom, stokjes, een haak
 Betere cacaogewassen voor een beter levensonderhoud
Betere cacaogewassen voor een beter levensonderhoud Notre Dame:angst voor lood leidt tot nieuwe opruimregels, apparatuur
Notre Dame:angst voor lood leidt tot nieuwe opruimregels, apparatuur Poll:Energiebesparende gewoonten variëren in populariteit
Poll:Energiebesparende gewoonten variëren in populariteit Geoptimaliseerde positionering van geothermische boorgaten vermindert seismische activiteit
Geoptimaliseerde positionering van geothermische boorgaten vermindert seismische activiteit
Hoofdlijnen
- Energiebesparende LED's stimuleren wereldwijd lichtvervuiling
- Onderzoekers ontdekken dat het nauwkeurig transcriberen van DNA het herstel van DNA opheft
- De reden voor het kleuren van een exemplaar op de microscoop
- Is de remedie tegen kanker een virus?
- Probeer deze 5 dagelijkse gewoonten om je leven dit jaar te verbeteren
- Schapen kunnen menselijke gezichten van foto's herkennen
- VN schotelt vijgcactus voor als antwoord op voedselzekerheid
- Wetenschappers geven 's werelds eerste DNA-kaart van een bedreigde Australische muis vrij, en het zal helpen om deze te redden
- Kennis van larvale vissen slechts een druppel op de gloeiende plaat
- Aanzienlijke vooruitgang bij het stabiliseren van perovskiet-zonnecellen

- Nieuw op grafeen gebaseerd systeem kan ons helpen elektrische signalen in hart- en zenuwcellen te zien

- Chirale gouden nanodeeltjes gebruiken om de immuunrespons te verbeteren

- Nieuwe methode voor het maken van kleine katalysatoren belooft veel voor luchtkwaliteit

- Nieuwe manieren ontwerpen om materiaal te begrijpen

 Wetenschappers van USGS onderzoeken hoe orkanen aan kracht winnen
Wetenschappers van USGS onderzoeken hoe orkanen aan kracht winnen Peroxisomen: defintie, structuur en functie
Peroxisomen: defintie, structuur en functie Wat kan invloed hebben op chemie resultaten?
Wat kan invloed hebben op chemie resultaten?  Vloeibare kristallen die kleurveranderende inkt kunnen vervangen en valsemunterij kunnen voorkomen
Vloeibare kristallen die kleurveranderende inkt kunnen vervangen en valsemunterij kunnen voorkomen Kustwateren zijn onverwachte hotspots voor stikstofbinding
Kustwateren zijn onverwachte hotspots voor stikstofbinding Hoe lockdown-afspeellijsten werden gebruikt om emoties te uiten tijdens de pandemie
Hoe lockdown-afspeellijsten werden gebruikt om emoties te uiten tijdens de pandemie Wat is een waterige oplossing?
Wat is een waterige oplossing?  De vergelijking van een spreidingsplot
De vergelijking van een spreidingsplot
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

