
Wetenschap
Lipidepolymeer maakt veilige levering van RNA-medicijnen aan de longen mogelijk
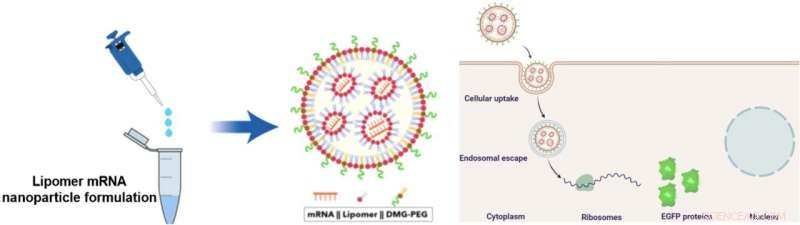
Het lipomeer wordt gecombineerd met mRNA en DMG-PEG om mRNA-dragende nanodeeltjes (NP's) te vormen. Deze NP's kunnen de lever omzeilen om het mRNA rechtstreeks aan de longcellen af te leveren. De wetenschappers gebruikten mRNA dat codeert voor verbeterd groen fluorescerend eiwit (EGFP) voor visualisatie van de eiwitten. Krediet:Mahmoud M. Abd Elwakil, et al., Materialen Horizons . 7 juni 2021
Onderzoekers van de Hokkaido University in Japan hebben een bibliotheek van op lipiden gebaseerde verbindingen gemaakt en getest om een manier te vinden om RNA-medicijnen veilig en effectief aan de longen te leveren. Hun analyses, gepubliceerd in het tijdschrift Materials Horizons, heeft een lipidepolymeer geïdentificeerd dat in de toekomst zou kunnen worden gebruikt voor de behandeling van acuut ademnoodsyndroom, pulmonale hypertensie en longkanker.
De pandemische reactie van COVID-19 heeft ons allemaal bekend gemaakt met RNA-vaccins die genetische code in cellen vervoeren om de productie van viruseiwitten aan te zetten die onze beschermende immuniteit activeren. RNA-medicijnen laten een groot potentieel zien voor de behandeling van een grote verscheidenheid aan andere ziekten door op dezelfde manier de eiwitproductie in cellen te sturen, zonder de noodzaak om DNA in te voegen of te verwijderen. Maar wetenschappers worden geconfronteerd met verschillende uitdagingen bij hun veilige levering aan gerichte cellen. Een succesvolle maar complexe benadering is het dragen van de RNA-codes in nanodeeltjes bedekt met verbindingen, zogenaamde targeting liganden, die kunnen binden aan specifieke cellen. Dit heeft gewerkt voor het richten van levercellen.
De farmaceutische wetenschapper Hideyoshi Harashima van Hokkaido University en polymeerchemicus Toshifumi Satoh leidden een team van onderzoekers bij het ontwikkelen en testen van een bibliotheek van op ε-decalacton gebaseerde verbindingen, lipiden die de lever zouden kunnen omzeilen - die toxines en vreemde stoffen afbreekt - en specifiek RNA-code in de longen afleveren. Harashima ontving onlangs de Høst-Madsen-medaille, de hoogste wetenschappelijke onderscheiding toegekend door The International Pharmaceutical Federation (FIP).

Vrij mRNA richtte zich op geen enkel orgaan (links), terwijl NP's die lipomeer AA03-DL-10 bevatten specifiek mRNA dat codeert voor EGFP naar de longen transporteerden en acht uur na intraveneuze toediening aan muizen groene fluorescerende eiwitten produceerden. Krediet:Mahmoud M. Abd Elwakil, et al., Materialen Horizons , 7 juni 2021
De wetenschappers werkten met twee nauw verwante ringvormige verbindingen:ε-caprolacton en ε-decalacton. Van lipidenanodeeltjes (NP's) die deze lactonen bevatten, werd eerder aangetoond dat ze zich ophopen in de longen. Ze werden onderworpen aan ringopeningsreacties met een van de elf aminoalcoholen. De resulterende producten werden verder geclassificeerd op basis van het molecuulgewicht van elke arm. De producten werden gecombineerd met mRNA en een andere verbinding genaamd DMG-PEG om mRNA-dragende NP's te vormen. NP's gemaakt van ε-caprolacton waren onstabiel, dus ging het team alleen verder met de NP's van ε-decalacton.
Het team testte de afgifte van RNA-dragende ε-decalacton-NP's eerst in laboratoriumkankercellen en vervolgens intraveneus in muizen. Ze gebruikten mRNA dat codeert voor verbeterd groen fluorescentie-eiwit (EGFP) om de bestemming van de NP's te identificeren. uiteindelijk, ze ontdekten dat ε-decalacton in combinatie met een lineaire aminoalcohol genaamd AA03 het beste resultaat opleverde. De onderzoeken toonden aan dat NP's die dit lipomeer bevatten in staat waren grotendeels de lever te omzeilen en het RNA-materiaal specifiek in de longen te transporteren. De NP's werden opgeslokt door het celmembraan en het RNA-gehalte kwam vrij in het cytoplasma van de longcellen.
"We hebben aangetoond dat het uitbreiden van de chemische ruimte van slimme materialen de fabricage van nanodeeltjes voor moeilijk bereikbare doelen mogelijk zou kunnen maken zonder de noodzaak om liganden te targeten, ", zegt Harashima. "Het ontwerpen van combinatorische bibliotheken die diverse ε-decalactonlipomeren bieden, zou een gemakkelijke en schaalbare strategie kunnen zijn voor de ontwikkeling van gentherapieën van de volgende generatie voor organen buiten de lever."
 Explosieve bosbranden in Californië kunnen tot december branden
Explosieve bosbranden in Californië kunnen tot december branden Onderzoek naar orkaanschade zal waarschijnlijk wereldwijd helpen
Onderzoek naar orkaanschade zal waarschijnlijk wereldwijd helpen Rusland onderzoekt vervuiling voor Pacifische kust na ecologische ramp
Rusland onderzoekt vervuiling voor Pacifische kust na ecologische ramp Grote tsunami trof Zuid-China in 1076, zeggen wetenschappers
Grote tsunami trof Zuid-China in 1076, zeggen wetenschappers Mineralen in bergrivieren vertellen het verhaal van aardverschuivingen stroomopwaarts
Mineralen in bergrivieren vertellen het verhaal van aardverschuivingen stroomopwaarts
Hoofdlijnen
- Het verzoenen van taxonveroudering met de Red Queens-hypothese
- De gemiddelde levensduur van skeletspiercellen
- Vogels onthullen het belang van goede buren voor gezondheid en veroudering
- Daar is een studie over:het stenen tijdperk had net zoveel linkse mensen
- Hoe malaria het immuunsysteem bedriegt?
- Hoe biologie te integreren met chemie en natuurkunde
- Aussie uilen vallen door rattengif
- Hoe een microscoop te gebruiken om cellen te zien
- Hoe werkt een DP-cel?
- Labstudie roept vragen op over de impact van nanodeeltjes

- De samenstelling van nanodeeltjes transformeren met behulp van elektrochemie
- Innovatieve nanotransistor voor eenvoudige meting van elektrolytconcentratie in bloed
- Met koolstof nanobuisjes, een weg naar flexibele, goedkope sensoren
- Onderzoek toont aan dat oude kranten kunnen worden gebruikt om koolstofnanobuisjes te laten groeien

 Wat zijn de lichamelijke aanpassingen van een koala?
Wat zijn de lichamelijke aanpassingen van een koala?  Wetenschappers ontwikkelen een nieuw medicijn voor diagnostiek en behandeling van kanker
Wetenschappers ontwikkelen een nieuw medicijn voor diagnostiek en behandeling van kanker Klimaatverandering kan lenen duurder maken voor staten en steden
Klimaatverandering kan lenen duurder maken voor staten en steden Waar gaan kogels naartoe als geweren recht de lucht in worden geschoten?
Waar gaan kogels naartoe als geweren recht de lucht in worden geschoten?  Bereken de gemiddelde diepte
Bereken de gemiddelde diepte  Ideeën voor een Science Fair-project over hoe verschillende vloeistoffen de groei van planten beïnvloeden
Ideeën voor een Science Fair-project over hoe verschillende vloeistoffen de groei van planten beïnvloeden  Nanotechnologie pakt diabetes aan
Nanotechnologie pakt diabetes aan Onderzoek:Akkerplanten nemen microplastics op
Onderzoek:Akkerplanten nemen microplastics op
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

