
Wetenschap
Onderzoek naar celmechanica maakt chemotherapie vriendelijker

Element met een bemonsteringssonde (gemarkeerd) in de atomaire krachtmicroscoop (AFM) in het Spectroscopic Imaging Laboratory van het Institute of Nuclear Physics, Poolse Academie van Wetenschappen. Krediet:IFJ PAN
Kwaadaardige tumorcellen ondergaan gemakkelijker mechanische vervorming dan normale cellen, waardoor ze door het lichaam kunnen migreren. De mechanische eigenschappen van prostaatkankercellen die zijn behandeld met de meest gebruikte geneesmiddelen tegen kanker zijn onderzocht aan het Instituut voor Kernfysica van de Poolse Academie van Wetenschappen in Krakau. Volgens de onderzoekers is huidige medicijnen kunnen effectiever en in lagere doses worden gebruikt.
Bij kanker, een sleutelfactor die bijdraagt aan de vorming van metastase is het vermogen van de neoplastische cellen om mechanische vervorming te ondergaan. Aan het Instituut voor Kernfysica van de Poolse Academie van Wetenschappen (IFJ PAN) in Krakau, er wordt al een kwart eeuw onderzoek gedaan naar de mechanische eigenschappen van cellen. De laatste studie, uitgevoerd in samenwerking met de afdeling Medische Biochemie van het Jagiellonian University Medical College, betrekking had op verschillende geneesmiddelen die momenteel worden gebruikt bij chemotherapie voor prostaatkanker, en specifiek hun impact op de mechanische eigenschappen van kankercellen. De resultaten zijn optimistisch:alles wijst erop dat de doses van sommige medicijnen kunnen worden verlaagd zonder het risico te lopen hun effectiviteit te verminderen.
Chemotherapie is een uiterst brute aanval, niet alleen op de kankercellen van de patiënt, maar op alle cellen in het lichaam. Door het te gebruiken, artsen hopen dat de meer gevoelige tumorcellen zullen sterven voordat de gezonde beginnen te sterven. In deze situatie, het is van cruciaal belang om te weten hoe het optimale medicijn in een bepaald geval te kiezen en hoe de minimale dosis te bepalen, wat enerzijds de effectiviteit van de behandeling garandeert en anderzijds de nadelige effecten van de therapie minimaliseert.
Al in 1999, natuurkundigen van de IFJ PAN toonden aan dat kankercellen mechanisch gemakkelijker vervormen. In praktijk, dit feit betekent dat ze zich efficiënter door de nauwe bloedvaten van de bloedsomloop en/of lymfestelsels kunnen persen.
"De mechanische eigenschappen van een cel worden bepaald door elementen van het cytoskelet, zoals de microtubuli die we onderzoeken, opgebouwd uit tubuline (een eiwit), actinefilamenten en intermediaire filamenten gemaakt van eiwitten zoals keratine of vimentine, " zegt Prof. Malgorzata Lekka van de afdeling Biofysische Microstructuren IFJ PAN en voegt eraan toe:"Biomechanische metingen van cellen worden uitgevoerd met behulp van een atoomkrachtmicroscoop. Afhankelijk van de behoeften, we kunnen de sonde min of meer op de cel drukken, en op deze manier verkrijgen we een mechanische respons afkomstig van structuren die ofwel aan het oppervlak liggen, d.w.z. op het celmembraan, of dieper, zelfs in de celkern. Echter, om informatie te verkrijgen over de effecten van een geneesmiddel, we moeten evalueren welke bijdrage elk type cytoskeletvezel levert aan de mechanische eigenschappen van de cel."

Promovendus Andrzej Kubiak bij de atoomkrachtmicroscoop. Krediet:IFJ PAN
In de momenteel gerapporteerde resultaten, de fysici uit Krakau presenteerden experimenten met de commercieel verkrijgbare DU145 humane prostaatkankercellijn. Deze lijn werd gekozen vanwege de resistentie tegen geneesmiddelen. Langdurige blootstelling aan drugs ondergaan, deze cellen worden na verloop van tijd resistent tegen de medicijnen en gaan niet alleen niet dood, maar beginnen zelfs te delen.
"We hebben ons gericht op de effecten van drie veelgebruikte medicijnen:vinflunine, colchicine en docetaxel. Ze werken allemaal in op de microtubuli, wat wenselijk is omdat deze vezels essentieel zijn voor celdeling. Docetaxel stabiliseert de microtubuli en verhoogt daardoor ook de stijfheid van de tumorcellen en maakt het voor hen moeilijk om door het lichaam te migreren. De andere twee geneesmiddelen destabiliseren de microtubuli, zodat kankercellen kunnen migreren, maar vanwege de verstoorde functies van het cytoskelet, ze kunnen niet delen, " zegt promovendus Andrzej Kubiak, de eerste auteur van het artikel gepubliceerd in de prestigieuze nanoschaal .
De onderzoekers uit Krakau analyseerden de levensvatbaarheid en mechanische eigenschappen van cellen 24, 48 en 72 uur na medicamenteuze behandeling, en het bleek dat de grootste veranderingen drie dagen na blootstelling aan het geneesmiddel werden waargenomen. Hierdoor konden ze twee concentraties medicijnen bepalen:een hogere, die cellen vernietigden, en een lager, waarbij, hoewel cellen overleefden, hun mechanische eigenschappen bleken te zijn veranderd. Voor duidelijke redenen, wat er in het laatste geval met de cellen gebeurde, was van bijzonder belang. De precieze interpretatie van sommige resultaten vereiste verschillende instrumenten, zoals een confocale microscoop en flowcytometrie. Het gebruik ervan was mogelijk dankzij de samenwerking met het Instituut voor Farmacologie van de Poolse Academie van Wetenschappen in Krakau, de afdeling Celbiologie van de Faculteit Biochemie, Biofysica en Biotechnologie van de Jagiellonische Universiteit en de Universiteit van Milaan (Departement Natuurkunde, Universita degli Studi di Milano).
"Het is al enige tijd bekend dat wanneer microtubuli beschadigd zijn, sommige van hun functies worden overgenomen door actinefilamenten. De combinatie van metingen van de mechanische eigenschappen van cellen met beelden van confocale en fluorescentiemicroscopen stelde ons in staat om dit effect waar te nemen. We waren in staat om nauwkeurig de gebieden in de cel te bepalen die door een bepaald medicijn worden beïnvloed en begrijpen hoe de impact ervan in de loop van de tijd verandert, " benadrukt promovendus Kubiak.
Uit het onderzoek van de natuurkundigen van Krakau kunnen praktische conclusies worden getrokken. Bijvoorbeeld, het effect van vinflunine is duidelijk zichtbaar in het nucleaire gebied, maar wordt gecompenseerd door de actinefilamenten. Als resultaat, de cel blijft stijf genoeg om zich te blijven vermenigvuldigen. Anderzijds, 48 uur na toediening van het medicijn, de effecten van docetaxel zijn het meest zichtbaar, voornamelijk aan de celperiferie. Dit feit maakt ons ook attent op de grotere rol van actinefilamenten en betekent dat de therapie moet worden ondersteund met een medicijn dat op deze filamenten inwerkt.
"Tot nu, er is weinig onderzoek gedaan naar de effectiviteit van lage concentraties kankermedicijnen. We laten zien dat de kwestie echt de moeite waard is om je in te verdiepen. Want als we de werkingsmechanismen van individuele medicijnen begrijpen, we kunnen hun huidige effectiviteit behouden - en soms zelfs vergroten - terwijl we tegelijkertijd de bijwerkingen van chemotherapie verminderen. Op deze manier, chemotherapie kan patiëntvriendelijker worden, die niet alleen van invloed moeten zijn op de fysieke gezondheid van de patiënt, maar ook op hun mentale houding die zo noodzakelijk is in de strijd tegen kanker, " concludeert prof. Lekka.
Hoofdlijnen
- Zal er ooit een gelukkige pil zijn?
- Nieuwe online database brengt het genoom in beeld met behulp van moleculaire structuur
- Hoe gigantische tropische fruitvleermuizen te redden:werk samen met lokale jagers die vleermuistanden als geld gebruiken
- Structuur van het cardiovasculaire systeem
- Hoe biologische antropologie werkt
- Invasieve soorten lieveheersbeestjes bedreigt andere lieveheersbeestjes in Engeland
- De rol van GTE in DNA-extractie
- Onderzoekers brengen druggable genomische doelwitten in kaart in evoluerende malariaparasieten
- Hoe Flow Cytometry-resultaten te begrijpen
- Optische emissie van tweedimensionaal arseensulfide bereid in plasma

- Magnetisme en licht combineren om kanker te bestrijden
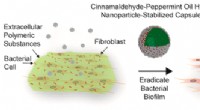
- Pepermuntolie en kaneel kunnen helpen bij het behandelen en genezen van chronische wonden
- Het fijnste goudstof ter wereld

- ORNL-microscopie brengt direct problematische lithiumdendrieten in batterijen in beeld

 Theoretische interpretaties van de pulsar-timinggegevens die onlangs zijn vrijgegeven door NANOGrav
Theoretische interpretaties van de pulsar-timinggegevens die onlangs zijn vrijgegeven door NANOGrav Met behulp van gegevens uit de echte wereld, wetenschappers beantwoorden belangrijke vragen over een atmosferische release
Met behulp van gegevens uit de echte wereld, wetenschappers beantwoorden belangrijke vragen over een atmosferische release Wat gebeurt er met het volume van een gas tijdens compressie?
Wat gebeurt er met het volume van een gas tijdens compressie?  Californië bestrijdt vuur met vuur om gigantische sequoia's te beschermen
Californië bestrijdt vuur met vuur om gigantische sequoia's te beschermen Willekeurige effecten sleutel tot het indammen van epidemieën
Willekeurige effecten sleutel tot het indammen van epidemieën Model helpt robots om meer te navigeren zoals mensen doen
Model helpt robots om meer te navigeren zoals mensen doen Afbeelding:Somber maanlandschap gemaakt voor rover-test
Afbeelding:Somber maanlandschap gemaakt voor rover-test Het volledige verhaal over klimaatverandering vereist een lange blik
Het volledige verhaal over klimaatverandering vereist een lange blik
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


