
Wetenschap
Borstkanker-op-een-chip voor het testen van geneesmiddelen voor immunotherapie

Borstkanker-chip. Krediet:Khademhosseini Lab
Er zijn veel mechanismen waarmee het lichaam reageert op vreemde indringers. Een daarvan betreft de T-cellen van het immuunsysteem, die een aantal verschillende eiwitten op hun oppervlak hebben die 'checkpoint-eiwitten' worden genoemd. Deze checkpoint-eiwitten binden aan eiwitten op het oppervlak van andere cellen en kunnen resulteren in stimulatie of onderdrukking van T-celactiviteit. Normaal gesproken, oppervlakte-eiwitten op vreemde of binnendringende cellen zullen een stimulatie van T-celactiviteit tegen deze cellen produceren, terwijl onderdrukking van T-cellen een ingebouwd mechanisme is om te voorkomen dat het immuunsysteem de normale lichaamscellen aanvalt.
tumorcellen, echter, kan soms het immuunsysteem te slim af zijn door oppervlakte-eiwitten te vertonen die binden met T-celcontrolepunteiwitten om onderdrukking van T-celactiviteit te veroorzaken. In sommige gevallen, interactie van deze tumoroppervlakte-eiwitten met T-cellen zorgt er zelfs voor dat de T-cellen scheuren. In recente jaren, wetenschappers hebben geprobeerd "checkpoint-remmer"-geneesmiddelen te ontwikkelen die deze onderdrukkende checkpoint-interacties tegengaan om de immuunrespons van het lichaam op tumorcellen te reactiveren. Een van deze geneesmiddelen is door de Amerikaanse FDA goedgekeurd voor de behandeling van gemetastaseerd melanoom; andere zijn beschikbaar of in ontwikkeling om andere maligniteiten te behandelen.
Ondanks deze vorderingen, echter, het blijft moeilijk om te bepalen welke kankerpatiënten waarschijnlijk in aanmerking komen voor dit type therapie en welke medicijnen het meeste potentieel hebben. Het ontwikkelen van een methode om deze uitdagingen aan te pakken, zou van groot belang zijn bij het bepalen van de veiligste, meest effectieve medicijnen voor kankerpatiënten, terwijl ze tegelijkertijd tijd en geld besparen. Om een dergelijke methode praktisch te maken voor klinisch gebruik, het moet in staat zijn om snel grote aantallen potentiële immunotherapie-geneesmiddelen tegen levende tumorcellen te testen voor nauwkeurige, gemakkelijk analyseerbare gegevens.
Een samenwerkend team van het Terasaki Institute for Biomedical Innovation (TIBI) heeft een dergelijk systeem met succes ontworpen en getest. Ze begonnen met het kweken van bolvormige aggregaten van borstkankercellen in een op maat gemaakte, 3D geprint, transparante chip met conische microwells. Deze microwells zijn ontworpen voor optimale groei en stabiliteit van de celbolletjes. Tests uitgevoerd op de cellulaire bolletjes van de microwells bevestigden de levensvatbaarheid van de cellen en hun productie van T-cel-deactiverende oppervlakte-eiwitten.
"De kenmerken van onze microwell-gebaseerde chip zijn de sleutel tot onze succesvolle ontwikkeling van een immunoactief weefselmodel, " zei Wujin Zon, doctoraat, van het team van het Terasaki Institute. "De transparantie van de chip maakt directe microscopische observatie mogelijk. En het ontwerp maakt testen in grote hoeveelheden mogelijk, die zich goed leent voor de snelle screening van immunotherapeutische geneesmiddelen."
Om de effectiviteit van checkpointremmers te testen bij het activeren van de antitumorrespons van T-cellen, het team onderzocht vervolgens hoe een T-cel zich normaal gedraagt tijdens activering. Wanneer een T-cel wordt gestimuleerd om cellulaire indringers aan te vallen, het scheidt eiwitten af die cytokinen worden genoemd, die andere immuuncellen naar de invasieplaats mobiliseren en de cellen stimuleren om zich te vermenigvuldigen en de indringers te vernietigen. Meting van deze cytokinen kan daarom het niveau van activering van een T-cel aangeven.
Het team creëerde vervolgens een efficiënte, geautomatiseerd systeem om cytokineniveaus te meten met behulp van hun met borstkanker beladen microwell-chip. Experimenten met dit systeem werden uitgevoerd met behulp van anti-checkpoint-eiwitgeneesmiddelen; de resultaten toonden aan dat bij incubatie van de borstkankercellen met de T-cellen, cytokineproductie werd verhoogd door het gebruik van de medicijnen, wat hun effectiviteit aantoont bij het activeren van de T-cellen.
Een andere manier waarop het team hun borstkankerchip gebruikte, was om het effect van de borstkankercellen op gestimuleerde T-cellen te beoordelen. De T-cellen werden fluorescerend gelabeld en toegevoegd aan de borstkankercellen in de microwells; de transparantie van de chip maakte directe observatie van hun cellulaire interactie mogelijk met behulp van fluorescentiemicroscopie. Deze borstkankercellen veroorzaken normaal gesproken scheuren van de T-cellen, maar experimenten uitgevoerd met controlepuntremmers toonden aan dat de medicijnen de levensvatbaarheid van T-cellen in de culturen verhoogden, visueel demonstreren hoe ze de effecten van T-celruptuur kunnen tegengaan door tumorcelinteractie.
De borstkankerchip werd ook gebruikt voor de directe observatie van hoe de T-cellen de cellulaire bollen van de borstkanker infiltreerden; dit type infiltratie is een maat voor de antitumoractiviteit en levensvatbaarheid van een T-cel. Na het labelen van elke groep cellen met afzonderlijke kleurstoffen en het mengen in de microwells van de chip, T-celinfiltratie kan direct worden gevisualiseerd met behulp van fluorescentiemicroscopie met hoge resolutie. Experimenten uitgevoerd met checkpoint-remmers gaven aan dat er meer T-cellen waren en dieper in de borstkankercellen doordrongen in de aanwezigheid van de medicijnen.
Samengevat, de TIBI-onderzoekers waren in staat om robuuste en efficiënte methoden te ontwerpen voor het karakteriseren van de interactie tussen tumor- en immuuncellen en voor snelle, grootschalige en klinisch relevante manieren om immunotherapeutische geneesmiddelen tegen tumorcellen te screenen. De microwell-chip en het bijbehorende apparaat kunnen ook worden gebruikt om andere typen tumorcellen en individuele patiëntcellen op te nemen voor het optimaliseren van de respons van de patiënt en voor het screenen en ontwikkelen van aanvullende geneesmiddelen tegen kanker.
"Manieren bieden om klinische beslissingen en gepersonaliseerde geneeskunde voor patiënten te optimaliseren, is een topdoel van ons instituut, " zei Ali Khademhosseini, doctoraat, directeur en CEO van het Terasaki Instituut. "Dit werk is een belangrijke stap in de richting van het bereiken van dat doel op het gebied van kankerimmunotherapie."
 Kunstmatige antimicrobiële peptiden kunnen helpen om resistente bacteriën te overwinnen
Kunstmatige antimicrobiële peptiden kunnen helpen om resistente bacteriën te overwinnen Wat wordt kalk gebruikt voor waterbehandeling?
Wat wordt kalk gebruikt voor waterbehandeling?  Nieuwe aanpak voor fotosynthetische productie van koolstofneutrale biobrandstof uit groene algen
Nieuwe aanpak voor fotosynthetische productie van koolstofneutrale biobrandstof uit groene algen Nieuwe rekentechniek lost gecomprimeerde röntgengegevens op
Nieuwe rekentechniek lost gecomprimeerde röntgengegevens op Aniondotering op hoog niveau voor snelle ladingsoverdrachtskinetiek voor condensatoren
Aniondotering op hoog niveau voor snelle ladingsoverdrachtskinetiek voor condensatoren
 Siciliaans dorp ruimt as op, stenen van de uitbarsting van de Etna
Siciliaans dorp ruimt as op, stenen van de uitbarsting van de Etna Overstromingen in Paraguay dwingen duizenden huizen te evacueren
Overstromingen in Paraguay dwingen duizenden huizen te evacueren Top 5 manieren waarop NASA het milieu helpt
Top 5 manieren waarop NASA het milieu helpt  Ozon op lagere breedtegraden herstelt niet, ondanks genezing van ozongaten in Antarctica
Ozon op lagere breedtegraden herstelt niet, ondanks genezing van ozongaten in Antarctica Gegevens over stedelijke emissies op lange termijn laten een afname zien in landen met een hoog inkomen
Gegevens over stedelijke emissies op lange termijn laten een afname zien in landen met een hoog inkomen
Hoofdlijnen
- Zelfs als je nog niet weet dat je ziek bent, je gezicht zal je verraden
- Hoe schat ik de celgrootte met een microscoop?
- Onderzoekers onthullen nieuwe inzichten in de controle van cellulaire steigers
- De Durian-industrie zou kunnen lijden zonder de bedreigde fruitvleermuis
- Een mogelijke verklaring voor hoe kiemlijnen worden verjongd
- Wat is celcompartimentering en waarom doet het zich voor?
- De effecten van tornado's op mens en natuur
- Vijf belangrijke orgaansystemen van het lichaam
- Wat zijn organellen in een prokaryotische cel?
- Zilveren nanodeeltjes in kleding wassen uit - en kunnen een bedreiging vormen voor de menselijke gezondheid en het milieu

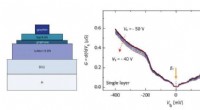
- Een nieuw platform om de elektronische eigenschappen van grafenen te bestuderen
- Kleurrijk eco-textiel dankzij enzymen van nanoformaat

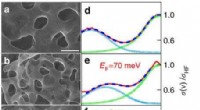
- Driedimensionaal grafeen:experiment bij BESSY II laat zien dat optische eigenschappen afstembaar zijn
- Chemici maken nanobuisstructuren die kunnen uitzetten en krimpen zonder af te breken

 Ruimtearcheologiestudie:leven en cultuur op het internationale ruimtestation
Ruimtearcheologiestudie:leven en cultuur op het internationale ruimtestation Southwest Airlines verschuift opnieuw MAX retourdatum
Southwest Airlines verschuift opnieuw MAX retourdatum Astronomen vinden aardachtige planeten die water kunnen bevatten
Astronomen vinden aardachtige planeten die water kunnen bevatten Hoe werkt een oliebron?
Hoe werkt een oliebron?  Wetenschappers ontdekken nieuwe vormen van veldspaat
Wetenschappers ontdekken nieuwe vormen van veldspaat De donkere kanten van planeten buiten het zonnestelsel delen verrassend vergelijkbare temperaturen
De donkere kanten van planeten buiten het zonnestelsel delen verrassend vergelijkbare temperaturen Hoe reproduceren Cheetahs?
Hoe reproduceren Cheetahs?  Wat is een propionzuur?
Wat is een propionzuur?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

