
Wetenschap
Nieuwe technologie voor het afleveren van nanocarrier-medicijnen passeert de bloed-hersenbarrière
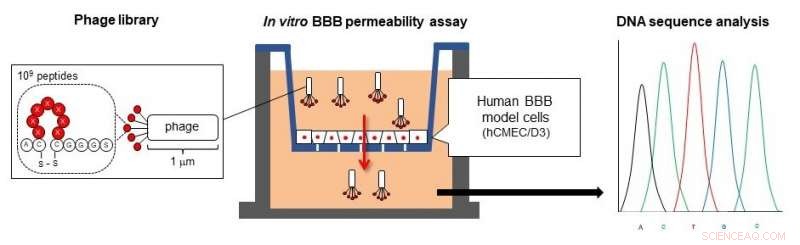
Een onderzoeksgroep van Kumamoto University verzamelde fagen die menselijke bloed-hersenbarrièremodelcellen binnendringen en analyseerde de aminozuursequentie van de peptiden op de doordringende fagen. Krediet:professor Sumio Ohtsuki
Een Japans onderzoeksteam heeft een cyclisch peptide (een keten van circulair gebonden aminozuren) ontwikkeld die de penetratie van de bloed-hersenbarrière (BBB) verbetert. Door het cyclische peptide aan het oppervlak van nanodeeltjes te hechten, onderzoek en ontwikkeling van nieuwe medicijn-nanodragers voor medicijnafgifte aan de hersenen wordt mogelijk.
In tegenstelling tot de bloedcirculatie naar de perifere organen in het lichaam, de BBB voorkomt verschillende stoffen, waaronder veel medicijnen, van het bloed naar de hersenen gaan. Biofarmaceutica en macromoleculaire geneesmiddelen trekken de aandacht als nieuwe behandelingen voor voorheen onbehandelbare ziekten en voor het verbeteren van de resultaten. Echter, deze geneesmiddelen met een hoog molecuulgewicht kunnen de BBB niet binnendringen. Technologieën die ze aan de hersenen kunnen leveren, zouden aanzienlijke vooruitgang opleveren bij de ontwikkeling van medicijnen die op de hersenen inwerken.
Gericht op het ontwikkelen van technologieën die toepasbaar zijn op verschillende drugs, een onderzoeksteam van Kumamoto University, Japan werkte aan de ontwikkeling van een cyclisch peptide dat de BBB kan binnendringen. In hun zoektocht naar een peptide met de gewenste functie, ze wendden zich tot virussen die fagen worden genoemd. Uit een faagbibliotheek met cyclische peptiden met 10 9 soorten aminozuursequenties, de onderzoekers zochten naar fagen die menselijke BBB-modelcellen konden binnendringen en analyseerden hun sequenties. Aangezien de grootte van een faag (ongeveer 1, 000 nanometer) is groter dan macromoleculaire geneesmiddelen, de wetenschappers verwachtten dat deze cyclische peptiden ook de penetratie van geneesmiddelen in de BBB mogelijk zouden maken.
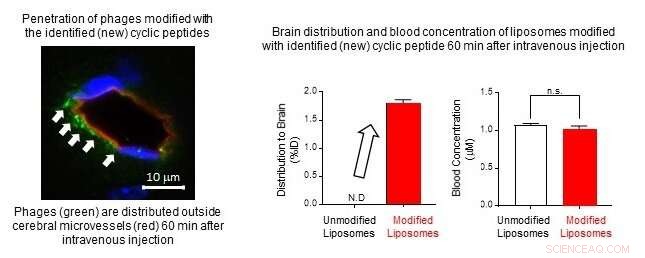
(Links) De fagen met het nieuwe cyclische peptide werden intraveneus in een muis geïnjecteerd. Zestig minuten later werden de hersenen geanalyseerd en werden fagen in de hersenen gedetecteerd. Krediet:professor Sumio Ohtsuki
Van de twee nieuwe cyclische peptiden die ze ontdekten, één bevorderde faagpenetratie, niet alleen in menselijke BBB-modelcellen, maar ook in BBB-modelcellen van apen en ratten. Verder, deze faag kon 60 minuten na intraveneuze injectie in de hersenen van een muis worden gevonden. In aanvullende experimenten, de onderzoekers wijzigden liposomen door het cyclische peptide aan het oppervlak van liposomen toe te voegen, waardoor kunstmatige nanodeeltjes van 150 nanometer werden gecreëerd. Toen dit gemodificeerde liposoom intraveneus in een muis werd geïnjecteerd, het werd 60 minuten later ook in de hersenen gedetecteerd, wat aantoont dat het nieuwe cyclische peptide de penetratie van faag- en liposoomnanodeeltjes door de BBB vergemakkelijkt, waardoor levering in de hersenen mogelijk is.
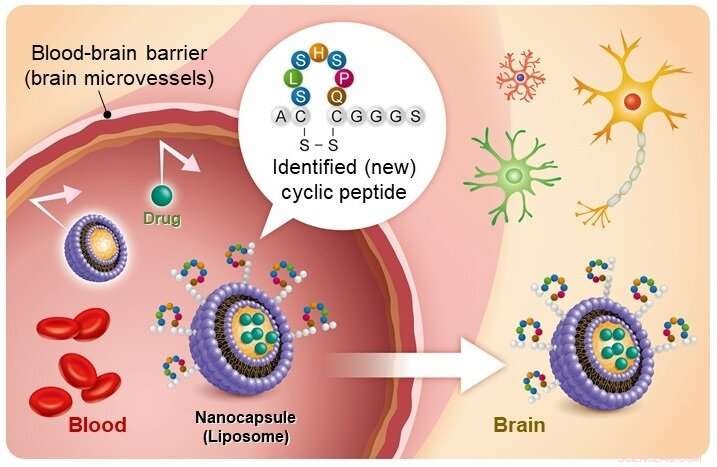
Het afleveren van geneesmiddelen door nanocarrier door de bloed-hersenbarrière kan worden gedaan met behulp van het nieuw ontdekte cyclische peptide. Krediet:professor Sumio Ohtsuki
"Liposomen zijn een nanodrager die verschillende stoffen kan inkapselen. Het liposoom waarvan het oppervlak is gemodificeerd met dit nieuwe cyclische peptide, kan worden gebruikt als een nanodrager om de BBB te omzeilen. Er is een manier geopend om macromoleculaire medicijnen aan de hersenen te leveren, " zei professor Ohtsuki. "We verwachten dat dit onderzoek aanzienlijk zal bijdragen aan de ontwikkeling van geneesmiddelen voor ziekten van het centrale zenuwstelsel, inclusief de ziekte van Alzheimer."
 Team werpt nieuw licht op fotosynthese
Team werpt nieuw licht op fotosynthese Efficiënte synthese van ginkgo-verbinding kan leiden tot nieuwe medicijnen, groene insecticiden
Efficiënte synthese van ginkgo-verbinding kan leiden tot nieuwe medicijnen, groene insecticiden Natuurkundige maakt ademhalingstoestellen van het type N95 met een suikerspinmachine
Natuurkundige maakt ademhalingstoestellen van het type N95 met een suikerspinmachine Verwoestend plantenvirus wordt in atomaire details onthuld
Verwoestend plantenvirus wordt in atomaire details onthuld Nieuwe röntgentechnologie kan een revolutie teweegbrengen in de manier waarop artsen afwijkingen identificeren
Nieuwe röntgentechnologie kan een revolutie teweegbrengen in de manier waarop artsen afwijkingen identificeren
 Nieuwe methode om de temperatuur van de ijskap op afstand te meten gedemonstreerd
Nieuwe methode om de temperatuur van de ijskap op afstand te meten gedemonstreerd Welke dieren leven op de pelagische zone?
Welke dieren leven op de pelagische zone?  Hoe ecotoerisme inheemse gemeenschappen kan schaden
Hoe ecotoerisme inheemse gemeenschappen kan schaden Fettuccine Rock zou het leven op Mars kunnen signaleren
Fettuccine Rock zou het leven op Mars kunnen signaleren  Studie laat zien hoe mens en natuur significante veranderingen teweegbrengen in de gezondheid van mondiale rivieren
Studie laat zien hoe mens en natuur significante veranderingen teweegbrengen in de gezondheid van mondiale rivieren
Hoofdlijnen
- Welke organellen bevinden zich in een prokaryote cel?
- mRNA: definitie, functie en structuur
- Nieuwe procedure voor snellere detectie van milieueffecten van zalmkwekerijen
- Hoe werkt het skeletsysteem met het ademhalingsstelsel?
- Iraakse dierenliefhebbers gaan online om zwerfdieren in Bagdad te redden
- Hoe een tRNA-reeks te krijgen van een DNA-reeks
- Zilte zwembadbacteriën kunnen opruimen en opstarten
- Onderzoek toont aan dat bodemradar fijne wortels in gewassen kan detecteren
- Welke cellen kunnen worden gezien door het menselijk oog?
- Onderzoekers stemmen wrijving in ionische vaste stoffen af op nanoschaal
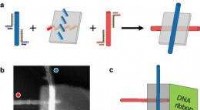
- Wetenschappers ontwikkelen DNA-origami-broodplanken op nanoschaal voor circuits van koolstofnanobuisjes
- De massa van massaloze elektronen meten

- High-throughput ontdekking van 2D-magneten
- Nieuwe vezel-nanogeneratoren kunnen leiden tot elektrische kleding

 Bijwerkingen Cetylpyridiniumchloride
Bijwerkingen Cetylpyridiniumchloride Onderzoekers bouwen een deeltjesversneller die op een chip past
Onderzoekers bouwen een deeltjesversneller die op een chip past Astronomen brengen enorme leegte in kaart in onze kosmische omgeving
Astronomen brengen enorme leegte in kaart in onze kosmische omgeving Praktische werkgerelateerde taken kunnen burn-out bij nieuwe medewerkers verminderen
Praktische werkgerelateerde taken kunnen burn-out bij nieuwe medewerkers verminderen Wat zijn enkele ideeën voor 3D-wiskundeprojecten?
Wat zijn enkele ideeën voor 3D-wiskundeprojecten?  Lab sondes moleculaire limiet van plasmonics
Lab sondes moleculaire limiet van plasmonics Hoe de massa van een Cube
Hoe de massa van een Cube Nieuwe techniek voor het maken van lichtgewicht materialen die stijver en sterker zijn dan voorheen mogelijk was
Nieuwe techniek voor het maken van lichtgewicht materialen die stijver en sterker zijn dan voorheen mogelijk was
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Swedish | German | Dutch | Danish | Norway | Portuguese |

-
Wetenschap © https://nl.scienceaq.com

