
Wetenschap
Een revolutie in de ontwikkeling van vaccins, maar zullen we er allemaal van profiteren?

Dankzij nieuwe technologie, het is misschien mogelijk om over drie maanden een vaccin tegen het nieuwe coronavirus klaar te hebben voor testen op mensen. Meestal duurt dit enkele jaren, zegt de auteur van dit artikel. Krediet:Spondylolithesis/iStock
Door de "instructiehandleidingen" te manipuleren die de celfunctie in ons lichaam regelen, we zullen binnenkort veel ziekten kunnen bestrijden, inclusief de nieuwe uitbraak van het coronavirus. Echter, in het slechtste scenario, dergelijke innovaties zullen alleen de rijken ten goede komen.
Onlangs, er werd gemeld dat binnen een maand een vaccin tegen het nieuwe coronavirus klaar zou kunnen zijn voor dierproeven, en op mensen binnen drie maanden. Dit proces duurt normaal gesproken enkele jaren, maar innovatieve vaccintechnologie kan het werk met recordsnelheden doen.
De nieuwe technologie maakt gebruik van mRNA (afkorting van messenger RNA), die nucleïnezuren draagt - de chemische 'bouwstenen' van het leven. Messenger RNA fungeert als een "werkkopie" van de genen (gemaakt van DNA) die ons lichaam moet lezen om de eiwitten te maken die de levensprocessen in onze cellen aansturen. RNA vertegenwoordigt een familie van moleculen die structureel vergelijkbaar is met DNA.
Onderzoek naar mRNA wordt in razend tempo uitgevoerd, maar is grotendeels in handen van een klein aantal farmaceutische bedrijven uit de particuliere sector. Dit is lastig vanuit het oogpunt van de volksgezondheid.
Extreem duur
Zoals het geval is met momenteel beschikbare geneesmiddelen die andere vormen van RNA bevatten, vaccins en medicijnen op basis van mRNA kunnen extreem duur zijn om te produceren.
Als iedereen, inclusief de armsten in de samenleving, gaat deelnemen aan de gezondheidsrevolutie beloofd door mRNA-technologie, onderzoek moet in alle sectoren plaatsvinden en mag niet worden beperkt tot particuliere ondernemingen.
Maar daarvoor is de publieke sector nodig, zowel in Noorwegen als wereldwijd, om in deze technologie te investeren.
Grote ruimte voor verbetering
Laten we duidelijk zijn. De vaccins die we tegenwoordig gebruiken, vormen een solide basis voor de wereldwijde gezondheid.
De ontwikkeling van een traditioneel antiviraal vaccin begint meestal met de isolatie van het geheel of delen van een pathogeen virus, die vervolgens min of meer inactief wordt. Het wordt vervolgens in het lichaam geïnjecteerd om een vereiste immuunrespons te stimuleren.
Deze strategie werkt sinds het einde van de 18e eeuw, toen het eerste pokkenvaccin werd ontwikkeld.
Maar sindsdien is er veel gebeurd. Volgens de particuliere stichting die door Bill en Melinda Gates is opgericht om de ontwikkeling van vaccins te ondersteunen, vaccins hebben tussen 1990 en 2017 het leven van 122 miljoen kinderen gered.
Echter, er is nog veel ruimte voor verbetering.
Afscheid van allergische reacties
De huidige benaderingen voor de ontwikkeling van vaccins zijn gecompliceerde processen die worden gekenmerkt door veel onzekerheid en veel testen, wat allemaal tijd kost.
Bovendien, virussen die in vaccins worden gebruikt, moeten zo zijn ontworpen dat ze precies het juiste niveau van virulentie bereiken dat de gewenste immuunrespons stimuleert. Als de stimulatie te mild is, het vaccin heeft geen effect. Als het te sterk is, de ontvanger wordt ziek.
Veel van onze huidige vaccins bevatten ook sporen van de verbinding formaline, die in enkele gevallen allergische reacties veroorzaken. Maar formaline kan worden geëlimineerd als we vaccins op basis van mRNA gebruiken.
Dus wat is het geheim?
Handleiding voor de cellen in ons lichaam
Messenger RNA is in feite een "handleiding" waarnaar onze cellen verwijzen om eiwitten te maken. Eiwitten zijn essentieel voor de opname en verwerking van voedingsstoffen in ons lichaam, evenals de afbraak van schadelijke stoffen en lichamelijke vernieuwing.
De meest voorkomende medicijnen werken door eiwitfuncties te veranderen. Echter, deze veranderingen zijn vaak onnauwkeurig - met bijwerkingen die van onbeduidend tot levensbedreigend kunnen zijn.
Messenger RNA bestaat uit vier nucleïnezuurcomponenten afgekort tot A, jij, C en G. De configuratie van deze componenten wordt gelezen door de cellen zoals de instructies in een kookrecept. Als de mRNA-instructies niet kunnen worden gelezen, zijn boodschap zal geen effect hebben en er zullen zich dus geen bijwerkingen ontwikkelen. Maar als het bericht goed wordt gelezen, het lichaam zal precies de juiste soorten eiwitten maken die het nodig heeft - niet meer en niet minder, op het juiste moment en op de juiste plaats.
Vaccins en andere medicijnen die op dit proces zijn gebaseerd, openen dus de deur naar verbazingwekkende mogelijkheden.
Eiwitcoderende virusfragmenten verpakt in synthetische moleculen
Zodra de genetische samenstelling van een nieuw virus in kaart is gebracht, we kunnen de belangrijkste fragmenten ervan coderen in een synthetisch mRNA-molecuul en het als een vaccin aan het lichaam afleveren.
Het lichaam gebruikt de instructies in het vaccin om een nieuw eiwit te maken. Het immuunsysteem reageert, maar de beschermende reactie vordert zonder enig risico op infectie. Op deze manier, het lichaam maakt zich klaar om het virus te bestrijden wanneer het zijn intrede doet.
De uitdaging waar we voor staan is dus tweeledig. Ten eerste, de productie en het beheer van mRNA is een veeleisend proces. Ten tweede, het is moeilijk gebleken om de genetische "werkkopieën" intact af te leveren op de locaties in onze cellen waar ze het meest nodig zijn. Echter, wetenschappers hebben deze problemen overwonnen door mRNA-moleculen te verpakken in op lipiden gebaseerde nanocapsules - en zo de weg vrij te maken voor de behandeling van een hele reeks ziekten.
Kanker bestrijden
De lijst met mogelijke toepassingen varieert van geneesmiddelen ter bestrijding van kanker, erfelijke genetische aandoeningen en neurologische ziekten, tot vaccins tegen infecties.
Bij SINTEF, we werken aan het gebruik van nanodeeltjes-mRNA bij de behandeling van zogenaamde triple-negatieve borstkanker, wat een van de meest dodelijke vormen van de ziekte is. Dit werk maakt deel uit van een project genaamd EXPERT dat door de EU wordt gefinancierd met 150 miljoen NOK.
In op nanodeeltjes gebaseerde oplossingen van dit type, het mRNA-fragment kan gemakkelijk worden vervangen zonder dat het medicijn zich anders in het lichaam verdeelt. Dus, wanneer we nieuwe feiten over een bepaalde ziekte verkrijgen, de weg naar een effectieve medicamenteuze behandeling kan kort zijn.
Betrokkenheid van de publieke sector
De keerzijde van dit verhaal zijn de hoge kosten die gepaard gaan met RNA-medicamenteuze behandelingen, en hier ligt de uitdaging. Door de wereldwijde investeringen van de publieke sector in onderzoek op dit gebied te consolideren, het kan mogelijk zijn om de monopolisering van de productie van mRNA-geneesmiddelen door marktgestuurde particuliere ondernemingen te voorkomen.
Alleen op deze manier kan mRNA-technologie worden toegepast in het belang van iedereen - in lijn met de duurzaamheidsdoelstellingen van de VN.
 Een kraftig afvalproduct gebruiken:op weg naar een lager brandstofverbruik
Een kraftig afvalproduct gebruiken:op weg naar een lager brandstofverbruik Onderzoekers hopen dat een robo-neus K-9-officieren een pauze kan geven
Onderzoekers hopen dat een robo-neus K-9-officieren een pauze kan geven Tegengestelde actie zou de industriële gasscheiding kunnen verbeteren
Tegengestelde actie zou de industriële gasscheiding kunnen verbeteren Handheld spectrale analysator verandert smartphone in diagnostisch hulpmiddel
Handheld spectrale analysator verandert smartphone in diagnostisch hulpmiddel Chemici vereenvoudigen de synthese van antitumorverbindingen
Chemici vereenvoudigen de synthese van antitumorverbindingen
Hoofdlijnen
- Wat zijn de vijf belangrijkste functies van het skeletsysteem?
- DNA-ontdekking kan licht werpen op zeldzame kinderziekte
- Voorspelling (biologie): definitie, soorten en voorbeelden
- Zouden herten aanwijzingen kunnen bevatten over het verband tussen malariaresistentie en sikkelcel?
- Het is onwaarschijnlijk dat de jacht op trofeeën de evolutie beïnvloedt
- Lichtgroene planten besparen stikstof zonder in te boeten aan fotosynthetische efficiëntie
- Het belang van het bestuderen van de DNA-genetica van het menselijk geslacht
- Zeeleeuwen hebben unieke snorharen waarmee ze zelfs de snelste vis kunnen vangen
- De morfologie van algen
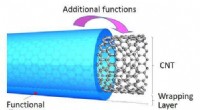
- Het verpakken van koolstofnanobuisjes in polymeren verbetert hun prestaties
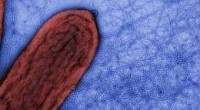
- Onderzoeksteam ontdekt nieuwe geleidende eigenschappen van door bacteriën geproduceerde draden
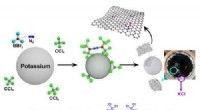
- Studie opent band-gap grafeen
- Technische materialen:op maat gemaakte magneten

- Wetenschappers onderzoeken transport van nanodeeltjes in het menselijk lichaam
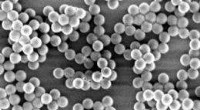
 Nieuw ecologisch proces om goedkopere biobrandstof te produceren
Nieuw ecologisch proces om goedkopere biobrandstof te produceren Wild-dweilingen identificeren
Wild-dweilingen identificeren Beter begrip van waterstofperoxideregulatie kan leiden tot nieuwe inzichten in ziekteontwikkeling
Beter begrip van waterstofperoxideregulatie kan leiden tot nieuwe inzichten in ziekteontwikkeling Skelet van T-rex zou recordprijs kunnen halen op veiling in New York
Skelet van T-rex zou recordprijs kunnen halen op veiling in New York De gezondheidszorg is een belangrijke bron van schadelijke emissies
De gezondheidszorg is een belangrijke bron van schadelijke emissies Keramische honingraatluchtfilters kunnen stadsvervuiling verminderen
Keramische honingraatluchtfilters kunnen stadsvervuiling verminderen Materialen die worden gebruikt voor het maken van plastic zakken
Materialen die worden gebruikt voor het maken van plastic zakken Alexa als je nieuwe bestie:kan een AI-robot of stemassistent je helpen om je minder eenzaam te voelen?
Alexa als je nieuwe bestie:kan een AI-robot of stemassistent je helpen om je minder eenzaam te voelen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

