
Wetenschap
Onderzoekers ontwikkelen spuit-injecteerbare, zelfuitbreidbare en ultraaanpasbare magnetische nanosheets
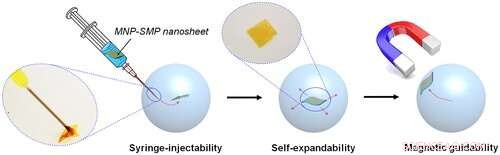
Krediet:ACS
Spuit-injecteerbare biomaterialen, medische hulpmiddelen en gemanipuleerde weefsels hebben veel aandacht getrokken als minimaal invasieve implantaten voor diagnose, therapie en regeneratieve geneeskunde.
vrijstaande polymere ultradunne films, gewoonlijk aangeduid als polymere nanosheets, zijn een van de meest gebruikte platforms voor biomedische apparaten met injectiespuiten vanwege hun flexibiliteit en vervormbaarheid.
Deze nanosheets zijn minder dan 1 micrometer dik, die dunner is dan een haarlok (haar is meestal ongeveer 100 micrometer breed). Ze zijn een veelbelovend platform voor medicijnafgifte door middel van naaldinjectie.
Ondanks de recente ontwikkeling in nanosheettechnologieën die gebruik maken van polymelkzuur (PLA) en polymelkzuur-co-glycolzuur (PLGA), polymere nanosheets moeten nog verschillende technische uitdagingen overwinnen om als een effectief injecteerbaar platform te dienen:namelijk, beperking in de grootte van nanosheets die kunnen worden geïnjecteerd via medische naalden, suboptimale mechanische robuustheid (bijv. scheuren tijdens injectie), en beperkte controle over vormherstel en bewegingscontrole na injectie.
Om deze beperkingen te overwinnen, onderzoekers van het Digital Manufacturing and Design (DManD) Centre in de Singapore University of Technology and Design (SUTD) ontwikkelden nanosheets met behulp van op polyurethaan gebaseerd vormgeheugenpolymeer (SMP) en magnetische nanodeeltjes (MNP) om ongekende mogelijkheden te demonstreren om nanosheets te verwerken. SMP biedt twee unieke mechanische eigenschappen:een grote verandering in de Young's moduli door de verandering in temperatuur, en vormgeheugeneffect (SME) om de opgeslagen vorm te herstellen.
In aanvulling, de onderzoekers toonden aan dat de gefabriceerde SMP-nanosheets magnetisch kunnen worden gemaakt met MNP om contactloze bewegingscontrole uit te voeren met behulp van een extern magnetisch veld. specifiek, de volgende vier mogelijkheden werden gedemonstreerd door gebruik te maken van de 710 nm dikke nanosheet met de glasovergangstemperatuur (Tg) van 25 °C:spuitinjecteerbaarheid door medische naalden, zelfuitbreidbaarheid na uitwerpen, vervormbaarheid en verwijderbaarheid op de biologische oppervlakken, en geleidbaarheid in een extern magnetisch veld. Deze mogelijkheden maken in vivo praktische toepassingen mogelijk als een injectiespuit-injecteerbaar platform.
Als bijkomend voordeel, de verandering van de modulus door temperatuur biedt een uniek vermogen om de hechting en verwijdering van de MNP-SMP nanosheet op de biologische oppervlakken te regelen. Dit zou moeilijk te bereiken zijn geweest met conventionele nanosheets met een constante modulus en is niet eerder aangetoond.
Het overwegen van de injectie met injectiespuiten van moleculaire medicijnen of cellulaire constructies in interne organen, de onderzoekers voegden aan de MNP-SMP nanosheets een extra laag PLGA toe, dat vooral bekend staat als een biomateriaal dat wordt gebruikt voor medicijnafgifte, om de functionaliteit als drager van moleculaire en cellulaire geneesmiddelen uit te breiden. Dit kan worden gedaan zonder afbreuk te doen aan de aangetoonde mogelijkheden. SMP en MNP boden dezelfde mogelijkheden aan de nanosheets met een extra laag PLGA, suggereert het enorme potentieel van de ontwikkelde nanosheets voor medicijn- en celafgifte.
"De MNP-SMP-nanobladen kunnen verder worden gefunctionaliseerd door medicijnen te laden of af te drukken, cellen en elektrische circuits op het oppervlak door opkomende printtechnologieën te integreren, zoals inkjetprinten, 3D-printen en bioprinten, " zei Dr. Kento Yamagishi van SUTD, de hoofdauteur van het artikel.
"De MNP-SMP-nanosheets zullen bijdragen aan de ontwikkeling van geavanceerde injectiespuit-injecteerbare medische apparaten als een platform om medicijnen en cellen naar de specifieke plaats of laesie in het lichaam te brengen voor minimaal invasieve diagnose en therapie, " voegde hoofdonderzoeker toe, Universitair docent Michinao Hashimoto van SUTD.
 Synergie voor opslag:al duizenden jaren kernafval bevatten
Synergie voor opslag:al duizenden jaren kernafval bevatten Dagelijks gebruik van Helium Gas
Dagelijks gebruik van Helium Gas Wetenschappers automatiseren de analyse van de elektrolytsamenstelling voor de productie van aluminium
Wetenschappers automatiseren de analyse van de elektrolytsamenstelling voor de productie van aluminium Kijken naar een medicijn in actie:precieze werking antikankermedicijnen in de cel opgehelderd
Kijken naar een medicijn in actie:precieze werking antikankermedicijnen in de cel opgehelderd Wetenschappers kijken naar vetmetabolisme in levende vissen, observeer real-time lipidenbiochemie
Wetenschappers kijken naar vetmetabolisme in levende vissen, observeer real-time lipidenbiochemie
 Branden verdrievoudigen in moerasland Pantanal in Brazilië in 2020
Branden verdrievoudigen in moerasland Pantanal in Brazilië in 2020 Wil je iets doen aan klimaatverandering, maar weet je niet hoe? Het aanpassen van deze 3 delen van je leven zal het grootste verschil maken
Wil je iets doen aan klimaatverandering, maar weet je niet hoe? Het aanpassen van deze 3 delen van je leven zal het grootste verschil maken Nieuw onderzoek onthult hoe orkaan Lane vuur en regen naar de Hawaiiaanse eilanden bracht
Nieuw onderzoek onthult hoe orkaan Lane vuur en regen naar de Hawaiiaanse eilanden bracht Afbeelding:NASA's Aqua-satelliet legt rook vast die voor de kust van Californië opstookt
Afbeelding:NASA's Aqua-satelliet legt rook vast die voor de kust van Californië opstookt Vijf manieren waarop kunst kan helpen de plasticcrisis op te lossen
Vijf manieren waarop kunst kan helpen de plasticcrisis op te lossen
Hoofdlijnen
- Hoeveel zintuigen heeft een mens?
- Is het ethisch om stamcellen te gebruiken?
- Type energie geproduceerd door fotosynthese
- Nieuwe gen-editor gebruikt om ziekte in embryo's op te lossen:studie
- Een ezelsverhaal:Nigeria wordt de belangrijkste exporthub voor verstoppingen
- Campylobacter gebruikt andere organismen als Trojaans paard om nieuwe gastheren te infecteren
- Antibiotica ontdekking in de afgrond
- Hoe een bloeiende legale marihuana-industrie de luchtkwaliteit kan schaden
- Wat is nodig voor de glycolyse om te beginnen?
- Wetenschappers vinden mogelijke vervanging voor platina als katalysator

- Onderzoekers bereiken bijna de kwantumlimiet met nanodrums

- Wetenschappers gebruiken DNA om een transistor te assembleren uit grafeen

- Wetenschappers maken zilveren nanodraden op basis van DNA-moleculen

- Ontwikkeling van kostenefficiënte elektrokatalysator voor waterstofproductie
 Tools ontwikkelen om nepnieuws te bestrijden
Tools ontwikkelen om nepnieuws te bestrijden DNA programmeren om medicijnen tegen kanker af te leveren
DNA programmeren om medicijnen tegen kanker af te leveren Wetenschapper brengt gigantisch virus in kaart
Wetenschapper brengt gigantisch virus in kaart Weerpatronen in woestijnen
Weerpatronen in woestijnen  Het vertrek van Amazon kan techbedrijven uit New York afschrikken
Het vertrek van Amazon kan techbedrijven uit New York afschrikken Nepnieuws-vaccin werkt:Pre-bunking-game vermindert de gevoeligheid voor desinformatie
Nepnieuws-vaccin werkt:Pre-bunking-game vermindert de gevoeligheid voor desinformatie Groeiende wereldbevolking:onderzoek naar voedselproductie mist een holistisch perspectief
Groeiende wereldbevolking:onderzoek naar voedselproductie mist een holistisch perspectief FAA beveelt inspecties van Boeing 737 NG-vliegtuigen op structurele scheuren
FAA beveelt inspecties van Boeing 737 NG-vliegtuigen op structurele scheuren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

