
Wetenschap
Isoleren van intacte bacteriën uit bloed met behulp van een microfluïdisch monolietapparaat
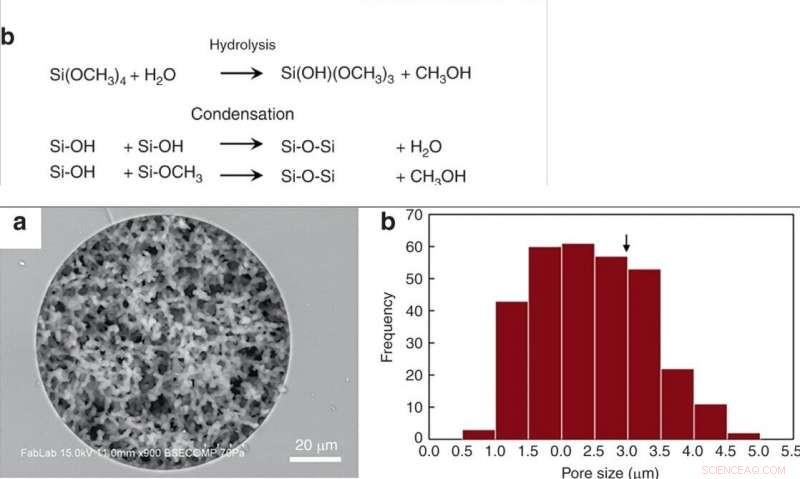
TOP:(a) Synthese van poreuze silicamonoliet in capillaire en thermoplastische schimmel van fused silica via sol-gel-chemie. (b) Competitieve reacties tijdens de synthese van monoliet. Silanolgroepen die aanwezig zijn op glascapillairen vormen tijdens deze stap covalente bindingen met de monoliet. BODEM:(a) SEM-beeld van een silica-monoliet gesynthetiseerd in een fused silica-capillair van 100 m ID, onthullende uniforme porositeit en uitstekende wandverankering van de monoliet. (b) Histogram van poriegrootte. De kritische diameter voor RBC-hemolyse (2r*) is gemarkeerd met een pijl. Krediet:microsystemen en nano-engineering, doi:10.1038/s41378-019-0063-4
Opkomende eencellige diagnostiek vertrouwt op het potentieel om bacteriën snel en efficiënt te isoleren uit complexe biologische matrices. In een recente studie die nu is gepubliceerd in Microsystemen en nano-engineering , Jung Y. Han en collega's van de interdisciplinaire faculteiten Werktuigbouwkunde, Chemical Biomolecular Engineering en Bioengineering in de VS hebben een apparaat ontwikkeld om intacte en levensvatbare bacteriën uit volbloed te isoleren met behulp van een microfluïdische, poreuze silica monoliet. Ze bereikten mechanische hemolyse en zorgden voor doorgang van intacte en levensvatbare bacteriën door de monolieten voor op grootte gebaseerde bacteriële isolatie en selectieve lysis. Han et al. beschreef een proces om grote hoeveelheden discrete capillairgebonden monolietelementen en millimeterschaal monolietstenen te synthetiseren om te integreren in microfluïdische chips.
Ze onderzochten de impact van monolithische morfologie, geometrie en stroomomstandigheden op cellysis en stroomregimes die selectieve cellysis en selectieve passage van meerdere gram-negatieve en gram-positieve bacteriën mogelijk maakten. De techniek van Han et al. maakte snelle monstervoorbereiding en bacteriële analyse mogelijk in combinatie met eencellige Raman-spectrometrie. Het werk biedt unieke monstervoorbereidingsstappen ter ondersteuning van snelle en kweekvrije bacteriële analyse voor toepassingen in point-of-care biomedische apparaten.
Bacteriën in het bloed kunnen leiden tot sepsis, infectie van weefsels en andere ernstige medische aandoeningen, die vroege identificatie van bloedoverdraagbare bacteriën vereisen voor een effectieve behandeling. Het vermogen om bacteriën snel te identificeren met behulp van point-of-care-diagnostiek kan het klinische potentieel voor een optimale behandeling tijdens infectie in een vroeg stadium aanzienlijk vergroten. De bestaande gouden standaard voor bacteriële karakterisering is gebaseerd op fenotypische celcultuuranalyse en vereist ten minste 24 uur om monsters te verzamelen voor kweek en analyse in een diagnostisch en klinisch microbiologisch laboratorium. De bestaande techniek is robuust en goedkoop, maar kan geen tijdige resultaten opleveren om de beginfasen van de behandeling te begeleiden.
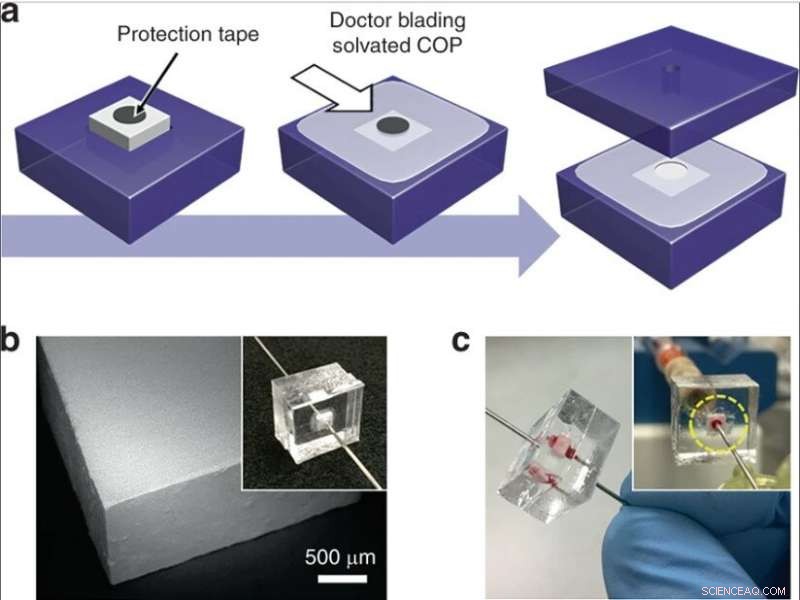
(a) Integratie van een silica-monolietsteen in een thermoplastische chip. Een cirkelvormige tape wordt op een monoliet geplaatst die in een COP-substraat is gestoken, en gesolvateerde COP wordt aangebracht op het blootgestelde oppervlak. Na gedeeltelijk drogen, de band wordt verwijderd, het apparaat is omsloten door een ander COP-substraat, en vloeistofpoorten worden in gaten gestoken die een stroompad door de monoliet verschaffen. (b) SEM-beeld van een monolietbaksteen gesneden door een wafelblokjeszaag. (c) Afbeelding van een apparaat tijdens volbloedperfusie. Krediet:microsystemen en nano-engineering, doi:10.1038/s41378-019-0063-4
In het huidige werk, Han et al. verkende microfluïdische apparaten geïntegreerd met poreuze silica-monolieten als eenvoudige doorstroomelementen voor selectieve bloedcelanalyse en de intacte isolatie van bacteriën. Monolieten zijn zeer poreuze materialen die zijn samengesteld uit open celmorfologie met kronkelende paden van vloeistofstroom. Wetenschappers kunnen monolithische poriemorfologie beheersen via hoge mechanische oppervlaktespanning tijdens celperfusie voor mechanische hemolyse van bloedcellen, terwijl intacte en levensvatbare bacteriën de kronkelende stroompaden kunnen afleggen voor hun cultuurvrije isolatie. Han et al. gebruikte de benadering van selectieve passage voor bacteriën in volbloed onder stroomomstandigheden voor gram-positieve en gram-negatieve soorten, ondanks verschillen van de bacteriestammen. De techniek van selectieve monolietlysis met hoge doorvoer in combinatie met krachtige analytische methoden zoals Raman-spectroscopie kan een cultuurvrije analyse van bacteriën in volbloed op het niveau van de enkele cel mogelijk maken.
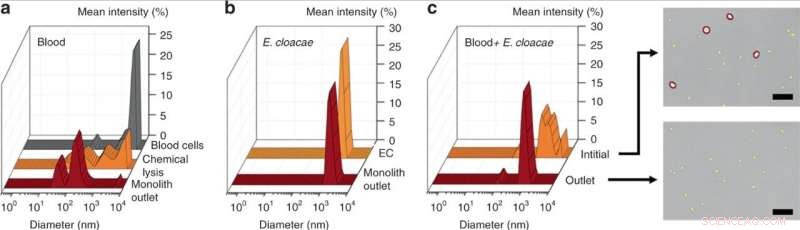
DLS-meting van (a) initiële 25× verdund bloed, chemisch gelyseerd bloed, en bloed gelyseerd door perfusie door het monolietapparaat, het onthullen van een significante vermindering van de grootte van celresten voor mechanische monolietlysis ten opzichte van chemische lysis. (b) DLS-meting van E. cloacae gesuspendeerd in 1 × PBS, en monster geperfuseerd door het monolietapparaat, toont geen verandering in de grootte van bacteriën. (c) DLS-meting van 100 × verdund bloed verrijkt met E. cloacae, en monster verzameld uit de uitlaat van een poreuze monoliet. De brede piek in het inlaatmonster duidt op een gemengde populatie van bloedcellen en kleine bacteriële cellen, terwijl het uitlaatmonster een significante vermindering van grote (> 2 m) cellen vertoonde, zoals bevestigd in de optische beelden. Schaalbalken = 25 µm. Krediet:microsystemen en nano-engineering, doi:10.1038/s41378-019-0063-4
Han et al. gemodificeerde eerder gerapporteerde siliciummonolietsyntheseprocessen, gevolgd door hydrolyse en condensatie van silica tot silicaglas bij lage temperaturen. Om de silicamonoliet te bereiden, de wetenschappers gebruikten een voorloperoplossing bestaande uit alkylsilicaten, polyethyleenglycol (PEG) als porogeen, ureum als bron van hydroxylionen om heterogeniteit en azijnzuur te minimaliseren. Toen ze het synthetische proces optimaliseerden, de resulterende monolieten waren homogeen en goed verankerd aan de capillaire wanden van silica. De wetenschappers maten de dikte van de uiteindelijke monolietstructuur van het skelet en berekenden de permeabiliteit ervan met behulp van hoogwaardige vloeistofchromatografie om experimentele omstandigheden te beheersen. Om intrinsieke variatie te minimaliseren, Han et al. snijd de resulterende capillaire buisjes in segmenten van 5 cm lang om de permeabiliteit voor gebruik te testen.
Vervolgens ontwikkelden ze twee complementaire methoden voor lage en hoge doorvoer om silicamonolieten te integreren in microfluïdische systemen. Om een lage doorvoer mogelijk te maken, de wetenschappers hebben monolietbevattende capillaire segmenten ingebed in thermoplastische microfluïdische chips om de monoliet tijdens integratie te beschermen. Voor selectieve lysis met hoge doorvoer gebruikten ze monolieten met grotere dwarsdoorsnede-oppervlakken binnen de microfluïdische apparaten. De complete fabricagemethode leverde een uitstekende betrouwbaarheid op voor een lekvrije werking tijdens volbloedperfusie.
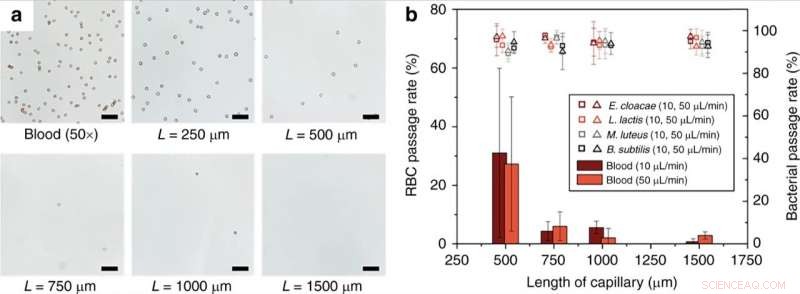
(a) Monolietlengte-afhankelijkheid van RBC-hemolyse. helemaal, 50 x verdund bloed in 1 x PBS werd geperfuseerd door capillaire monolieten van verschillende lengtes met een stroomsnelheid van 10 L / min. (b) Doorgangssnelheid van RBC en levensvatbare bacteriën bij verschillende stroomsnelheden en lengtes van monolietbevattend capillair. Schaalbalken = 50 m. Foutbalken zijn ±1SD. Contrast van optische beelden werd aangepast voor zichtbaarheid. Krediet:microsystemen en nano-engineering, doi:10.1038/s41378-019-0063-4
Als proof-of-principle, Han et al. geselecteerde Enterobacter cloacae (gram-negatief, staafvormige bacteriën) om hun doeltreffendheid van passage te onderzoeken, naast drie gram-positieve bacteriën; Lactococcus lactis, Micrococcus luteus en Bacillus subtilis. Tijdens de experimenten, ze perfuseerden bacteriële oplossingen door de microfluïdische monolieten met verschillende geometrie en stroomomstandigheden om de passage van bacteriën en de lysis van bloedcellen te testen met behulp van dynamische lichtverstrooiing (DLS). Bijvoorbeeld, de perfusie van gezuiverde E. cloacae door de monoliet leverde geen waarneembare veranderingen in de DLS-pieken op, wijst op de intacte passage van bacteriën.
De wetenschappers toonden het effect van de lengte van het poreuze monolietapparaat op de efficiëntie van de lysis van rode bloedcellen (RBC). De resultaten gaven aan dat de RBC-lysis-efficiëntie significant toenam voor monolietlengtes boven 1 mm. Han et al. bestudeerde ook het lot van witte bloedcellen (WBC's) tijdens de werking van het monolietapparaat, de cellen konden niet door de monoliet gaan zonder te worden gelyseerd, vergelijkbaar met RBC's. Technisch gezien, RBC's vervormd tot een schijfvorm om door de monoliet te gaan, wat een significant verhoogde membraanspanning veroorzaakte om te resulteren in RBC-lysis. Ter vergelijking, bacteriële cellen hadden vergelijkbare afmetingen als de monolietporiën en hadden daarom minder celwandexpansie nodig voor een succesvolle passage zonder breuk. De wetenschappers optimaliseerden de parameters van het apparaat zodat verschillende bacteriën hoge niveaus van membraanstress kunnen verdragen zonder te scheuren. Verdere ontwikkelingen zorgden voor een intacte passage van bacteriën zonder afbraak en met levensvatbaarheid.
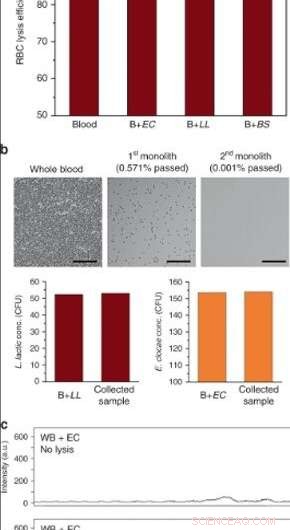
(a) RBC-lysis-efficiëntie van volbloed in apparaten met hoge doorvoer na perfusie bij 10 L / min (EC E. cloacae, LL L. lactis, BS B. subtilis. Foutbalken zijn ±SD. N = 3 voor bloed en B + EC, en N = 2 voor B + LL, B + BS. (b) Bloedcellysis en bacteriële scheiding na seriële operatie met behulp van twee monolieten. Oppervlakken werden gepassiveerd met BSA/Tween 20. Meer dan 99,999% RBC-lysis werd verkregen met behoud van levensvatbaarheid van L. lactis en E. cloacae. Schaalbalken = 100 µm. c Raman-spectra van volbloed verrijkt met E. cloacae (boven) voor en (onder) na verwerking door poreuze silicamonoliet. Krediet:microsystemen en nano-engineering, doi:10.1038/s41378-019-0063-4.
Voor bacteriële passage met hoge doorvoer, de wetenschappers verdunnen het bloed in de capillaire apparaten. Echter, als een alternatief, ze zouden ook de capaciteit van monolieten voor de lysis van volbloed kunnen vergroten. De apparaten verwerkten meer dan 400 µL volbloed verrijkt met bacteriën voordat ze een significante toename van de tegendruk vertoonden, door verstopping als gevolg van cellysis en ook door intacte leukocyten (WBC's) die in de poreuze matrix zijn opgesloten.
Om doelbacteriën te lokaliseren, Han et al. verkregen een monster afgezet op een glasplaatje, nadat het door het monoliet-proces is gegaan. Ze voerden eencellige Raman-analyse uit door de optische sonde handmatig over het monster te scannen. Ze verwachten het gebruik van selectieve lysistechnologie, gekoppeld aan confocale Raman-microscopie in de toekomst om het proces van het detecteren van bacteriële stammen van belang bij lage concentraties op een gedefinieerde locatie van belang te verbeteren.
Op deze manier, Jung Y. Han en collega's ontwikkelden een microfluïdische monoliet om intacte bacteriën efficiënt te isoleren met uitgebreide theranostische, point-of-care potentieel voor klinische toepassingen. Ze stellen zich de vereniging voor van confocale Raman-microscopiehulpmiddelen die momenteel grotendeels beperkt zijn tot het onderzoekslaboratorium met opkomende geminiaturiseerde en draagbare systemen om de weg vrij te maken voor snelle en draagbare point-of-care-apparaten.
© 2019 Wetenschap X Netwerk
 Röntgenlaseronderzoek identificeert kristallijn tussenproduct in onze weg naar ademen
Röntgenlaseronderzoek identificeert kristallijn tussenproduct in onze weg naar ademen Zeer efficiënte methode om polyisopreenrubber met ultrahoog molecuulgewicht te synthetiseren
Zeer efficiënte methode om polyisopreenrubber met ultrahoog molecuulgewicht te synthetiseren Onderzoeker ontwikkelt een nieuwe, darm-gezonde pindakaas
Onderzoeker ontwikkelt een nieuwe, darm-gezonde pindakaas Video:Waarom ruikt de maan naar buskruit?
Video:Waarom ruikt de maan naar buskruit? Geen laboratorium nodig:nieuwe technologie kan infecties binnen enkele minuten diagnosticeren
Geen laboratorium nodig:nieuwe technologie kan infecties binnen enkele minuten diagnosticeren
 Het aanbrengen van steenstof op akkerlanden kan tot 2 miljard ton CO2 uit de atmosfeer opnemen
Het aanbrengen van steenstof op akkerlanden kan tot 2 miljard ton CO2 uit de atmosfeer opnemen Klimaatverandering maakt herhaling Dust Bowl twee keer zo waarschijnlijk
Klimaatverandering maakt herhaling Dust Bowl twee keer zo waarschijnlijk We hebben vooruitgang geboekt om de wereldwijde uitstoot te beteugelen, maar het is een fractie van wat nodig is
We hebben vooruitgang geboekt om de wereldwijde uitstoot te beteugelen, maar het is een fractie van wat nodig is Sneeuw heeft mogelijk een aantal bloemen vertraagd voor de eerste dag van de lente
Sneeuw heeft mogelijk een aantal bloemen vertraagd voor de eerste dag van de lente Onderzoek onthult dat klimaatverandering kwetsbare berghabitats drastisch kan veranderen
Onderzoek onthult dat klimaatverandering kwetsbare berghabitats drastisch kan veranderen
Hoofdlijnen
- Verrassende ontdekking - hoe de Afrikaanse tseetseevlieg echt je bloed drinkt
- Onderzoeksartikelen werpen licht op een decennium lang stamcelmysterie
- Gaan roodharigen uitsterven?
- Hoe werken het ademhalings- en cardiovasculaire systeem samen?
- Uitbreiding van Braziliaans suikerriet kan de wereldwijde CO2-uitstoot verminderen
- Staan we op een kantelpunt met onkruidbestrijding?
- Wat zijn de rollen van chlorofyl A & B?
- Hoe een mRNA-sequentie
- Er is een genetische reden waarom Labrador Retrievers geobsedeerd zijn door voedsel
- Onderzoekstrio schetst manieren waarop nanodiamanten worden gebruikt om kanker te behandelen
- Onderzoekers ontdekken nieuwe route naar spin-gepolariseerde contacten op silicium

- In sediment levende wezens die gevaar lopen door nanodeeltjes in gewone huishoudelijke producten

- Filmen van de thermische dood van elektronen in materie

- Studie introduceert nieuwe vacuümkanaaltransistors op nanoschaal

 Waar worden mensen blij van?
Waar worden mensen blij van?  Inductiewet van Faradays: definitie, formule en voorbeelden
Inductiewet van Faradays: definitie, formule en voorbeelden  Zilveren nanodraden demonstreren onverwacht zelfgenezend mechanisme
Zilveren nanodraden demonstreren onverwacht zelfgenezend mechanisme Afbeelding:Partial Gravity Simulator oefenen
Afbeelding:Partial Gravity Simulator oefenen Businessgroepen die alleen voor vrouwen zijn, marginaliseren en slagen er niet in om leden mondiger te maken
Businessgroepen die alleen voor vrouwen zijn, marginaliseren en slagen er niet in om leden mondiger te maken Hoe maansverduisteringen werken
Hoe maansverduisteringen werken  Planten & dieren geboren in North Dakota
Planten & dieren geboren in North Dakota Astronomen observeren hoe twee zonnen materie verzamelen in een binair systeem
Astronomen observeren hoe twee zonnen materie verzamelen in een binair systeem
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

