
Wetenschap
Glazige koolstofmicronaalden:een nieuw apparaat voor transdermale toediening van medicijnen
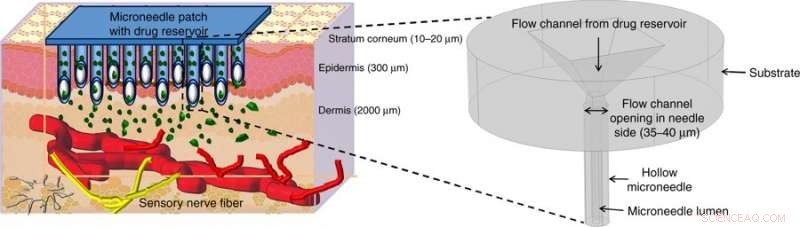
Geïllustreerde medicijnafgifte met behulp van holle micronaalden (MN's). Holle MN's doorboren de huid om boven de pijngevoelige zenuwen in het transdermale gebied van de huid te reiken en geven het medicijn pijnloos af via geschikte activeringsmethoden. De afbeelding aan het begin toont een vergroot beeld van de micronaaldstructuur die in dit werk wordt voorgesteld. Krediet:microsystemen en nano-engineering, doi:https://doi.org/10.1038/s41378-018-0039-9.
Micronaalden zijn ontworpen om medicijnen transdermaal (via de huid) en relatief pijnloos toe te dienen tijdens klinische toepassingen. In een recente studie, Richa Mishra en haar collega's ontwikkelden een nieuwe techniek om polymeerfilms om te zetten in een breukbestendige glasachtige vorm van koolstof om micronaalden te ontwikkelen. Het geoptimaliseerde transdermale medicijnafgifteapparaat werd gefabriceerd met behulp van fotolithografie om een biocompatibele en robuuste micronaald te vormen voor preklinische toepassingen.
De wetenschappers genereerden eerst een reeks verticale, holle buizen gemaakt van het epoxygebaseerde polymeer SU-8 op een siliciumsubstraat. De microstructuren werden geslepen tot naaldachtige vormen door warmtebehandeling in een zuurstofvrije oven en het eindproduct was volledig samengesteld uit willekeurig geordende koolstofatomen. Daaropvolgende materiaalkarakterisering omvatte nano-inspringing om de oppervlaktestijfheid te meten. De glasachtige koolstofstructuren waren robuust genoeg om de menselijke huid binnen te dringen zonder te breken. De resultaten van het onderzoek zijn gepubliceerd op: Microsystemen en nano-engineering .
De auteurs hebben het conventionele koolstof-micro-elektromechanische systeem (C-MEMS) -proces beschreven dat wordt gebruikt om de micronaalden te fabriceren. In het proces, Misra et al. gebruikte een schaalbare en onomkeerbare stap van pyrolyse, waar de voorloper van vooraf gevormde SU-8-micronaalden werden omgezet in glasachtige koolstofstructuren. De experimenten werden uitgevoerd in een inerte atmosfeer bij hoge temperaturen (~900 0 C) om hun oorspronkelijke vorm te behouden na het krimpen. Bij conversie naar glasachtige koolstof, de micronaalden erfden de bijbehorende eigenschappen van hardheid, biocompatibiliteit, thermische en chemische weerstand.
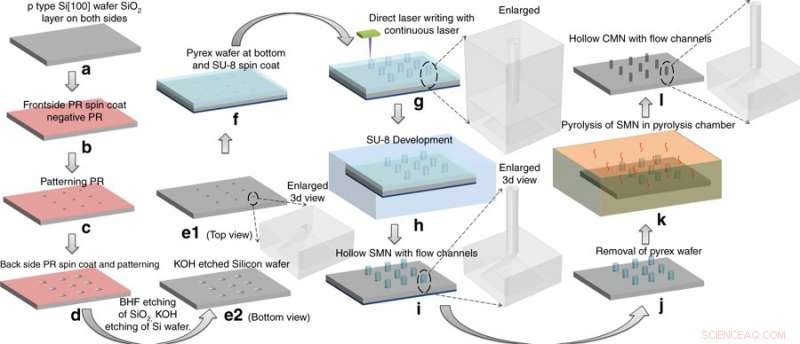
Fabricageproces:het omzetten van SU-8 micronaalden (SMN's) in holle glasachtige koolstofmicronaalden (CMN's) door pyrolyse. De SMN-structuren zijn gekrompen met behoud van hun algehele geometrie. Krediet:microsystemen en nano-engineering, doi:https://doi.org/10.1038/s41378-018-0039-9
De onderzoekers vergeleken de hardheid en Young's modulus van de koolstof- en SU-8-micronaalden om de verhoogde sterkte te begrijpen die wordt veroorzaakt door het C-MEMS-proces. Daarna werd het structurele krimpen van koolstofmicronaalden bij pyrolyse geschat. Misra et al. voerde diepgaande materiaalkarakterisering uit met energiedispersieve röntgenspectroscopie (EDX) om oppervlaktechemie en Raman-spectroscopie te begrijpen om het atomaire percentage koolstof in de kristallijne structuur van de micronaald te schatten.
De resultaten bevestigden de glasachtige samenstelling van de micronaalden. Aanvullende compressie- en buigtesten bepaalden de maximale krachten die de micronaalden konden weerstaan. De apparaten waren bestand tegen krachten die ongeveer twee orden van grootte hoger waren dan de weerstandskrachten van de huid. De apparaten werden vervolgens in het onderzoek getest op het huidoppervlak van een muismodel.
Het gebruik van koolstof in de geneeskunde is niet nieuw; voorbeelden zijn toepassingen in orthopedische gewrichten, als koolstofvezels/composieten in orthopedische operaties en als materialen in chirurgische instrumenten. De eigenschappen van koolstofvezels om 3D-steigerachtige structuren te vormen, hebben een veelbelovende capaciteit aangetoond bij de regeneratie van botweefsel. De op maat gemaakte eigenschappen van koolstof hebben ze geschikt gemaakt om transdermale medicijnafgifte micronaalden (MN) te fabriceren voor geavanceerde medicijn- en vaccinafgifte.
Voor competentie, MN's moeten een optimale lengte hebben voor effectieve medicijnafgifte, maar wees kort genoeg om pijn te voorkomen. Materiaalwetenschappers onderzoeken strategieën om klinisch levensvatbare materialen en methoden te selecteren die in korte tijd commercieel kunnen worden vertaald.
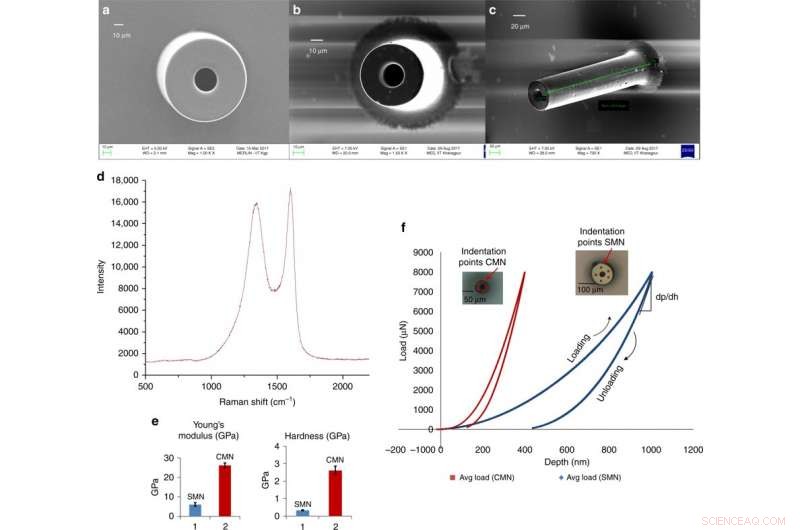
Glasachtige koolstofmicronaalden voor transdermale medicijnafgifte afgeleid van een schaalbaar C-MEMS-proces. a) Scanning-elektronenmicrofoto van een SMN (buitendiameter 100 m, binnendiameter 50 m). b) Overeenkomstig gepyrolyseerd MN. c) Gekantelde weergave van hetzelfde CMN. d) Raman-spectrum van de koolstofmicronaald. e) Vergelijking van Young's modulus en hardheid voor de SU-8 en koolstof MN's. f) Load vs. verplaatsingsgegevens voor een SMN en overeenkomstig gepyrolyseerd CMN. Krediet:microsystemen en nano-engineering, doi:https://doi.org/10.1038/s41378-018-0039-9.
De belangrijkste vereisten voor MN's zijn onder meer biocompatibiliteit, kracht en gecontroleerde medicijnafgifte. Vaste MN's kunnen worden ontwikkeld met polymeren, silicium, staal, titanium en nikkel via subtractieve of additieve processen. Een nadeel van solide MN's is hun beperkte capaciteit voor optimale medicijnafgifte. Anderzijds, holle MN's kunnen met externe druk aan een medicijnreservoir worden bevestigd voor optimale medicijnafgifte.
Misra et al. koos de voorloper SU-8 vanwege zijn hoge vernettingssterkte, biocompatibiliteit, goedkoop, door licht geïnduceerde polymerisatie en compatibiliteit met het micro-elektronische industrieproces. Hol te fabriceren, glasachtige koolstof micronaalden (CMN's), het C-MEMS-proces werd voor het eerst aangepast om SU-8 micronaalden (SMN's) te modelleren met behulp van direct laserschrijven, gevolgd door hun omzetting in glasachtige CMN's via pyrolyse. Microfluïdische poorten werden geëtst in een siliciumwafel, volgens een eerder protocol ontwikkeld door hetzelfde onderzoeksteam. De resulterende producten (CMN's) werden gekenmerkt door hun mechanische eigenschappen, inclusief hardheid en Young's modulus in vergelijking met hun voorloper SMN's. De resultaten gaven aan dat CMN's superieur waren.
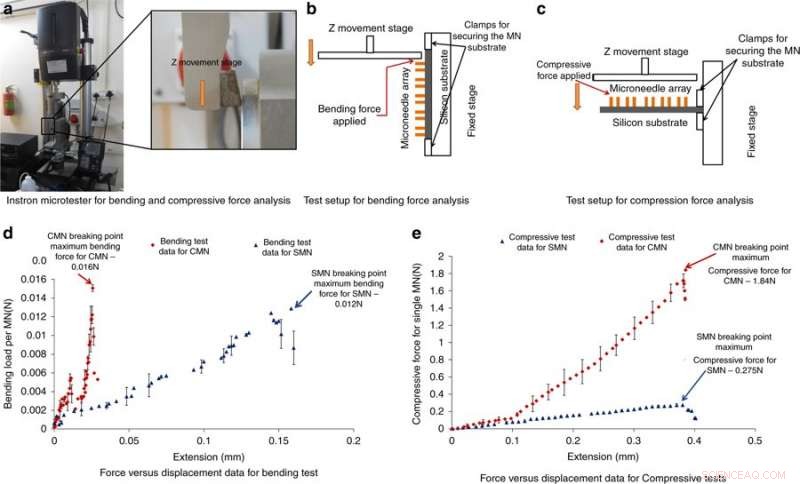
Instron microtester voor analyse en resultaten van buig- en drukkracht. a) Foto van de Instron-microtester die wordt gebruikt voor analyse van buig- en drukkracht. b) Testopstelling voor buigkrachtanalyse. c) Testopstelling voor compressiekrachtanalyse. d) Kracht versus verplaatsingsresultaten van de buigtest. e) Kracht versus verplaatsingsresultaten van de compressietest. Krediet:microsystemen en nano-engineering, doi:https://doi.org/10.1038/s41378-018-0039-9
Misra et al. observeerden en kwantificeerden de afmetingen van SMN-precursoren en bijbehorende gepyrolyseerde CMN-structuren met behulp van scanning-elektronenmicroscopie (SEM) -beelden. Na pyrolyse, de diameter en wanddikte van de micronaald namen af. De EDX-resultaten toonden een verhoogd atomair percentage koolstofelementen voor koolstof-MN's. De afwezigheid van stikstof in de samenstelling van de koolstofmicronaald duidde op de verwijdering ervan tijdens verhitting. Het percentage zuurstofgehalte was te wijten aan de CMN-structuur en de Si/SiO 2 ondergrond oppervlak. Raman-spectroscopie toonde de glasachtige kristallijne aard van de uiteindelijke microstructuur aan door middel van verificatie van het koolstofproduct. De resultaten kwamen overeen met eerdere onderzoeken.
De wetenschappers verkregen gegevens over de verplaatsing van de lading via nano-indentatie voor de afzonderlijke SU-8- en koolstofstructuren. Ze berekenden de hardheid en elasticiteitsmodulus met behulp van het Oliver Pharr-model. De resultaten toonden een hardheid van 0,33 GPa en Young's modulus van 5,52 GPa voor SMN. Bij conversie naar CMN via pyrolyse, de indrukresultaten toonden een hogere elasticiteit van het materiaal, de hardheid nam achtvoudig toe tot 2,62 GPa en de Young's modulus nam 4,8-voudig toe tot 26,97 GPa.
Om het vermogen van MN's te begrijpen om krachten te weerstaan zonder te breken tijdens het inbrengen in de huid, Misra et al. uitgevoerde buig- en drukkrachtmetingen van de constructie. Typisch, een MN ondervindt weerstand bij huidpenetratie, de uitgeoefende kracht moet daarom groter zijn dan de tegengestelde kracht. Om buiging/compressie te testen, de MN's werden in een Instron-microtester geladen en een metalen plaat werd naar de MN's gedreven totdat ze braken; als de uitgeoefende belasting lager was dan de maximale druk- of buigkracht, de naalden zullen niet breken. Een scherpe daling van de drukkracht of buigkracht duidde op een breukpunt. De resultaten toonden aan dat CMN's veel sterker waren dan de voorlopers, waardoor ze weerstand kunnen overwinnen tijdens huidpenetratie.
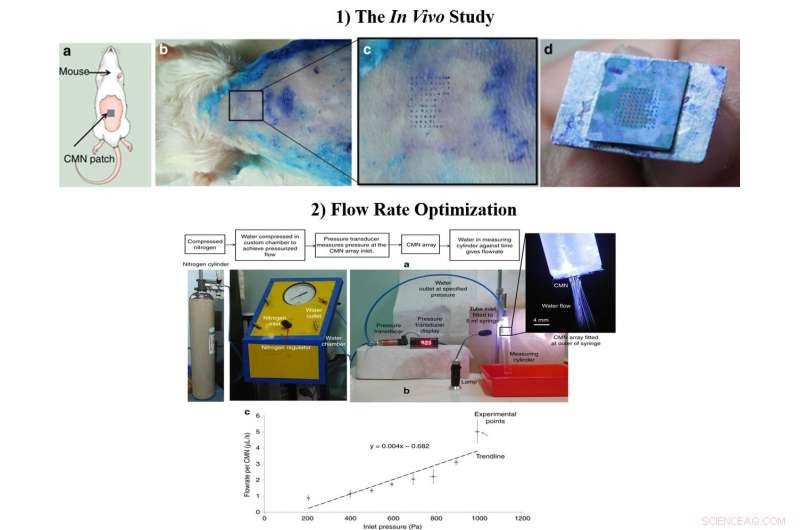
1) De in vivo studie a) Schema van de MN-insertietest op muizen. b) Biologische insertietest uitgevoerd op 6 tot 8 weken oude Zwitserse Albino-muizen. c) Vergrote weergave van het huidgebied doorboord door de CMN's. d) Intact array van 10 × 10 na meerdere inserties. 2) Het geoptimaliseerde debiet, a) Testopstelling voor debietmeting. b) Debiet per micronaald bij verschillende inlaatdrukken. Krediet:microsystemen en nano-engineering, doi:https://doi.org/10.1038/s41378-018-0039-9
Na bevestiging van het mechanische karakter en de superioriteit van holle CMN's in het laboratorium, Richa Mishra en collega's voerden in vivo experimenten uit om de CMN's op muizenhuid te testen. Een micronaaldreeks die vers in methyleenblauw was gedompeld, werd op de huid van een Zwitsers Albino-muismodel gedrukt en meerdere keren langzaam teruggetrokken. De naaldsporen van methyleenblauw waren zichtbaar, de MN's bleven intact na meerdere inserties en een array-afstand van 500 µm was optimaal voor verdere studies in het laboratorium.
De wetenschappers optimaliseerden de stroomafmetingen tijdens het fabricageproces en voegden microfluïdische leidingen met kleinere afmetingen toe voor verbeterde MN-functionaliteit. Om de stroomsnelheden te testen, ze bevestigden een injectiespuit van 5 ml met een aangepaste kamer met gedeïoniseerd water. Toen de wetenschappers de gemiddelde stroomsnelheid versus druk voor individuele MN's maten, de resultaten toonden aan dat de medicijnafgifte uiteindelijk kon worden gecontroleerd door de inlaatdruk te wijzigen.
De definitieve materiaalkarakteriseringstechniek in het onderzoek was nano-indentatie, omdat de parameter oppervlaktehardheid en Young's modulus kwantificeerde om de superioriteit van CMN's te verifiëren. Toekomstig werk omvat de ontwikkeling van gecontroleerde medicijnafgifte, met een micropomp en een medicijnreservoir geïntegreerd in het MN-ontwerp. Op deze manier, de wetenschappers streven naar het ontwikkelen van geavanceerde toedieningssystemen voor geneesmiddelen en vaccins in de gezondheidszorg die kostenefficiënt zijn, nauwkeurig en pijnloos voor de patiënt.
© 2019 Wetenschap X Netwerk
 Zeer lichtgevende inkten gemaakt van koper-jodium hybride clusters met aggregatie-geïnduceerde emissie
Zeer lichtgevende inkten gemaakt van koper-jodium hybride clusters met aggregatie-geïnduceerde emissie Draagbare biosensor waarschuwt voor hartaanval en beroerte
Draagbare biosensor waarschuwt voor hartaanval en beroerte Hoe Amp om te zetten in elektronen per seconde
Hoe Amp om te zetten in elektronen per seconde  Chemische lusverbranding voor CO2-neutrale gasinstallaties
Chemische lusverbranding voor CO2-neutrale gasinstallaties RNA-basisbouwsteen voor het eerst biokatalytisch geproduceerd
RNA-basisbouwsteen voor het eerst biokatalytisch geproduceerd
Hoofdlijnen
- Hands-on Science Activiteiten op Blood
- Lijst van de toepassingen van elektroforese
- Een 3D-poster maken van de celcyclus
- Wat is één reden waarom de classificatie van protisten in één koninkrijk moeilijk is?
- Hoeveel spieren heb je nodig om te glimlachen?
- 10 onderzoeken die compleet bizarre dingen met elkaar verbinden
- Wat is een virus,
- Licht schijnen op het sociale leven van virussen
- Wat is de structuur van stamcellen?
- Studie onthult nieuw mechanisme voor celcommunicatie over lange afstand
- Zuurstof-bevorderde synthese van grafeen nanoribbons op Cu (111)

- Onderzoek toont aan dat een veel goedkopere katalysator waterstof kan genereren in een commercieel apparaat

- Eendimensionaal materiaal is krachtig voor de volgende generatie elektronica

- Wetenschappers ontdekken dat mechanisch gedrag van kleine structuren wordt beïnvloed door atoomdefecten

 Nieuw, gevoeliger sensor voor het evalueren van de veiligheid van geneesmiddelen
Nieuw, gevoeliger sensor voor het evalueren van de veiligheid van geneesmiddelen Lyft en Uber worden dagelijkse ritten met passen
Lyft en Uber worden dagelijkse ritten met passen Snelheid van magnetische domeinmuren bleek fundamenteel beperkt te zijn
Snelheid van magnetische domeinmuren bleek fundamenteel beperkt te zijn Wat is het verschil tussen hagedissen en gekko's?
Wat is het verschil tussen hagedissen en gekko's?  Voor meisjes, buiten wetenschap leren gekoppeld aan betere cijfers, kennis
Voor meisjes, buiten wetenschap leren gekoppeld aan betere cijfers, kennis Kunstmatige selectie (selectieve fokkerij): definitie & voorbeelden
Kunstmatige selectie (selectieve fokkerij): definitie & voorbeelden Wauw! mysteriesignaal uit de ruimte eindelijk uitgelegd
Wauw! mysteriesignaal uit de ruimte eindelijk uitgelegd Welke bijdragen heeft J.J. Thomson Make to the Atom?
Welke bijdragen heeft J.J. Thomson Make to the Atom?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

