
Wetenschap
Rode gloed helpt bij het identificeren van nanodeeltjes voor het leveren van RNA-therapieën
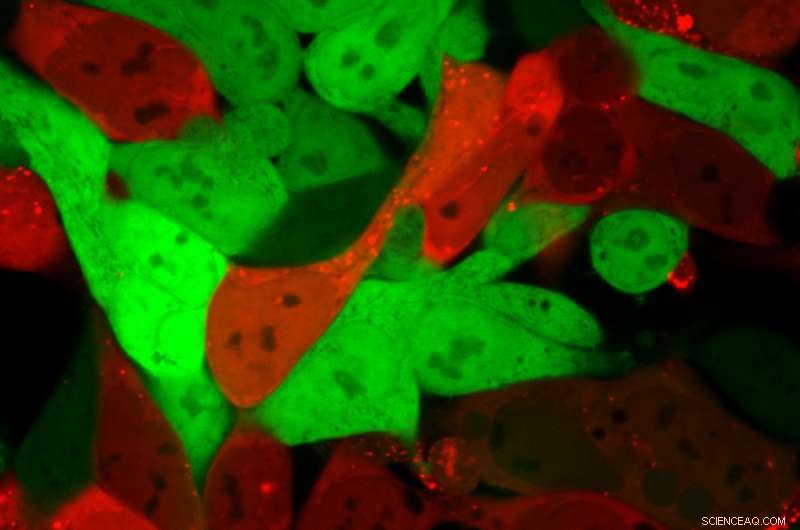
Cellen die normaal heldergroen zijn, worden helderrood nadat lipide-nanodeeltjes een mRNA-lading hebben afgeleverd die codeert voor Cre. Rode cellen bevatten het mRNA, terwijl groene cellen dat niet doen. Krediet:Daryll Vanover, Georgië Tech
Een nieuw screeningproces zou de identificatie van nanodeeltjes die geschikt zijn voor het afleveren van therapeutisch RNA in levende cellen drastisch kunnen versnellen. De techniek zou onderzoekers in staat stellen om honderden nanodeeltjes tegelijk te screenen, het identificeren van de organen waarin ze zich ophopen - en verifiëren dat ze met succes een RNA-lading in levende cellen kunnen afleveren.
Gebaseerd op werk dat bekend staat als "DNA-barcoding, " de techniek voegt unieke DNA-fragmenten in maar liefst 150 verschillende nanodeeltjes in voor gelijktijdige testen. De nanodeeltjes worden vervolgens in diermodellen geïnjecteerd en mogen naar organen zoals de lever reizen, milt of longen. Genetische sequencing-technieken identificeren vervolgens welke DNA-gelabelde nanodeeltjes specifieke organen hebben bereikt.
In een paper gepubliceerd op 1 oktober in het tijdschrift Proceedings van de National Academy of Sciences , een onderzoeksteam beschrijft dat het proces een stap verder gaat om te verifiëren dat de nanodeeltjes de cellen van de specifieke organen zijn binnengekomen. Naast de DNA-barcode, de onderzoekers plaatsten in elk nanodeeltje een stukje mRNA dat wordt omgezet in een eiwit dat bekend staat als 'Cre'. Het Cre-eiwit genereert een rode gloed, het identificeren van cellen die de nanodeeltjes zijn binnengekomen en met succes het mRNA-medicijn hebben afgeleverd, waardoor de onderzoekers kunnen identificeren welke nanodeeltjes RNA-medicijnen kunnen afleveren aan de cellen van de specifieke organen.
"Deze techniek, bekend als Fast Indication of Nanoparticle Discovery (FIND), ons in staat zal stellen de juiste vervoerder veel sneller en goedkoper te identificeren dan we in het verleden hebben kunnen doen, " zei James E. Dahlman, assistent-professor aan de Wallace H. Coulter Department of Biomedical Engineering aan Georgia Tech en Emory University. "Als resultaat, de kans dat we dragers voor specifieke weefsels kunnen vinden, zou drastisch moeten toenemen."
De FIND-techniek zou in vitro screening vervangen, die beperkt succes heeft bij het identificeren van nanodeeltjesdragers voor de genetische therapieën. Het onderzoek werd ondersteund door financiering van de National Institutes of Health, en van de Cystic Fibrosis Research Foundation, de Parkinson's Disease Foundation en het Bayer Hemofilie Awards-programma.

James Dahlman, een assistent-professor in de Wallace H. Coulter Department of Biomedical Engineering aan Georgia Tech en Emory University, bevat een microfluïdische chip die wordt gebruikt om nanodeeltjes te fabriceren die kunnen worden gebruikt om therapeutische genen af te leveren. Krediet:Rob Vilt, Georgië Tech
Therapieën op basis van RNA en DNA kunnen een breed scala aan genetisch gebaseerde ziekten aanpakken, inclusief atherosclerose, waar dergelijke therapieën de opbouw van plaque in slagaders kunnen omkeren. Nanodeeltjes die worden gebruikt om RNA en DNA in cellen af te leveren, zijn gemaakt van verschillende ingrediënten waarvan de niveaus kunnen worden gevarieerd, waardoor het potentieel voor tienduizenden verschillende nanodeeltjes ontstaat. Het vinden van de juiste combinatie van deze ingrediënten om zich op specifieke cellen te richten, vereiste uitgebreide trial-and-error-ontdekkingsprocessen die het gebruik van RNA- en DNA-therapieën hebben beperkt.
Door gebruik te maken van het DNA-barcoderingsproces kunnen honderden mogelijke combinaties van nanodeeltjes tegelijkertijd worden getest in een enkel dier, maar tot nu toe, onderzoekers konden alleen vertellen dat de combinatie specifieke organen had bereikt. Door te onderzoeken welke cellen in de organen de rode gloed hebben, ze kunnen nu verifiëren dat de nanodeeltjes de streepjescodes droegen en functionele mRNA-medicijnen in de cellen afleverden.
In de krant, de onderzoekers melden dat ze twee nanodeeltjes hebben ontdekt die efficiënt siRNA afleveren, sgRNA en mRNA naar endotheelcellen in de milt. De onderzoekers geloven dat hun techniek therapeutisch RNA en DNA kan leveren aan een breed scala aan endotheelceltypes, en misschien ook voor het immuunsysteem en andere celtypen.
"Het veld is in staat geweest om functionele genetische medicijnen aan de lever te leveren, en we proberen nu onze technologie te gebruiken om aan verschillende organen en celtypes te leveren om therapieën mogelijk te maken om alle celtypes in de lever te behandelen, " zei Cory Sago, de eerste auteur van het papier en een Ph.D. kandidaat in Dahlmans lab. "Nu we een systeem hebben waarmee we deze vragen op een heel specifiek oplossingsniveau kunnen onderzoeken, we willen nu op een efficiëntere manier andere celtypes aanpakken."
Dahlman verwacht de nieuwe technologie snel in gebruik te kunnen nemen.

James Dahlman, een assistent-professor in de Wallace H. Coulter Department of Biomedical Engineering aan Georgia Tech en Emory University, wordt getoond in zijn laboratorium. Krediet:Christopher Moore, Georgië Tech
"We hopen projecten op te pakken die normaal jaren nodig zouden hebben en een aantal ervan binnen de komende 12 maanden af te ronden, " zei hij. "FIND zou kunnen worden gebruikt om allerlei nucleïnezuurgeneesmiddelen in cellen te vervoeren. Dat kunnen kleine RNA's zijn, grote RNA's, kleine DNA's en grote DNA's - veel verschillende soorten genetische medicijnen die nu worden ontwikkeld in onderzoekslaboratoria."
Technische uitdagingen die voor ons liggen, zijn onder meer aantonen dat het identificeren van een affiniteit voor muisorganen voorspelt welke deeltjes in het menselijk lichaam zullen werken, en dat de aanpak werkt voor verschillende klassen van genetische therapieën.
Experimenteel, Het laboratorium van Dahlman produceert de nanodeeltjes in drie formuleringsstations die ongeveer 90 seconden nodig hebben om elk van de ongeveer 250 gebruikte monsters te produceren. De resulterende nanodeeltjes worden vervolgens onderzocht op het juiste groottebereik - 40 tot 80 nanometer in diameter - voordat ze worden gezuiverd en gesteriliseerd voor injectie in de dieren.
Na drie dagen, de onderzoekers scheiden cellen die gloeiend rood zijn en rangschikken de DNA-fragmenten erin om te identificeren welke chemische samenstellingen het meest succesvol waren in het binnendringen van cellen van specifieke organen. De meest veelbelovende chemische samenstellingen worden gebruikt om een nieuwe batch kandidaat-nanodeeltjes te ontwikkelen voor een nieuwe screeningronde, die ongeveer een week in beslag neemt.
"We willen de beste deeltjes ontwikkelen die we kunnen, " zei Sago. "Elk van de componenten is belangrijk, en we werken eraan om elk onderdeel goed te krijgen voor het celtype waarin we geïnteresseerd zijn. Er is veel optimalisatie vereist."
 Linkse of rechtse moleculen helpen materiële structuren
Linkse of rechtse moleculen helpen materiële structuren Hoe zout water om te zetten in zoet water (drinkwater)
Hoe zout water om te zetten in zoet water (drinkwater)  Het overwinnen van de uitdagingen bij gecontroleerde thermische depositie van organische diradicalen
Het overwinnen van de uitdagingen bij gecontroleerde thermische depositie van organische diradicalen Nieuwe manier om RNA te zien kan ziekteverwekkers helpen bestrijden
Nieuwe manier om RNA te zien kan ziekteverwekkers helpen bestrijden Hoe watertestresultaten te lezen
Hoe watertestresultaten te lezen
 Ongewone sneeuw doodt 4, brengt een groot deel van Spanje tot stilstand
Ongewone sneeuw doodt 4, brengt een groot deel van Spanje tot stilstand Een Science Fair-project over geurbeïnvloeding Taste
Een Science Fair-project over geurbeïnvloeding Taste Milieustudies ondersteunen Trumps schoonste bewering niet
Milieustudies ondersteunen Trumps schoonste bewering niet Monstercycloon treft door COVID geteisterde westkust van India
Monstercycloon treft door COVID geteisterde westkust van India Tropische bomen gebruiken unieke methode om droogte te weerstaan
Tropische bomen gebruiken unieke methode om droogte te weerstaan
Hoofdlijnen
- De vergeten wetenschapper die de weg vrijmaakte voor de ontdekking van de DNA-structuur
- Waarom mensen schreeuwen,
- Welke soorten moleculen katalyseren RNA-splitsing?
- Energiestroom (ecosysteem): definitie, proces en voorbeelden (met diagram)
- Het belang van asymmetrie bij bacteriën
- De rol van Taq-polymerase in PCR
- Welke soorten moleculen kunnen door het plasmamembraan passeren via eenvoudige diffusie?
- Foster-kikkervisjes triggeren het ouderlijk instinct bij gifkikkers
- Wat is een voorbeeld in een levend systeem van hoe moleculair van vorm is?
- Wanorde kan batterijen stabiliseren

- Onderzoekers rapporteren energiezuinige schakelapparatuur op nanoschaal

- Onverwacht water verklaart de oppervlaktechemie van nanokristallen

- Nieuwe zonneceltechnologie legt hoogenergetische fotonen efficiënter vast

- DNA-origami gebruiken om nano-apparaten van de toekomst te bouwen
 Hoe wordt actieve kool in poedervorm gebruikt?
Hoe wordt actieve kool in poedervorm gebruikt?  Ozongeneratoren kunnen helpen bij het oplossen van verontreiniging veroorzaakt door rook uit derdehands
Ozongeneratoren kunnen helpen bij het oplossen van verontreiniging veroorzaakt door rook uit derdehands Grote wetenschappelijke doorbraak op subatomair niveau belooft veilige communicatie
Grote wetenschappelijke doorbraak op subatomair niveau belooft veilige communicatie Heeft Catfish Lay Eggs?
Heeft Catfish Lay Eggs?  Sleutelhangerdetector kan voedselallergenen opvangen voordat het te laat is
Sleutelhangerdetector kan voedselallergenen opvangen voordat het te laat is Met ultrakoude chemie, onderzoekers krijgen een eerste blik op wat er precies gebeurt tijdens een chemische reactie
Met ultrakoude chemie, onderzoekers krijgen een eerste blik op wat er precies gebeurt tijdens een chemische reactie 2D-materialen stimuleren de vermenigvuldiging van dragers
2D-materialen stimuleren de vermenigvuldiging van dragers Weer aan het werk gaan is net zo belangrijk als loskomen van het werk, studie vondsten
Weer aan het werk gaan is net zo belangrijk als loskomen van het werk, studie vondsten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

