
Wetenschap
Autonome genexpressiecontrole nanodevice zal bijdragen aan medische zorg
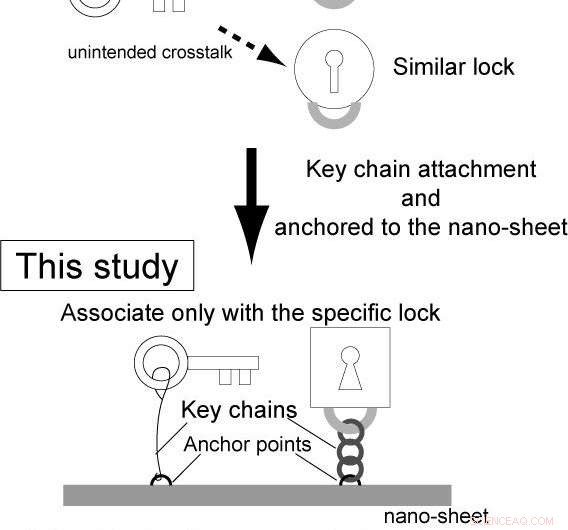
Fig. 1 Effect van integratiebenadering. Krediet:Hisasi Tadakuma / Universiteit van Osaka
Genexpressie is een fundamenteel van het leven, waarbij elke cel specifieke genen in- en uitschakelt. Dus, een autonoom apparaat dat de aan-uitschakeling zou kunnen regelen, zou van grote waarde zijn in de medische zorg.
Synthetische genetische circuits zijn een technologie om genexpressie te controleren en cellen te programmeren om gewenste functies uit te voeren. Daarom, door de complexiteit van het genetische circuit te vergroten, kunnen we het lot van de cellen nauwkeuriger controleren.
Echter, de complexiteit van genetische circuits blijft laag. Dit is zo omdat, in conventionele reactie-diffusiesystemen, de enzymen en substraten worden apart geleverd, en niet-specifieke binding van de enzymen aan de substraten veroorzaakt onbedoelde overspraak tussen de verschillende circuits.
Door de Universiteit van Osaka geleide onderzoekers, in een gezamenlijk onderzoeksproject met de Universiteit van Tokyo, Universiteit van Kyoto, en Waseda-universiteit, geconstrueerde geïntegreerde genlogica-chips genaamd "gen-nanochips". Met behulp van geïntegreerde factoren op de nanochips, deze op zichzelf staande nanochips kunnen genen aan- en uitzetten binnen een enkele chip, om onbedoelde overspraak te voorkomen.
De onderzoekers toonden de autonome reacties van de nanochips in kunstmatige cellen:omgevingsdetectie, informatieberekening en productuitvoer op het niveau van één chip. Hun onderzoeksresultaten zijn gepubliceerd in Natuur Nanotechnologie .
DNA-nanotechnologie is een veelzijdige methode die wordt gebruikt om aangepaste structuren te construeren en nauwkeurige moleculaire lay-outs te controleren. De onderzoekers gebruikten een rechthoekig vel (90 nm breed, 60 nm diep, 2 nm hoog), en geïntegreerd enzym, RNA-polymerase (RNAP, een enzym dat RNA synthetiseert uit een DNA-template), en meerdere doelwitgensubstraten.
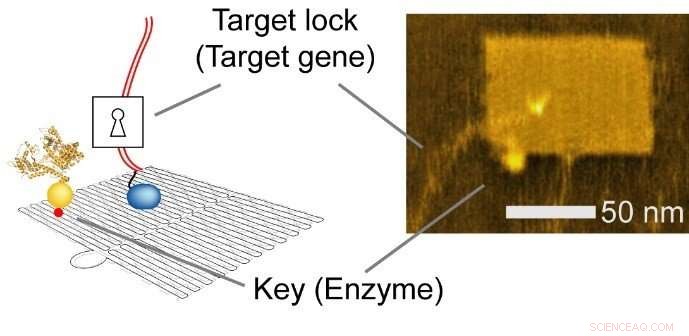
Fig. 2 Geïntegreerde nanochip. Links, Schematische voorstelling. Rechts, atoomkrachtmicroscopie (AFM) afbeelding. Krediet:Hisashi Tadakuma / Universiteit van Osaka
Het nano-layoutvermogen van DNA-nanotechnologie stelt de onderzoeker in staat om genexpressieniveaus rationeel te ontwerpen door de intermoleculaire afstanden tussen het enzym en de doelgenen te veranderen, waardoor de botsingsefficiëntie en de daaropvolgende reactie worden beïnvloed.
De onderzoekers integreerden verder sensoren. Ideaal, een sensor die elk type signaal kan detecteren, moet minimale ontwerpbeperkingen hebben. Echter, conventionele methoden hebben te lijden gehad van verschillende beperkingen (bijv. materialen). Dit is zo omdat, in conventionele genetische circuits, de sensor maakt deel uit van het substraat van het enzym (bijv. DNA in transcriptie; zie opmerking voor details).
Omgekeerd, in dit onderzoek, het sensorgedeelte was onafhankelijk van de enzymatische reactie. Dus, de onderzoekers kunnen elk sensormateriaal gebruiken dat de effectieve intermoleculaire afstand bij signaalherkenning verandert, waardoor de constructie van verschillende sensoren die reageren op verschillende signalen (microRNA's, chemische bestanddelen, eiwitten en licht). Bovendien, door het combineren en integreren van sensoren die reageren op verschillende signalen, de onderzoekers zijn erin geslaagd de genetische circuits met foto's te herprogrammeren.
Eindelijk, de nanochip stelde de onderzoekers in staat om de constructie van een genetisch circuit te vereenvoudigen dat reageerde op een kunstmatige cel, een water-in-olie druppel, en ze konden het miRNA-profiel berekenen, door simpelweg de orthogonale chips te mengen, uitbreiding van de kracht van het genetische circuit.
Corresponderende auteur Hisashi Tadakuma zegt:"Alle factoren die nodig zijn voor transcriptiereacties bevinden zich op deze geïntegreerde nanochip, dus omgevingsgevoel, informatieberekening, en productuitvoer kan worden voltooid op het niveau van één chip. In de nabije toekomst, autonome nanochips zullen nuttig zijn om de cel gezond te houden door de genexpressie ruimtelijk en tijdelijk te beheersen, die het ideaal van het gezegde 'voorkomen is de beste remedie' zal belichamen. "
Ideaal, een sensor die elk type signaal kan detecteren, moet minimale ontwerpbeperkingen hebben. Echter, conventionele methoden hebben te lijden gehad van verschillende beperkingen (bijv. materialen). Dit is zo omdat, in conventionele genetische circuits, de efficiëntie van binding tussen een enzym zoals RNAP (sleutel) en een doelgen (doelslot), specifiek een promotorsequentie op het DNA-molecuul, wordt gecontroleerd door transcriptiefactoren (regulatoren). Omdat regulatoren en enzymen zich moeten binden aan de sensor (operatorgebied) in de buurt van het doelslot, het materiaal van de sensor moet een substraat zijn van de regulatoren en enzymen (bijv. DNA in transcriptie), en de regulator zou een DNA-bindend eiwit moeten zijn. Dus, zowel de regelaar (signaal) als sensor hebben materiële beperkingen.
Echter, in dit onderzoek, de bindingsfrequentie en de daaropvolgende reactie worden gecontroleerd door (1) de intermoleculaire afstand tussen een enzym en een doelgen, en (2) de kenmerken van de sleutelhanger (bijv. stijfheid, lengte). Het sensorgedeelte is dus onafhankelijk van de enzymatische reactie, en de sensor en regelaars hebben geen materiële beperkingen, waardoor de verschillende sensoren kunnen reageren op verschillende signalen (chemische verbindingen, eiwitten en licht).
Hoofdlijnen
- What Is Crossing Over in Genetics?
- Nieuwe gen-editor gebruikt om ziekte in embryo's op te lossen:studie
- Verschil tussen triglyceriden en fosfolipiden
- De voordelen van Anaerobe Ademhaling
- Wat doet zich voor als de Zygote één minder chromosoom heeft dan het gebruikelijke?
- Een 3D-poster maken van de celcyclus
- Wilgenroosje:de roze pionier
- Indonesische smokkelaars stopten exotische vogels in pijpen:politie
- Waarom zijn sommige dieren moeilijker te klonen dan andere?
- Ingenieurs ontwikkelen tot nu toe het zwartste zwarte materiaal

- Optische technieken onderzoeken giftige stoffen in cellen

- Onderzoekers creëren synthetische nanoporiën gemaakt van DNA

- Atoomstralen creëert nieuwe apparaten om nanodeeltjes te meten
- Productie van complexe 3D-metalen structuren op nanoschaal mogelijk gemaakt

 Defecten zijn perfect in lasergeïnduceerd grafeen
Defecten zijn perfect in lasergeïnduceerd grafeen Geluid van elektromagnetische energie die beweegt tussen Saturnus, Enceladus
Geluid van elektromagnetische energie die beweegt tussen Saturnus, Enceladus Koraalriffen hebben problemen - hoe kunnen mensen zich aanpassen?
Koraalriffen hebben problemen - hoe kunnen mensen zich aanpassen? Hoe oplossingen met verzadigd zoutwater voor te bereiden
Hoe oplossingen met verzadigd zoutwater voor te bereiden  Opportunity bereikt de afgrond van de volhardingvallei
Opportunity bereikt de afgrond van de volhardingvallei Nieuwe wetenschap achter biologisch afbreekbare teenslippers op basis van algen
Nieuwe wetenschap achter biologisch afbreekbare teenslippers op basis van algen Tektonische platen begonnen eerder te verschuiven dan eerder werd gedacht
Tektonische platen begonnen eerder te verschuiven dan eerder werd gedacht S&P waarschuwt dat 1 op de 10 Amerikaanse bedrijven mogelijk in gebreke blijft bij het aflossen van schulden
S&P waarschuwt dat 1 op de 10 Amerikaanse bedrijven mogelijk in gebreke blijft bij het aflossen van schulden
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


