
Wetenschap
Een biologische benadering van precisiegeneeskunde richt zich op een oneindig aantal ziekten

Krediet:Universiteit van Tel Aviv
De biologische complexiteit van kanker en andere ziekten vereist een formidabeler arsenaal aan therapieën dan momenteel beschikbaar is. De meeste therapeutische benaderingen negeren het dynamische moleculaire netwerk van genen, zich in plaats daarvan richten op slechts zeer weinig geselecteerde ziektegerelateerde genen.
Een nieuwe studie van de Universiteit van Tel Aviv gepubliceerd in Natuur Nanotechnologie stelt een nieuwe benadering voor om genen te manipuleren met behulp van een zelfassemblerend platform dat nucleïnezuren levert, zoals kleine interfererende RNA's (siRNA's), naar verschillende celsubsets. Terwijl de huidige praktijken van precisiegeneeskunde gericht zijn op een enkele cellulaire receptor, het nieuwe modulaire platform biedt een robuuste biologische benadering en kan de sleutel zijn tot de toekomst van gepersonaliseerde geneeskunde.
"De op siRNA-bezorging gerichte dragers die tegenwoordig worden gebouwd, richten zich op specifieke cellen en vereisen chemische conjugatie van het doelmiddel, " zegt Prof. Dan Peer van het Laboratorium voor Precisie Nanogeneeskunde aan de TAU's School of Molecular Cell Biology and Biotechnology, die het onderzoek leidde. "Het nieuwe platform is gebaseerd op biologische affiniteit, een zelf-assemblerende aanpak die kan worden vertaald om een eindeloos aantal ziekten en aandoeningen aan te pakken."
Onderzoek voor de studie werd uitgevoerd door de eerste co-auteurs Dr. Ranit Kedmi en Nuphar Veiga en collega's van Prof. Peer's TAU Laboratory, in samenwerking met Prof. Itai Benhar van TAU's School of Molecular Cell Biology and Biotechnology, Dr. Michael Harlev van het veterinaire servicecentrum van TAU, Dr. Mark Belkhe van Integrated DNA Technologies (IDT) en prof. Judy Lieberman van Boston Chidren's Hospital en Harvard Medical School.
De "linker" lokaliseren
Volgens prof. Peer, het nieuwe platform "verwijdert veel van de hindernissen" die de precisiegeneeskunde vandaag de dag teisteren. Het hart van het bezorgplatform is de "linker, " een lipoproteïne dat bindt aan het constante gebied van het antilichaam. Aangezien alle antilichamen van dezelfde familie een gemeenschappelijk gebied delen, een eenvoudige wijziging van het antilichaam resulteert in een nieuwe afgiftedrager die zich aanpast aan de doelreceptor van keuze.
"Omdat de constructie ervan afhankelijk is van affiniteitsinteracties, het is niet nodig om chemische conjugatie-optimalisaties te introduceren om de methode te laten functioneren, ", zegt prof. Peer. "Linkers zitten vast in het membraan van nanodeeltjes en binden aan een vast gebied van elk antilichaam van hetzelfde isotype. Dit biedt een veilige doorgang naar een theoretisch onbeperkte selectie van dragers die zich richten op verschillende celoppervlakreceptoren."
"Wij geloven dat dit modulaire leveringsplatform een mijlpaal is die precisiegeneeskunde echt haalbaar maakt, " zegt mevrouw Veiga. "De uitdaging was hoe bepaalde therapieën te sturen die zijn ontworpen om genen van belang in specifieke cellen te manipuleren zonder een specifieke medicijndrager voor elk specifiek celtype te ontwikkelen. Het zou erg duur en onpraktisch zijn om miljoenen verschillende medicijnen te ontwikkelen om elk specifiek celtype en specifiek gen te behandelen. Liever, de nadruk zou moeten liggen op het ontwikkelen van een op nucleïnezuur gebaseerd hulpmiddel om genexpressie te manipuleren door middel van een eenvoudige, constante uitwisseling."
Snelle resultaten
Voor het onderzoek, de wetenschappers gebruikten het platform om colonmacrofagen te targeten om ontstekingssymptomen veroorzaakt door inflammatoire darmziekte (IBD) in muismodellen te verminderen. "Met deze gerichte dragers kan men gemakkelijk snelle resultaten behalen, " zegt prof. Peer. "De muizen vertoonden veel minder ontstekingen, wat de mogelijkheid suggereert om nieuwe IBD-therapeutische kansen te beloven."
De onderzoekers beïnvloedden ook muismodellen met mantelcellymfoom, het nieuwe platform gebruiken om kankercellen te targeten, celdood induceren en de algehele overleving drastisch verbeteren.
"Ons onderzoek ondersteunt de ontwikkeling van gerichte nucleïnezuurafgifteplatforms voor therapieën voor auto-immuunziekten en kanker, " zegt Prof. Peer. "Ons leveringsplatform kan voor elke patiënt worden aangepast om een potentieel eindeloos aantal receptoren te targeten.
"Het is flexibel genoeg om gemakkelijk aan te passen aan elke celsubset en om elk gen naar keuze neer te halen. We denken dat het een enorm onderzoeks- en therapeutisch potentieel heeft."
De onderzoekers zijn momenteel geïnteresseerd in het bevorderen van een proof-of-concept bij mensen.
 Continue en stabiele laserwerking dankzij goedkope perovskieten bij kamertemperatuur
Continue en stabiele laserwerking dankzij goedkope perovskieten bij kamertemperatuur Holografische bundelvorming om metallic 3D-printen een boost te geven
Holografische bundelvorming om metallic 3D-printen een boost te geven Wat zijn de specificaties en kwaliteiten voor stikstofzuiverheid?
Wat zijn de specificaties en kwaliteiten voor stikstofzuiverheid?  Video:Waarom dumpen we kunstmest op bosbranden?
Video:Waarom dumpen we kunstmest op bosbranden? Nieuwe studie verklaart Mycobacterium tuberculosis hoge weerstand tegen medicijnen en immuniteit
Nieuwe studie verklaart Mycobacterium tuberculosis hoge weerstand tegen medicijnen en immuniteit
 Monsterstorm in de Stille Oceaan vernietigt toeristische resorts in Tonga
Monsterstorm in de Stille Oceaan vernietigt toeristische resorts in Tonga Landbouwplukkers in VS zien onveilig hete werkdagen verdubbelen in 2050
Landbouwplukkers in VS zien onveilig hete werkdagen verdubbelen in 2050 Bezos Earth Fund geeft bijna $ 800 miljoen aan klimaatgroepen in eerste subsidieronde
Bezos Earth Fund geeft bijna $ 800 miljoen aan klimaatgroepen in eerste subsidieronde Hoe te identificeren van wilde paddestoelen in North Carolina
Hoe te identificeren van wilde paddestoelen in North Carolina Wat zijn de vier speciale breedtegraden?
Wat zijn de vier speciale breedtegraden?
Hoofdlijnen
- Genen dicteren niet altijd dat jongens jongens zullen zijn
- Honderden dode zeeschildpadden gevonden drijvend voor El Salvador
- Onderzoeksthema's in de biotechnologie
- Wat gebeurt er als er geen zuurstof beschikbaar is aan het einde van de langzame glycolyse?
- Van Alaska tot Amazonia:de eerste wereldwijde kaarten met eigenschappen die de groei van vegetatie stimuleren
- De betekenis van Penta E
- De juiste manier om DNA te repareren
- Wat zijn de structurele delen van de lange botten in het lichaam?
- Kunstmatige neurale netwerken kunnen het beheer van natuurhistorische collecties stimuleren
- Onderzoekers creëren zeer geleidende en elastische geleiders met behulp van zilveren nanodraden

- DNA-nanoschakelaars onthullen hoe levensmoleculen met elkaar in verbinding staan
- Thioketal nanodeeltjes:onderzoekers ontwikkelen oraal toedieningssysteem om inflammatoire darmziekten te behandelen
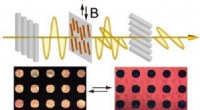
- Vloeibare kristallen gecontroleerd door magnetische velden kunnen leiden tot nieuwe optische toepassingen
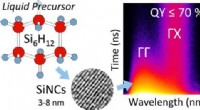
- Onderzoekers synthetiseren op silicium gebaseerde kwantumstippen
 Gratis routebeschrijving voor het maken van een barometer
Gratis routebeschrijving voor het maken van een barometer Afbeelding:De Columbus-module
Afbeelding:De Columbus-module Een close-up van een ongewone onderwateruitbarsting
Een close-up van een ongewone onderwateruitbarsting Waarom ontwikkelen weerballonnen zich op grote hoogte?
Waarom ontwikkelen weerballonnen zich op grote hoogte?  Vervuilde lucht veroorzaakt vroege sterfgevallen in de op fossiele brandstoffen gestookte Balkan
Vervuilde lucht veroorzaakt vroege sterfgevallen in de op fossiele brandstoffen gestookte Balkan Geologen identificeren de mineralogie van Mercurius
Geologen identificeren de mineralogie van Mercurius Klimaatverandering zal de wereldhandel in landbouwproducten hervormen
Klimaatverandering zal de wereldhandel in landbouwproducten hervormen NASA:ijzig object voorbij Pluto lijkt op roodachtige sneeuwpop
NASA:ijzig object voorbij Pluto lijkt op roodachtige sneeuwpop
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

