
Wetenschap
Zelf-geassembleerde nanostructuren raken hun doel
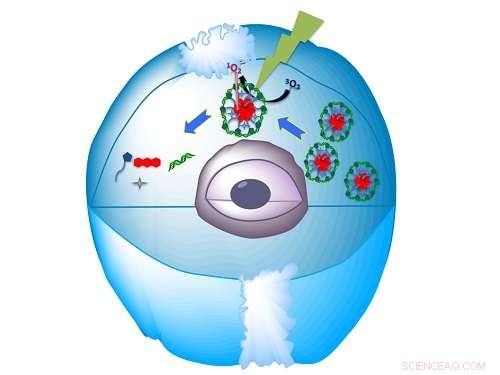
Het zelf-geassembleerde biocompatibele nanomateriaal levert het miRNA in de cel en laat het vervolgens vrij wanneer het door licht wordt geraakt. Krediet:KAUST
Een klein therapeutisch toedieningssysteem dat het vermogen van het lichaam om eiwitten te produceren kan controleren, is ontwikkeld door onderzoekers van de King Abdullah University of Science and Technology (KAUST) in Saoedi-Arabië.
Genen bevatten de instructies voor het maken van de eiwitten waaruit ons lichaam bestaat. Genetische informatie wordt vertaald in de eiwitten die nodig zijn om levende cellen te bouwen via een transcriptieproces waarbij de genetische code van DNA wordt gekopieerd naar een groot molecuul dat bekend staat als boodschapper-RNA (mRNA).
Dit transcriptieproces kan worden gewijzigd door korte dubbelstrengs RNA te introduceren, aangeduid als klein interfererend RNA (siRNA), die bindt aan het mRNA en de expressie van bepaalde genen remt. Het benutten van deze RNA-interferentie voor therapeutische toepassingen is moeilijk en vereist een materiaal dat het siRNA kan beschermen terwijl het door de bloedbaan reist, helpt het om het buitenmembraan van de cel te penetreren en het naar zijn doellocatie af te leveren.
"De levering van RNA is erg lastig omdat het gemakkelijk door cellen kan worden verteerd. Er zijn betere voertuigen nodig, zodat er meer RNA kan worden afgeleverd om genen te bewerken, ", zegt Niveen Khashab van het KAUST Smart Hybrid Materials Laboratory.
Khashab en haar collega's hebben nu biocompatibele nanostructuren aangetoond voor het leveren van siRNA en het efficiënt tot zwijgen brengen van genen1. Ze combineerden het macromolecuul histidine-capped-9, 10-dialkoxy-antraceen (HDA) en siRNA in water. Ze observeerden de zelfassemblage van bolvormige nanodeeltjes toen het water licht zuur was, maar niet wanneer het pH-neutraal was.
Khashab legt uit dat deze nanosferen worden gecreëerd door de elektrostatische interactie tussen het positief geladen HDA en het negatief geladen RNA. en dan wikkelen de twee lange armen van de HDA supramoleculaire zich om het siRNA om het te beschermen.
"Onze organische linker is in staat om te interageren met genetische materialen door waterstofbruggen en een leveringsvehikel te vormen, " legt Khashab uit. "De aanpak is schaalbaar en creëert reproduceerbare hoeveelheden ingekapseld RNA; het is ook biocompatibel en veilig."
De nanodeeltjes kunnen ook worden geactiveerd met zichtbaar licht. Wanneer bestraald door groene straling in aanwezigheid van een zure fluorescerende verbinding, bekend als eosine, de bol demonteert en geeft het siRNA vrij.
Het team toonde de effectiviteit van het nanodeeltje voor medicijnafgifte op B-cellymfoom 2, een mRNA-molecuul dat eiwitten creëert voor het reguleren van celdood. Ze toonden aan dat hun nanostructuren de gen-silencing-efficiëntie verbeteren en leidden tot gen-knockdown van meer dan 90 procent na blootstelling aan zichtbaar licht.
"De volgende stap is om het ontwerp aan te passen om andere ladingmoleculen zoals eiwitten te leveren en de lichtrespons op hogere golflengten in het nabij-infrarood te verbeteren, ' zegt Khashab.
 Nieuwe waterdichtings- en aangroeiwerende materialen ontwikkeld
Nieuwe waterdichtings- en aangroeiwerende materialen ontwikkeld Duurzame sterk geleidende elektrodematerialen van ultradunne koolstof nanovezel aerogels afgeleid van nanofibrillated
Duurzame sterk geleidende elektrodematerialen van ultradunne koolstof nanovezel aerogels afgeleid van nanofibrillated Fluorescerende sondes om cellulaire activiteit te bestuderen
Fluorescerende sondes om cellulaire activiteit te bestuderen Nieuw roodverschuivingsmechanisme van Ce3+ emissie in Ce
Nieuw roodverschuivingsmechanisme van Ce3+ emissie in Ce Een milieuvriendelijke methode voor de synthese van kaneelaldehyde
Een milieuvriendelijke methode voor de synthese van kaneelaldehyde
Hoofdlijnen
- Waarom hebben we grote hersenen?
- Dit is wat de wetenschap zegt over dierengevoel
- Waarom is bioinformatica belangrijk in genetisch onderzoek?
- De twee soorten exocriene secretoire cellen in de maag
- Olifantenstroperij in Afrika neemt af, maar ivoorvangsten nemen toe:studie
- Wat gebeurt er als je een lijk ontdooit?
- Wetenschappers roepen de VS op om onderzoek naar potmedicijnen voor huisdieren toe te staan
- Wie ontdekte hemoglobine?
- Top 5 onopgeloste hersenmysteries
- Hogesnelheidsmars door een laag grafeen
- Natuurkundigen benoemen en codificeren nieuw veld in nanotechnologie:elektronenkwantummetamaterialen

- Een model ontwikkelen dat cruciaal is voor het maken van betere apparaten

- Grafeen kan de sleutel zijn tot het versnellen van DNA-sequencing

- Onderzoekers stimuleren op silicium gebaseerde batterijen
 Een tektonische plaat bouwen voor een wetenschapsproject
Een tektonische plaat bouwen voor een wetenschapsproject Snapchat keert terug naar herontwerp waar gebruikers woedend over waren
Snapchat keert terug naar herontwerp waar gebruikers woedend over waren Motorola's Moto G7-lijn mikt op kopers van budgettelefoons met drie nieuwe telefoons
Motorola's Moto G7-lijn mikt op kopers van budgettelefoons met drie nieuwe telefoons Een robuust AI-centrisch indoor positioneringssysteem
Een robuust AI-centrisch indoor positioneringssysteem Heeft een 40 jaar oud Viking-experiment het leven op Mars ontdekt?
Heeft een 40 jaar oud Viking-experiment het leven op Mars ontdekt? 1, 001 manieren om een Nobelprijs te verliezen
1, 001 manieren om een Nobelprijs te verliezen Onderzoekers bestuderen de oppervlakken van ceria-nanodeeltjes
Onderzoekers bestuderen de oppervlakken van ceria-nanodeeltjes Het internet der dingen beveiligen in het kwantumtijdperk
Het internet der dingen beveiligen in het kwantumtijdperk
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

