
Wetenschap
Hersentumorcellen gepenetreerd door afbreekbare nanodeeltjes met genetische instructies
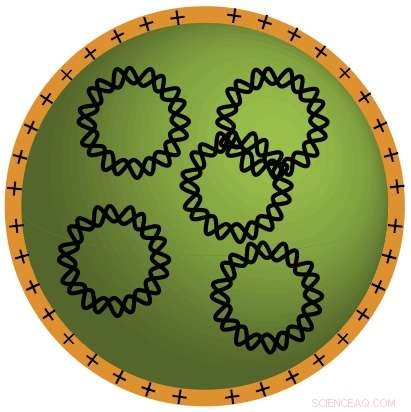
Biologisch afbreekbare plastic moleculen (oranje) zelf-assembleren met DNA-moleculen (verstrengeld, zwarte cirkels) om kleine nanodeeltjes te vormen die genen naar kankercellen kunnen dragen. Krediet:Stephany Tzeng
Samenwerken, Johns Hopkins biomedische ingenieurs en neurochirurgen melden dat ze kleine, biologisch afbreekbare "nanodeeltjes" die DNA naar hersenkankercellen bij muizen kunnen transporteren.
Het team zegt dat de resultaten van hun proof of principle-experiment suggereren dat dergelijke deeltjes geladen met "doodsgenen" op een dag aan hersenkankerpatiënten zouden kunnen worden gegeven tijdens neurochirurgie om selectief resterende tumorcellen te doden zonder normaal hersenweefsel te beschadigen.
Een samenvatting van de onderzoeksresultaten verscheen op 26 april online in het tijdschrift ACS Nano .
"Bij onze experimenten onze nanodeeltjes hebben met succes een testgen afgeleverd aan hersenkankercellen bij muizen, waar het toen werd ingeschakeld, " zegt Jordan Groen, doctoraat, een assistent-professor biomedische technologie en neurochirurgie aan de Johns Hopkins University School of Medicine. "We hebben nu bewijs dat deze kleine Trojaanse paarden ook genen kunnen dragen die selectief de dood in kankercellen induceren, terwijl gezonde cellen gezond blijven."
Green en zijn collega's concentreerden zich op glioblastomen, de meest dodelijke en agressieve vorm van hersenkanker. Met standaardbehandelingen van chirurgie, chemotherapie en bestraling, de mediane overlevingstijd is slechts 14,6 maanden, en verbetering zal alleen komen met het vermogen om tumorcellen te doden die resistent zijn tegen standaardbehandelingen, volgens Alfredo Quiñones-Hinojosa, MD, een professor in neurochirurgie aan de Johns Hopkins University School of Medicine en een lid van het onderzoeksteam.
Omdat de natuur de hersenen beschermt door het moeilijk te maken om via het bloed de cellen te bereiken, inspanningen richtten zich op het gebruik van deeltjes die tijdens de operatie tumorvernietigende DNA-instructies rechtstreeks naar kankercellen konden transporteren.
De eerste experimenten maakten gebruik van kankercellen die Quiñones-Hinojosa en zijn team uit gewillige patiënten verwijderden en in het laboratorium groeiden totdat ze kleine bolletjes cellen vormden, oncospheres genoemd, waarschijnlijk het meest resistent zijn tegen chemotherapie en bestraling, en in staat om nieuwe tumoren te creëren.
Quiñones-Hinojosa werkte vervolgens samen met Green om een voertuig te vinden voor genen die de dood zouden veroorzaken in de oncospheres. Green's laboratorium is gespecialiseerd in het produceren van kleine, ronde deeltjes gemaakt van biologisch afbreekbaar plastic waarvan de eigenschappen kunnen worden geoptimaliseerd voor het voltooien van verschillende medische missies. Door de atomen in het plastic te variëren, het team kan deeltjes maken die verschillende groottes hebben, stabiliteiten en affiniteiten voor water of olie. Voor deze studie is Het team van Green creëerde tientallen verschillende soorten deeltjes en testte hun vermogen om een testsequentie van DNA - met name een gen voor een rood of groen oplichtend eiwit - te dragen en af te leveren aan de oncospheres.
Door de overleving te beoordelen van de cellen die de deeltjes opslokken en de niveaus van rood of groen licht te meten die ze uitzonden, de onderzoekers bepaalden welke formulering van deeltjes het beste presteerde, testte vervolgens die formulering bij muizen met menselijke hersenkanker die afkomstig waren van hun patiënten.
Ze injecteerden de deeltjes rechtstreeks in muizen met een experimentele menselijke hersenkanker, en in de hersenen van gezonde muizen voor gebruik ter vergelijking. Verrassend genoeg, gezonde cellen produceerden zelden de gloeiende eiwitten, hoewel de DNA-dragende deeltjes in vergelijkbare aantallen tumorcellen en niet-tumorcellen binnendrongen. "Dit is precies wat je zou willen zien, kanker specificiteit, maar we onderzoeken nog steeds het mechanisme waardoor dit kan gebeuren, " zegt Green. "We hopen dat onze voortdurende experimenten hier licht op zullen werpen, zodat we wat we leren kunnen toepassen op andere scenario's."
"Het is opwindend om een manier te hebben gevonden om selectief genafgifte aan kankercellen te richten, ", zegt Quiñones-Hinojosa. "Het is een methode die veel haalbaarder en veiliger is voor patiënten dan traditionele gentherapie, die gemodificeerde virussen gebruikt om de behandeling uit te voeren."
Hij voegt eraan toe dat de deeltjes kunnen worden gevriesdroogd en ten minste twee jaar kunnen worden bewaard zonder hun effectiviteit te verliezen. "Met nanodeeltjes die zo lang stabiel blijven, kunnen we formuleringen ruim van tevoren en in grote batches maken, " zegt Stephany Tzeng, doctoraat, een lid van het team van Green. "Dit maakt ze gemakkelijk consistent te gebruiken in experimenten en operaties; we voegen water toe aan de deeltjes, en ze zijn klaar om te gaan."
In een verwante studie, online gepubliceerd op 27 maart in hetzelfde tijdschrift, Green's groep toonde ook aan dat een andere deeltjesformulering effectief zogenaamde siRNA's zou kunnen vervoeren en afleveren aan hersenkankercellen. siRNA's zijn zeer kleine moleculen die genetische informatie naar cellen transporteren, maar in tegenstelling tot DNA dat genen kan aanzetten, siRNA interfereert met de productie van bepaalde eiwitten en kan kankergenen uitschakelen.
Green legt uit dat siRNA's moeten worden ingekapseld in deeltjes die verschillen van de deeltjes die worden gebruikt om DNA te dragen, omdat siRNA's ongeveer 250 keer kleiner zijn dan de DNA-moleculen die gewoonlijk worden gebruikt voor gentherapie. "siRNA's zijn ook veel stijver dan DNA, en ze hoeven de celkern niet in omdat ze daarbuiten hun werk doen, in het cytoplasma, " hij zegt.
Een eerste bibliotheek van 15 biologisch afbreekbare deeltjesformuleringen werd getest op hun vermogen om siRNA's te dragen in menselijke glioblastomacellen die genetisch gemanipuleerd waren om groen fluorescerend eiwit (GFP) te maken. De siRNA's die aan de deeltjes werden toegevoegd, bevatten de GFP-code, dus succesvol gerichte cellen zouden niet meer groen gloeien.
Door de chemische eigenschappen van de deeltjes aan te passen, het team was in staat om een samenstelling te vinden die de gloed van GFP in de menselijke hersenkankercellen met 91 procent verminderde. Om het vermogen van de deeltjes te testen om dood-inducerende siRNA's af te geven, het team laadde de deeltjes met een mengsel van siRNA-codes die zijn ontworpen om te voorkomen dat belangrijke eiwitten worden gemaakt. Vervolgens voegden ze deze deeltjes toe aan hersenkankercellen en aan niet-kankerachtige hersencellen die in het laboratorium groeiden.
Net als in hun muizenstudie, het siRNA was effectiever - in dit geval bij het veroorzaken van celdood - in de hersenkankercellen (tot 97 procent effectief) dan in de niet-kankercellen (0 tot 27 procent, afhankelijk van het type nanodeeltjes).
Green benadrukt dat voor op nanodeeltjes gebaseerde genetische therapieën die veilig zijn voor patiënten, het specifieke siRNA of DNA dat in een klinische behandeling wordt afgeleverd, zou zorgvuldig worden gekozen, zodat, zelfs als er sprake was van off-target levering aan gezonde cellen, het zou alleen maar schadelijk zijn voor kankercellen. Groen wordt aangemoedigd door de resultaten tot nu toe. "Door te combineren wat we in deze twee onderzoeken hebben geleerd, misschien kunnen we zelfs deeltjes ontwerpen die tegelijkertijd DNA en siRNA kunnen leveren, "zegt hij. "Dat zou ons in staat stellen om de genetische zelfvernietigingscode die onze deeltjes afleveren nauwkeurig af te stemmen, zodat kankercellen afsterven en gezonde cellen niet."
"Dr. Green en zijn collega's hebben belangrijke stappen gezet bij de ontwikkeling van polymere nanodeeltjes voor DNA- en siRNA-afgifte, met veelbelovende specificiteit voor tumorcellen en verbeterde stabiliteit, " zei Jessica Tucker, doctoraat, programmadirecteur voor medicijn- en genafgiftesystemen en apparaten bij het National Institute of Biomedical Imaging and Bioengineering, die voor een deel van de financiering van deze studies zorgden. "Hoewel er nog veel uitdagingen zijn, dergelijk werk zou de behandelingsresultaten voor patiënten met glioblastoom en verwante hersentumoren mogelijk kunnen veranderen, waarvoor de huidige therapieën beperkte voordelen bieden."
 Het creëren van energieneutrale huizen, niet-giftige glitter en fossielvrije lijm met hout
Het creëren van energieneutrale huizen, niet-giftige glitter en fossielvrije lijm met hout Common Acid Base Indicators
Common Acid Base Indicators  Selectieve concentratie van kationische soorten
Selectieve concentratie van kationische soorten Nieuwe multidisciplinaire benadering voor het identificeren van complexe moleculaire adsorbaten
Nieuwe multidisciplinaire benadering voor het identificeren van complexe moleculaire adsorbaten Uit dikke lucht:kooldioxide omzetten in lichtemitterende koolstof
Uit dikke lucht:kooldioxide omzetten in lichtemitterende koolstof
 Waarom wereldwijde milieuactivisten zwijgen over de mijnbouwcrisis in Venezuela
Waarom wereldwijde milieuactivisten zwijgen over de mijnbouwcrisis in Venezuela Wat is het belang van de intertidale zone?
Wat is het belang van de intertidale zone?  Satellieten tonen verschillende kanten van orkaan Irma
Satellieten tonen verschillende kanten van orkaan Irma Spuitbussen voegen een nieuwe rimpel toe aan klimaatverandering in de tropische Stille Oceaan
Spuitbussen voegen een nieuwe rimpel toe aan klimaatverandering in de tropische Stille Oceaan Ultradun zonnescherm kan het Great Barrier Reef beschermen
Ultradun zonnescherm kan het Great Barrier Reef beschermen
Hoofdlijnen
- Onderzoek toont aan dat commerciële oogst van brekende schildpadden leidt tot bevolkingsafname
- De meeste zeeschildpadden zijn nu vrouwelijk in het noorden van het Great Barrier Reef
- Bij-nabootsende kaalvleugelmot zoemt na 130 jaar weer tot leven
- Is er echt een kurkcrisis?
- Biologisch onderzoek suggereert dat voeding van vaders vóór seks kan bijdragen aan de gezondheid van de baby
- 5 geheimen om erachter te komen Whatll zijn op het examen
- Menselijk genoom DNA-sequentietypen
- Verkoudheidsvirussen onthullen een van hun sterke punten
- De Saguaro Cactus is een iconisch symbool van het Amerikaanse zuidwesten
- Nieuwe biologische identiteit van ingeademde nanodeeltjes onthuld
- Onderzoekers gebruiken vloeibare inkt om betere zonnecellen te maken
- Poreus, supercondensatoren met ultralage temperatuur kunnen Mars van stroom voorzien, poolmissies

- Nieuwe coatingtechnologie gebruikt nanowormen om COVID-19 te doden
- Nieuwe bevroren rook kan robotchirurgie verbeteren energie opslag

 Lijst met de basisuitrusting voor het lassen
Lijst met de basisuitrusting voor het lassen  Zwart gat in het centrum van ons melkwegstelsel lijkt hongeriger te worden
Zwart gat in het centrum van ons melkwegstelsel lijkt hongeriger te worden Nanofibrillaire cellulosefilm om het uitvoeren van medische tests te vergemakkelijken
Nanofibrillaire cellulosefilm om het uitvoeren van medische tests te vergemakkelijken Cohesieonderzoekers ontrafelen het mysterie van waterstofeffecten op materialen
Cohesieonderzoekers ontrafelen het mysterie van waterstofeffecten op materialen Hoe een eenvoudige elektrische transformator voor school te bouwen
Hoe een eenvoudige elektrische transformator voor school te bouwen  Hoe de Edison Awards werken
Hoe de Edison Awards werken  Biomes of the Tundra: Food Chains and Webs
Biomes of the Tundra: Food Chains and Webs Simulatie van 195 miljoen jaar wereldklimaat in het Mesozoïcum
Simulatie van 195 miljoen jaar wereldklimaat in het Mesozoïcum
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

