
Wetenschap
Onderzoekers produceren uniforme antimoon-nanokristallen voor energieopslag
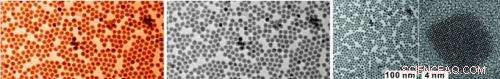
Onderzoekers van Empa en ETH Zürich zijn er voor het eerst in geslaagd om uniforme antimoon nanokristallen te produceren. Getest als componenten van laboratoriumbatterijen, deze kunnen een groot aantal zowel lithium- als natriumionen opslaan. Deze nanomaterialen werken met een hoge snelheid en kunnen uiteindelijk worden gebruikt als alternatieve anodematerialen in toekomstige batterijen met een hoge energiedichtheid.
De jacht is geopend - naar nieuwe materialen voor gebruik in de volgende generatie batterijen die op een dag de huidige lithium-ionbatterijen kunnen vervangen. Vandaag, de laatste zijn alledaags en bieden een betrouwbare stroombron voor smartphones, laptops en vele andere draagbare elektrische apparaten. Aan de ene kant, echter, elektrische mobiliteit en stationaire elektriciteitsopslag vereisen een groter aantal krachtigere batterijen; en de grote vraag naar lithium kan uiteindelijk leiden tot een tekort aan de grondstof. Daarom krijgt conceptueel identieke technologie op basis van natriumionen de komende jaren steeds meer aandacht. Hoewel 20 jaar lang onderzoek gedaan, materialen die natriumionen kunnen opslaan, blijven schaars.
Antimoon elektroden?
Een team van Empa en ETH Zürich onder leiding van Empa-onderzoeker Maksym Kovalenko is mogelijk een stap dichter bij het identificeren van alternatieve batterijmaterialen gekomen:ze zijn de eersten geworden die uniforme antimoon-nanokristallen synthetiseren, door hun speciale eigenschappen zijn ze uitstekende kandidaten voor een anodemateriaal voor zowel lithiumion- als natriumionbatterijen. De resultaten van het onderzoek van de wetenschappers zijn zojuist gepubliceerd in Nano-letters .
Voor een lange tijd, antimoon wordt beschouwd als een veelbelovend anodemateriaal voor hoogwaardige lithium-ionbatterijen, omdat dit metalloïde een hoge laadcapaciteit heeft, met een factor twee hoger dan die van veelgebruikt grafiet. Uit eerste onderzoeken bleek dat antimoon geschikt zou kunnen zijn voor oplaadbare lithium- en natriumionbatterijen omdat het beide soorten ionen kan opslaan. Natrium wordt beschouwd als een mogelijk goedkoop alternatief voor lithium, omdat het veel natuurlijker is en de reserves gelijkmatiger over de aarde zijn verdeeld.
Om antimoon zijn hoge opslagcapaciteit te laten bereiken, echter, het moet in een speciale vorm worden geproduceerd. De onderzoekers slaagden erin om uniforme - zogenaamde "monodisperse" - antimoonnanokristallen chemisch te synthetiseren die tussen de tien en twintig nanometer groot waren. Nanokristallen hebben een beslissend voordeel ten opzichte van grotere deeltjes:de volledige lithiëring of sodiatie van antimoon leidt tot grote volumetrische veranderingen. Met behulp van nanokristallen, deze modulaties van het volume kunnen omkeerbaar en snel zijn, en leiden niet tot onmiddellijke breuk van het materiaal. Een bijkomend belangrijk voordeel van nanokristallen (of nanodeeltjes) is dat ze vermengd kunnen worden met een geleidende koolstofvuller om aggregatie van de nanodeeltjes te voorkomen.
Ideale kandidaat voor anodemateriaal
Elektrochemische tests toonden aan dat elektroden gemaakt van antimoon-nanokristallen even goed presteren in natrium- en lithium-ionbatterijen. Dit maakt antimoon bijzonder veelbelovend voor natriumbatterijen, omdat de beste anodematerialen voor lithiumopslag (grafiet en silicium) niet werken met natrium.
Zeer monodisperse nanokristallen, met een grootteafwijking van tien procent of minder, maken het mogelijk om de optimale verhouding tussen grootte en prestatie te identificeren. Nanokristallen van tien nanometer of kleiner hebben last van oxidatie vanwege het grote oppervlak. Anderzijds, antimoonkristallen met een diameter van meer dan 100 nanometer zijn niet voldoende stabiel vanwege de eerder genoemde enorme volume-uitzetting en -krimp tijdens de werking van een batterij. De onderzoekers behaalden de beste resultaten met deeltjes van 20 nanometer groot.
Een ander belangrijk resultaat van het onderzoek, mogelijk gemaakt door deze ultra-uniforme deeltjes, is dat de onderzoekers een groottebereik van ongeveer 20 tot 100 nanometer hebben geïdentificeerd, waarbinnen dit materiaal uitstekende, grootte-onafhankelijke prestaties, zowel in termen van energiedichtheid als snelheidsvermogen. Deze eigenschappen maken het zelfs mogelijk om polydisperse antimoondeeltjes te gebruiken om dezelfde prestaties te verkrijgen als met zeer monodisperse deeltjes, zolang hun afmetingen binnen dit groottebereik van 20 tot 100 nanometer blijven. Experimenten van Kovalenko's groep op monodisperse nanodeeltjes van andere materialen tonen veel steilere verhoudingen tussen grootte en prestatie, zoals snel prestatieverval bij toenemende deeltjesgrootte, waardoor antimoon een unieke positie inneemt tussen de materialen die legeren met lithium en natrium. "Dit vereenvoudigt de taak om een economisch haalbare synthesemethode te vinden aanzienlijk", zegt Kovalenko. "De ontwikkeling van een dergelijke kosteneffectieve synthese is de volgende stap voor ons, samen met onze industriële partner."
Duurder alternatief
Betekent dit dat een alternatief voor de huidige lithium-ionbatterijen binnen handbereik ligt? Kovalenko schudt zijn hoofd. Hoewel de methode relatief eenvoudig is, de productie van voldoende hoogwaardige uniforme antimoon nanokristallen is nog te duur. "Globaal genomen, batterijen met natriumionen en antimoon-nanokristallen als anodes zullen alleen een veelbelovend alternatief vormen voor de huidige lithium-ionbatterijen als de productiekosten vergelijkbaar zullen zijn, " hij zegt.
Het zal hoogstwaarschijnlijk nog een decennium duren voordat een natriumionbatterij met antimoonelektroden op de markt kan komen. Het onderzoek naar het onderwerp staat nog in de kinderschoenen. "Echter, andere onderzoeksgroepen sluiten zich binnenkort aan bij de inspanningen, ’ is de chemicus overtuigd.
Kortom:Lithium-ion batterijen
Een huidige lithium-ionbatterij bestaat uit twee elektroden - een kathode en een anode. De anode is vaak gemaakt van grafiet, de kathode van metaaloxiden zoals kobaltoxide. De lithiumionen nestelen zich in deze materialen tijdens het laad- of ontlaadproces. De twee elektroden zijn gescheiden door een separator die alleen doorlaatbaar is voor lithiumionen die zich tussen de twee elektroden verplaatsen. Tijdens het ontladen van de batterij, de lithiumionen verschuiven van de anode naar de kathode. De elektronen maken een "omweg" via een extern elektronisch apparaat, die wordt aangedreven door de resulterende elektronenflux. Elektronen en ionen ontmoeten elkaar weer bij de kathode. Wanneer de batterij wordt opgeladen, lithiumionen en elektronen stromen in de tegenovergestelde richting. Om de batterij effectief en langdurig te laten werken, de ionen moeten gemakkelijk in en uit de elektrodematerialen kunnen bewegen. De vorm en grootte van de elektrodematerialen zouden niet veel moeten veranderen door de terugkerende absorptie en afgifte van de ionen.
 Zelfreinigend beton kan gebouwen er als nieuw uit laten zien
Zelfreinigend beton kan gebouwen er als nieuw uit laten zien Chemici stellen nieuwe heilzame katalysator voor voor uitgangsmaterialen in de farmacie
Chemici stellen nieuwe heilzame katalysator voor voor uitgangsmaterialen in de farmacie Hoe te bepalen of er een reactie was in een chemische vergelijking
Hoe te bepalen of er een reactie was in een chemische vergelijking  Nieuwe glasmaterialen gemaakt van organische en anorganische componenten
Nieuwe glasmaterialen gemaakt van organische en anorganische componenten Video:Vampierenfolklore heeft meer chemie dan je zou denken
Video:Vampierenfolklore heeft meer chemie dan je zou denken
 Onderzoekers ontwikkelen methode om schade door natuurrampen te beoordelen
Onderzoekers ontwikkelen methode om schade door natuurrampen te beoordelen Pollenseizoen in Zwitserland eerder en intenser door klimaatverandering
Pollenseizoen in Zwitserland eerder en intenser door klimaatverandering Slechts 1 pct van het grootste koraalrif van Japan gezond:onderzoek
Slechts 1 pct van het grootste koraalrif van Japan gezond:onderzoek Broeikasemissies van Siberische rivieren pieken naarmate de permafrost ontdooit
Broeikasemissies van Siberische rivieren pieken naarmate de permafrost ontdooit Serieus worden over het beperken van de opwarming van de aarde, de wereld kan zichzelf meer dan $ 20 biljoen besparen
Serieus worden over het beperken van de opwarming van de aarde, de wereld kan zichzelf meer dan $ 20 biljoen besparen
Hoofdlijnen
- Waarin verschillen mensen van onze voorouders?
- De functies van de linker temporale kwab
- Verschillen tussen gisten en vormpjes
- Een nieuwe studie toont aan dat mieren voor de verstandigere optie kiezen, zelfs als dat betekent dat je wat harder moet werken
- Interspecifieke concurrentie versus intraspecifieke concurrentie
- Verschil tussen triglyceriden en fosfolipiden
- Welke organel moet aanwezig zijn in grote aantallen in spiercellen?
- Welk Genotype zijn vrouwen?
- Bereken de percentages van adenine in een DNA-streng
- Boornitride is een veelbelovende weg naar praktische grafeenapparaten

- Experimenten laten zien hoe memristors werken
- Geneesmiddelleverende nanodeeltjes zoeken en vernietigen ongrijpbare kankerstamcellen

- Guinness record:het dunste glas ter wereld is slechts twee atomen dik

- Efficiëntierecord voor zwarte siliciumzonnecellen springt naar 22,1 procent

 Nieuwe strategie om een in de handel verkrijgbare iboga-alkaloïde om te zetten in post-iboga-alkaloïden
Nieuwe strategie om een in de handel verkrijgbare iboga-alkaloïde om te zetten in post-iboga-alkaloïden Handen wassen ondanks gebrek aan water
Handen wassen ondanks gebrek aan water Beter begrip van waterstofperoxideregulatie kan leiden tot nieuwe inzichten in ziekteontwikkeling
Beter begrip van waterstofperoxideregulatie kan leiden tot nieuwe inzichten in ziekteontwikkeling Hoe Cherry Cherry Trees te identificeren
Hoe Cherry Cherry Trees te identificeren Niet-invasieve intensiteitsmetingen van lage-energiestralen voor het eerst gedemonstreerd
Niet-invasieve intensiteitsmetingen van lage-energiestralen voor het eerst gedemonstreerd Berekening van bandwisselingen per mijl
Berekening van bandwisselingen per mijl  Laserdiode straalt diep UV-licht uit
Laserdiode straalt diep UV-licht uit Benodigde materialen voor fotosynthese
Benodigde materialen voor fotosynthese
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway | Italian |

-
Wetenschap © https://nl.scienceaq.com

