
Wetenschap
Niet-covalente krachten begrijpen:sleutelinteracties in de chemie en biologie
Hier zijn enkele kernpunten over niet-covalente krachten:
Soorten niet-covalente krachten:
* Waterstofbinding: Dit is het sterkste type niet-covalente interactie, waarbij een speciale dipool-dipoolinteractie betrokken is tussen een waterstofatoom dat covalent gebonden is aan een zeer elektronegatief atoom (zoals zuurstof of stikstof) en een elektronenpaar in het eenzame paar van een ander elektronegatief atoom. Voorbeelden hiervan zijn de waterstofbinding tussen watermoleculen en de basenparing in DNA.
* Ionische interacties: Deze komen voor tussen tegengesteld geladen ionen. Deze aantrekkingskracht is in water relatief sterk en speelt een sleutelrol bij de vorming van zouten en de stabilisatie van eiwitten.
* Van der Waals-interacties: Dit zijn zwakke krachten die voortkomen uit tijdelijke fluctuaties in de elektronenverdeling rond moleculen. Ze kunnen verder worden onderverdeeld in:
* Dipool-dipoolinteracties: Deze komen voor tussen polaire moleculen met permanente dipolen.
* Londense verspreidingstroepen: Deze komen voor tussen alle moleculen, zelfs niet-polaire, als gevolg van tijdelijke dipolen die worden veroorzaakt door elektronenfluctuaties.
* Hydrofobe interacties: Dit is technisch gezien geen kracht, maar eerder een gevolg van de neiging van niet-polaire moleculen om contact met water te vermijden. Ze zijn cruciaal voor de eiwitvouwing en membraanvorming.
Kenmerken van niet-covalente krachten:
* Zwakker dan covalente bindingen: Ze kunnen gemakkelijker worden verstoord door veranderingen in temperatuur of pH.
* Richting: Ze vertonen een specifieke directionaliteit en geometrie, wat belangrijk is voor de vorming van specifieke structuren zoals eiwitplooien.
* Gezamenlijk sterk: Hoewel individuele niet-covalente bindingen zwak zijn, kan hun gecombineerde effect aanzienlijk zijn.
Belang van niet-covalente krachten:
* Biologische processen: Ze zijn essentieel voor:
* Eiwitvouwing en stabiliteit
* Enzym-substraatinteracties
* DNA-replicatie en transcriptie
* Cel-celherkenning
* Membraanvorming
* Materiaalwetenschappen: Ze beïnvloeden de eigenschappen van polymeren, kunststoffen en andere materialen.
Voorbeelden van niet-covalente krachten in actie:
* Water: Waterstofbinding tussen watermoleculen is verantwoordelijk voor het hoge kookpunt en de oppervlaktespanning.
* DNA: Waterstofbruggen tussen de stikstofbasen houden de twee DNA-strengen bij elkaar.
* Eiwitvouwing: Een complex samenspel van hydrofobe interacties, waterstofbruggen en ionische interacties zorgt ervoor dat eiwitten in hun functionele driedimensionale vormen worden opgevouwen.
Over het algemeen zijn niet-covalente krachten van vitaal belang voor de structuur, functie en interacties van moleculen in biologische en chemische systemen. Hun kracht en gerichtheid maken een breed scala aan diverse en complexe interacties mogelijk die ten grondslag liggen aan het leven zelf.
 Krachtige nieuwe dataset onthult patronen van wereldwijde ozonvervuiling
Krachtige nieuwe dataset onthult patronen van wereldwijde ozonvervuiling Wanneer een Hummingbird Feeder in Austin, Texas
Wanneer een Hummingbird Feeder in Austin, Texas Nieuw onderzoek dat eerst het smelten van Antarctisch zee-ijs relateert aan weersverandering in de tropen
Nieuw onderzoek dat eerst het smelten van Antarctisch zee-ijs relateert aan weersverandering in de tropen Hebben oude koffiehuizen de basis gelegd voor het moderne consumentisme?
Hebben oude koffiehuizen de basis gelegd voor het moderne consumentisme?  Artefacten van de Anasazi Ancient Indian Tribe
Artefacten van de Anasazi Ancient Indian Tribe
Hoofdlijnen
- Welke van de volgende paren protisten en hun kenmerken is niet overeengekomen?
- Wat zijn kenmerken van alle organismen?
- De kern van een cel coördineert processen en activiteiten die in de cel plaatsvinden. welke twee systemen vervullen een soortgelijke functie in het menselijk lichaam?
- Hoe worden geproduceerde enkele cel -eiwitten?
- Wat voor soort organismen zijn de belangrijkste groepen ontleders?
- Welke eigenschappen hebben draken?
- Welke organellen worden aangetroffen in plantencellen die energie van zonlicht absorberen en gebruiken om chemische reacties aan te sturen, produceren zuurstof van suikers?
- Wat doet een antigeen?
- Wat doet het RESTPotory -systeem?
- Hoe inzichten in superkritische vloeistoffen ons kunnen helpen het binnenste van de gigantische gasplaneten te begrijpen

- Wetenschap volgt uit harige mysteries

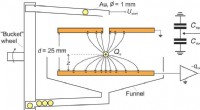
- Dynamiek van contactelektrificatie
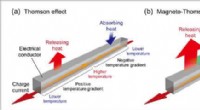
- 'S Werelds eerste directe waarneming van het magneto-Thomson-effect
- Onderzoeksteam bepaalt hoe elektronenspins interageren met kristalrooster in nikkeloxide

 De primaire functie van de nucleolus?
De primaire functie van de nucleolus?  Volkswagen biedt vanaf 2019 volledig elektrisch autodelen aan
Volkswagen biedt vanaf 2019 volledig elektrisch autodelen aan Wat gebeurt er met de kleine deeltjes materie in een vloeistof wanneer deze het vriespunt nadert?
Wat gebeurt er met de kleine deeltjes materie in een vloeistof wanneer deze het vriespunt nadert?  Wat is chemische k?
Wat is chemische k?  Kan een kopje zout en water beide een oplossing zijn?
Kan een kopje zout en water beide een oplossing zijn?  Onderzoek identificeert refugia voor klimaatverandering in droge bosregio
Onderzoek identificeert refugia voor klimaatverandering in droge bosregio Zwavelzuur (H₂SO₄) en salpeterzuur (HNO₃):chemische formules uitgelegd
Zwavelzuur (H₂SO₄) en salpeterzuur (HNO₃):chemische formules uitgelegd  Wat is de versnelling van een auto die constante snelheid 100 gaat?
Wat is de versnelling van een auto die constante snelheid 100 gaat?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

