
Wetenschap
Hoe is het mogelijk dat twee atomen van hetzelfde element verschillende massa's hebben?
Hier is een uitsplitsing:
* atomen: De basisbouwstenen van materie, bestaande uit protonen, neutronen en elektronen.
* element: Een stof die bestaat uit slechts één type atoom, gedefinieerd door het aantal protonen (atoomnummer).
* isotopen: Atomen van hetzelfde element met hetzelfde aantal protonen maar verschillende aantallen neutronen.
Omdat neutronen massa hebben, verschillen isotopen van hetzelfde element in hun atomaire massa . Dit komt omdat de massa van een atoom voornamelijk wordt bepaald door het aantal protonen en neutronen in zijn kern.
Voorbeeld:
* Carbon-12 (¹²C) heeft 6 protonen en 6 neutronen.
* Carbon-14 (¹⁴C) heeft 6 protonen en 8 neutronen.
Beide zijn koolstofatomen, maar ¹⁴C is zwaarder vanwege de extra neutronen.
Sleutelpunten:
* Atomisch nummer bepaalt het element.
* Massienummer (Aantal protonen + neutronen) bepaalt de isotoop.
* De aanwezigheid van isotopen legt uit waarom de atomaire massa van een element op het periodiek systeem geen heel getal is. Het is een gemiddelde van de massa van alle natuurlijk voorkomende isotopen van dat element.
Concluderend leidt de variatie in het aantal neutronen binnen isotopen van hetzelfde element tot verschillende atomaire massa's, hoewel de elementen zelf worden gedefinieerd door hun consistente aantal protonen.
Hoofdlijnen
- Wat het doel van mitochondria in een cel?
- Wat is een levend wezen dat prokaryotisch is?
- Hoe het Human Microbiome-project werkt
- Wat is een eencellige eukaryoot?
- Welke groep ziekteverwekkers zijn eencellige microscopische organismen?
- 'Als een tunnel voor cholesterol':Wetenschappers laten zien hoe 'slechte' cholesterol in de cellen terechtkomt
- Longhornteek voor het eerst ontdekt in het noorden van Missouri
- Wat zou u moeten doen bepalen of bacteriën die op een petri -plaat van de brouwerpot groeien, anaëroben zijn?
- Wat zijn de stappen in de meiose die de variabiliteit verhogen?
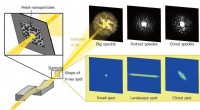
- Oude röntgenfoto's, nieuwe visie:een nanogerichte röntgenlaser
- Doorbraak van nanodeeltjes kan ongezien licht opvangen voor conversie van zonne-energie

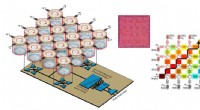
- Chip-scale Floquet topologische isolatoren om 5G draadloze communicatie te verbeteren
- Virtuele lens verbetert röntgenmicroscopie

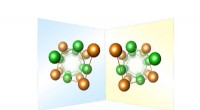
- Enantiomorph-distributiekaarten voor metalen en metaallegeringen
 Wat is de kracht die de korst uit elkaar trekt?
Wat is de kracht die de korst uit elkaar trekt?  De toenemende droogte stelt de veerkracht van het Amazone-regenwoud op de proef
De toenemende droogte stelt de veerkracht van het Amazone-regenwoud op de proef  Wat gebeurt er als twee bewegende objecten botsen, maar de een gaat sneller dan de andere?
Wat gebeurt er als twee bewegende objecten botsen, maar de een gaat sneller dan de andere?  Cijfers over ongelijkheid spreken niet voor zich
Cijfers over ongelijkheid spreken niet voor zich In de toekomst intensere en frequentere overstromingen en droogtes
In de toekomst intensere en frequentere overstromingen en droogtes Biosensor kan helpen bij het diagnosticeren van ziekten direct in serum
Biosensor kan helpen bij het diagnosticeren van ziekten direct in serum Onderzoek geeft inzicht in hoe bedrijven moeten reageren op negatieve publiciteit
Onderzoek geeft inzicht in hoe bedrijven moeten reageren op negatieve publiciteit  Eieren van wijnstokvretende insecten ontdekt op weg naar Californië:lopen wijngaarden gevaar?
Eieren van wijnstokvretende insecten ontdekt op weg naar Californië:lopen wijngaarden gevaar?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


