
Wetenschap
Hoe is John Dalton Ivent Atomic Theory?
1. Oude Griekse wortels: Het concept van atomen dateert uit het oude Griekenland met filosofen zoals Democritus en Leucippus. Ze stelden het idee voor dat materie bestond uit ondeelbare deeltjes.
2. Dalton's experimentele observaties: Dalton was een nauwgezette experimentalist. Hij bestudeerde het gedrag van gassen, met name hun meng- en reactieverhoudingen. Hij merkte op dat chemische reacties altijd specifieke verhoudingen van elementen (wet van duidelijke verhoudingen) betroffen en dat wanneer elementen in verschillende verhoudingen gecombineerd waren, ze verschillende verbindingen vormden (wet van meerdere verhoudingen).
3. De atomaire theorie posten: Op basis van zijn observaties stelde Dalton de volgende postulaten voor in zijn atoomtheorie:
* Alle materie bestaat uit atomen, die ondeelbare en onverwoestbare deeltjes zijn.
* atomen van een bepaald element zijn identiek in grootte, massa en andere eigenschappen.
* Atomen van verschillende elementen verschillen in grootte, massa en andere eigenschappen.
* chemische reacties omvatten de combinatie, scheiding of herschikking van atomen.
* Verbindingen worden gevormd wanneer atomen van verschillende elementen combineren in vaste, gehele nummerverhoudingen.
4. Voortbouwend op eerder werk: Dalton bouwde op het werk van andere wetenschappers, waaronder:
* Robert Boyle: Boyle's werk aan gassen hielp bij het leggen van de basis voor Dalton's begrip van het gedrag van materie.
* Antoine Lavoisier: Lavoisier's werk over het behoud van massa hielp Dalton om te begrijpen dat chemische reacties niet alleen de creatie of vernietiging van materie waren, maar eerder een herschikking van bestaande atomen.
5. Belang van de theorie van Dalton: Dalton's atomaire theorie bracht een revolutie teweeg in ons begrip van chemie. Het bood een raamwerk voor het verklaren van chemische reacties en de eigenschappen van stoffen. Het maakte ook de weg vrij voor toekomstige ontdekkingen op het gebied van atomaire structuur.
Belangrijke punten om te onthouden:
* De theorie van Dalton was niet perfect en is in de loop van de tijd verfijnd.
* We weten nu dat atomen deelbaar zijn in kleinere deeltjes en dat atomen van hetzelfde element iets verschillende massa's kunnen hebben (isotopen).
* Ondanks zijn beperkingen blijft de atomaire theorie van Dalton een fundamentele hoeksteen van de moderne chemie.
 Deeltjes die kleiner zijn dan een atoom
Deeltjes die kleiner zijn dan een atoom  Hoe verhoudt depositie zich tot co2?
Hoe verhoudt depositie zich tot co2?  Fasegescheiden eiwitachtige lijmen als zelforganizer van microfilamentnetwerken
Fasegescheiden eiwitachtige lijmen als zelforganizer van microfilamentnetwerken Schrijf de chemische vergelijking die de bereiding van etheen uit ethanol weergeeft?
Schrijf de chemische vergelijking die de bereiding van etheen uit ethanol weergeeft?  Gemeenschappelijke herbicideverbinding kan miljoenen levens redden
Gemeenschappelijke herbicideverbinding kan miljoenen levens redden
 Arctische permafrost stoot meer koolstofdioxide uit dan ooit werd gedacht
Arctische permafrost stoot meer koolstofdioxide uit dan ooit werd gedacht Wat zijn drie aanpassingen die reptielen hebben voor het behoud van water?
Wat zijn drie aanpassingen die reptielen hebben voor het behoud van water?  Bodemgemeenschappen bedreigd door vernietiging, instabiliteit van Amazone-bossen
Bodemgemeenschappen bedreigd door vernietiging, instabiliteit van Amazone-bossen Onderzoeker weegt op feeënkringen van Namibië
Onderzoeker weegt op feeënkringen van Namibië Spiders of Cape Cod, Massachusetts
Spiders of Cape Cod, Massachusetts
Hoofdlijnen
- Welke processen kunnen resulteren in de netto beweging van een stof naar de cel als deze geconcentreerder is dan de omgeving?
- Wat is Citrobacter Freundii -complex?
- Hoe is een bedrijf dat beheerders van secretaressies in dienst heeft en andere functies die vergelijkbaar zijn met meercellig organisme?
- Waarom is water belangrijk in cella?
- Waarom zijn er zo weinig vissen in de oceanen van de aarde?
- Is aardappelschuim een bacterieschimmel of virus?
- Lijst in volgorde van de structuren die voedsel door het typische spijsverteringsstelsel van gewervelde dieren moet passeren?
- Reuzenberenklauwsap kan je zonnebrand geven
- Hoe kan embryonale ontwikkeling worden gebruikt als bewijs voor evolutie?
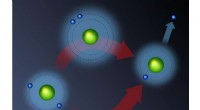
- Wetenschappers observeren hoe kwantumsuperposities zich binnen femtoseconden opbouwen in een heliumatoom
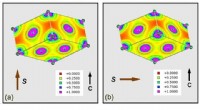
- Wetenschappers ontdekken mogelijk pad om samarium-kobaltmagneten te verbeteren
- GERDA-experiment klaar om zeldzaamste radioactief verval te ontdekken

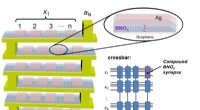
- Nieuwe memristor verhoogt de nauwkeurigheid en efficiëntie voor neurale netwerken op atomaire schaal
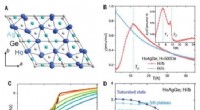
- Kagome-spinijs realiseren in een gefrustreerde intermetallische verbinding
 Tussen welke soorten elementen vindt covelente binding plaats?
Tussen welke soorten elementen vindt covelente binding plaats?  Vraag Siri vandaag niet naar Donald Trump
Vraag Siri vandaag niet naar Donald Trump Nieuw onderzoek laat zien welke soorten mensen het meest geneigd zijn hun belastingen te laag aan te geven
Nieuw onderzoek laat zien welke soorten mensen het meest geneigd zijn hun belastingen te laag aan te geven Is de snelheid van het licht het snelst in vloeistof?
Is de snelheid van het licht het snelst in vloeistof?  Hoe speelgoed gendergerelateerd werd - en waarom er meer nodig is dan een genderneutrale pop om de manier waarop jongens vrouwelijkheid waarnemen te veranderen
Hoe speelgoed gendergerelateerd werd - en waarom er meer nodig is dan een genderneutrale pop om de manier waarop jongens vrouwelijkheid waarnemen te veranderen Scholen concurreren met mobiele telefoons. Hier is hoe zij denken dat ze zouden kunnen winnen
Scholen concurreren met mobiele telefoons. Hier is hoe zij denken dat ze zouden kunnen winnen  Kun je 2 amp -lader gebruiken om een 3 -apparaat op te laden?
Kun je 2 amp -lader gebruiken om een 3 -apparaat op te laden?  Hoeveel mol gas bezetten 1,3 L bij een druk 3,89 atmosferen en temperatuur 323 K?
Hoeveel mol gas bezetten 1,3 L bij een druk 3,89 atmosferen en temperatuur 323 K?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

