
Wetenschap
Wat is de massa van een proton dat ongeveer gelijk is aan van?
De massa van een proton is ongeveer gelijk aan 1 Atomic Mass Unit (AMU) .
Dit is waarom:
* Atomic Mass Unit (AMU): Deze eenheid wordt gedefinieerd als 1/12e de massa van een koolstof-12-atoom.
* proton en neutronenmassa: Protonen en neutronen zijn de belangrijkste componenten van de kern van een atoom. Ze hebben zeer vergelijkbare massa's, waarbij protonen iets zwaarder zijn.
* benadering: Voor veel berekeningen is het handig om de massa van een proton (en neutron) te benaderen als 1 AMU.
Het is belangrijk op te merken dat de werkelijke massa van een proton iets meer dan 1 AMU is:
* protonmassa: 1.007276466879 AMU
Voor de meeste algemene doeleinden is de benadering van 1 AMU echter voldoende.
 Welk volume 2,5 M NaOH-oplossing is nodig om 2,0 liter 0,75 M NaOH te bereiden?
Welk volume 2,5 M NaOH-oplossing is nodig om 2,0 liter 0,75 M NaOH te bereiden?  Vindt er een reactie plaats als NiCl2(aq) wordt toegevoegd aan een reageerbuisje met Zn(NO3)2(aq)?
Vindt er een reactie plaats als NiCl2(aq) wordt toegevoegd aan een reageerbuisje met Zn(NO3)2(aq)?  Wat zijn 5 voorbeelden van oplosmiddelen?
Wat zijn 5 voorbeelden van oplosmiddelen?  Bioactief boraatglas op nanoschaal:een materiaal van de volgende generatie voor huidgenezing
Bioactief boraatglas op nanoschaal:een materiaal van de volgende generatie voor huidgenezing Methode voor het opslaan van monsters kan de gezondheidszorg in regio's met beperkte middelen verbeteren
Methode voor het opslaan van monsters kan de gezondheidszorg in regio's met beperkte middelen verbeteren
 Bleken van koraalriffen verminderd waar dagelijkse temperatuurveranderingen groot zijn
Bleken van koraalriffen verminderd waar dagelijkse temperatuurveranderingen groot zijn Onderzoek onthult bewijs van klimaatverandering in de permafrost van Yukon
Onderzoek onthult bewijs van klimaatverandering in de permafrost van Yukon Storm Elsa rukt op over Florida na bestorming van Cuba
Storm Elsa rukt op over Florida na bestorming van Cuba Studie koppelt openluchtrecreatie aan zorgen over waterkwaliteit
Studie koppelt openluchtrecreatie aan zorgen over waterkwaliteit Bij benaderingen voor bosbehoud moeten de rechten van de lokale bevolking worden erkend
Bij benaderingen voor bosbehoud moeten de rechten van de lokale bevolking worden erkend
Hoofdlijnen
- Geen designerbaby’s, maar genbewerking om ziekten te voorkomen? Misschien
- Leven gelukkige mensen langer?
- Waarom liegen mensen over dingen die gemakkelijk weerlegd kunnen worden?
- Sprinten richting uitsterven? Het aantal cheetahs daalt wereldwijd
- Overtroeft een politieke partij de ideologie?
- Wat is lefdatie?
- Zou u op een Democraat stemmen die zich als Republikein gedraagt?
- Je kunt echt op je naam lijken,
- Hoe verschilt DNA & RNA?
- Wetenschappers onthullen de kracht achter het gordijn - met neutronen

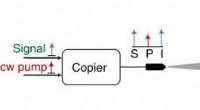
- Ruimtecommunicatie:ontwikkeling van een ontvanger van één foton per bit met behulp van bijna geruisloze fasegevoelige versterking
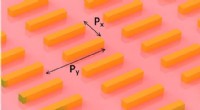
- Een nieuwe wet voor metamaterialen
- Ons bereik in de kosmos uitbreiden met nieuwe spiegelcoatings

- Studie onthult nieuwe materiaalinteracties die de gegevensopslag kunnen verbeteren

 Wat is de gecombineerde diameter van Mars en zijn manen?
Wat is de gecombineerde diameter van Mars en zijn manen?  Nanodeeltjes en hun grootte zijn misschien geen grote problemen
Nanodeeltjes en hun grootte zijn misschien geen grote problemen Wie heeft enkele van de sterrenbeelden genoemd?
Wie heeft enkele van de sterrenbeelden genoemd?  Wat gebeurt er op het chromosomale niveau als een resultaat van bevruchting?
Wat gebeurt er op het chromosomale niveau als een resultaat van bevruchting?  Grafeentapijten:zodat neuronen beter communiceren
Grafeentapijten:zodat neuronen beter communiceren Grote milieu-uitdaging aangezien microplastics schadelijk zijn voor ons drinkwater
Grote milieu-uitdaging aangezien microplastics schadelijk zijn voor ons drinkwater Nieuwe techniek om moleculen en materialen te bestuderen op kwantumsimulator ontdekt
Nieuwe techniek om moleculen en materialen te bestuderen op kwantumsimulator ontdekt Menselijke reacties van de uitbarsting Montserrat?
Menselijke reacties van de uitbarsting Montserrat?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

