
Wetenschap
Welke intermoleculaire krachten zijn aanwezig in SiF4?
Siliciumtetrafluoride (SiF4) is een moleculaire verbinding die bestaat uit een centraal siliciumatoom gebonden aan vier fluoratomen. Het siliciumatoom is omgeven door een tetraëdrische opstelling van fluoratomen en het molecuul is niet-polair. Hoewel het molecuul zelf niet-polair is, ondervindt het wel intermoleculaire krachten. Deze krachten staan bekend als van der Waals-krachten.
Van der Waals-krachten zijn zwakke intermoleculaire interacties die optreden tussen alle moleculen. Ze omvatten drie verschillende soorten interacties:permanente dipool-permanente dipoolinteracties, geïnduceerde dipool-geïnduceerde dipoolinteracties en Londense dispersiekrachten:
- Permanente dipool-permanente dipool-interacties optreden tussen moleculen die permanente dipolen hebben. In het geval van SiF4 is er geen permanent dipoolmoment omdat het molecuul symmetrisch is en de ladingen gelijkmatig verdeeld zijn. Daarom zijn er geen permanente dipool-permanente dipool-interacties aanwezig.
- Geïnduceerde dipool-geïnduceerde dipoolinteracties optreden tussen moleculen die tijdelijke dipolen hebben. Deze tijdelijke dipolen ontstaan wanneer de elektronenwolken van twee moleculen fluctueren en enigszins gepolariseerd raken. De fluctuaties in de elektronenwolken van één molecuul kunnen een dipool in een naburig molecuul induceren. Deze interactie is relatief zwak en is alleen significant als de moleculen heel dicht bij elkaar staan. In SiF4 zijn geïnduceerde dipool-geïnduceerde dipoolinteracties de zwakste van de drie soorten van der Waals-krachten als gevolg van de bijna bolvormige elektronenwolk van silicium.
- Londense verspreidingskrachten zijn de sterkste van de van der Waals-krachten en komen voor tussen alle moleculen, zelfs degenen die niet-polair zijn. Londense dispersiekrachten worden veroorzaakt door de tijdelijke fluctuaties in de elektronenwolken van moleculen. Deze fluctuaties kunnen onmiddellijke dipolen creëren, die vervolgens dipolen in aangrenzende moleculen kunnen induceren. Londense dispersiekrachten zijn aanwezig in SiF4 en zijn de belangrijkste kracht die verantwoordelijk is voor de aantrekking tussen SiF4-moleculen. Omdat de Londense dispersiekrachten over het algemeen sterker zijn voor grotere moleculen, zijn ze belangrijker voor SiF4 dan voor kleinere moleculen zoals CO2 of H2O.
Samenvattend zijn de intermoleculaire krachten die aanwezig zijn in SiF4 van der Waals-krachten , waaronder geïnduceerde dipool-geïnduceerde dipoolinteracties en Londense verspreidingskrachten . Permanente dipool-permanente dipool-interacties zijn niet aanwezig in SiF4 vanwege de afwezigheid van een permanent dipoolmoment.
 Ultraheldere röntgenstralen laten zien hoe planten binnen een fractie van een seconde op licht reageren
Ultraheldere röntgenstralen laten zien hoe planten binnen een fractie van een seconde op licht reageren Welke symbolen zie je in een laboratorium?
Welke symbolen zie je in een laboratorium?  Wat is een chemische eigenschap die kan worden gebruikt om calciumcarbonaat te identificeren?
Wat is een chemische eigenschap die kan worden gebruikt om calciumcarbonaat te identificeren?  Waarom bruist Alka Seltzer?
Waarom bruist Alka Seltzer?  Ontwikkeling van een met superbase vergelijkbare oxynitride-katalysator
Ontwikkeling van een met superbase vergelijkbare oxynitride-katalysator
 Krachtige tropische cycloon Veronica kijkt naar de Australische kust van Pilbara
Krachtige tropische cycloon Veronica kijkt naar de Australische kust van Pilbara Het verhaal achter een unieke donkere wetlandbodem
Het verhaal achter een unieke donkere wetlandbodem Waarom jonge stellen niet trouwen:ze zijn bang voor de verwoestingen van een scheiding
Waarom jonge stellen niet trouwen:ze zijn bang voor de verwoestingen van een scheiding  NASA-NOAA-satelliet kijkt in gescheurde ogen van tyfoon Tramis
NASA-NOAA-satelliet kijkt in gescheurde ogen van tyfoon Tramis Giftige en niet-giftige slangen
Giftige en niet-giftige slangen
Hoofdlijnen
- Nog een Homo-soort? Recente 3D-vergelijkende analyse bevestigt de status van floresiensis als een fossiele menselijke soort
- Verklaring van celspecialisatie
- Wat zijn de kansen? Waarschijnlijkheid lost een evolutionaire puzzel op
- Waarom kunstmatige intelligentie de gezondheidszorg nog niet heeft gerevolutioneerd
- Je bent wat je eet – als je een koraalrifvis bent
- Second Life-gegevens bieden inzicht in hoe trends zich verspreiden
- Paper onderzoekt hoe onderzoekers verantwoordelijkheid hebben voor de verhalen die zij opvragen en opnieuw vertellen
- Het is misschien tijd om de houdbaarheidsdatum op voedselverpakkingen te schrappen, zeggen slimme verpakkingsonderzoekers
- Nieuw onderzoek laat zien hoe amyloïde bèta de hersencellen binnendringt
- Magneten getoond om meer vermogen te creëren in elektrische generatoren

- Team weerlegt hypothesen over perovskiet-zonnecellen, waardoor betere benaderingen voor gerichte optimalisatie mogelijk zijn

- Defecten in vloeibare kristallen fungeren als gidsen in kleine oceanen, het sturen van deeltjesverkeer

- Natuurkundigen onderzoeken een veilig alternatief voor röntgenbeveiligingsscanners
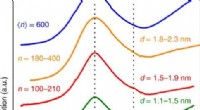
- Plasmonische kwantumgrootte-effecten in zilveren nanodeeltjes worden gedomineerd door interfaces en lokale omgevingen
 W.M. Keck Observatory zal diep in het intergalactische medium turen
W.M. Keck Observatory zal diep in het intergalactische medium turen Engels domineert wetenschappelijk onderzoek. Hier leest u hoe we dit kunnen oplossen en waarom het ertoe doet
Engels domineert wetenschappelijk onderzoek. Hier leest u hoe we dit kunnen oplossen en waarom het ertoe doet  Orkaan Oscar op satellietbeelden:een eenogig klein monster met een staart
Orkaan Oscar op satellietbeelden:een eenogig klein monster met een staart Kunstmatige organellen zetten vrije radicalen om in water en zuurstof
Kunstmatige organellen zetten vrije radicalen om in water en zuurstof betasten, slijpen, grijpen:uit nieuw onderzoek naar nachtclubs blijkt dat mannen het vaak doen, maar weten dat het verkeerd is
betasten, slijpen, grijpen:uit nieuw onderzoek naar nachtclubs blijkt dat mannen het vaak doen, maar weten dat het verkeerd is Wat is een standaardvormingsreactie?
Wat is een standaardvormingsreactie?  Wat is de naam van de chemische vergelijking CH3CH2OH plus 3O2 -------2C02 · 3H2O?
Wat is de naam van de chemische vergelijking CH3CH2OH plus 3O2 -------2C02 · 3H2O?  Wat is de hydroxide-ionenconcentratie van een oplossing met een pH van 12,40?
Wat is de hydroxide-ionenconcentratie van een oplossing met een pH van 12,40?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

