
Wetenschap
Waarom is boor niet-magnetisch?
Borium heeft een atoomnummer van 5, wat betekent dat het vijf elektronen heeft. Deze elektronen zijn gerangschikt in de atomaire orbitalen in de volgende configuratie:1s^2 2s^2 2p^1.
Zoals je kunt zien, heeft de 2p-orbitaal slechts één elektron. Dit betekent dat er geen ongepaarde elektronen in de atomaire structuur van boor voorkomen. Wanneer een magnetisch veld op een materiaal wordt aangelegd, zullen de ongepaarde elektronen zich parallel of antiparallel aan het veld uitlijnen. Deze uitlijning creëert een netto magnetisch moment, wat aanleiding geeft tot magnetisme.
Omdat boor geen ongepaarde elektronen heeft, kan het zijn elektronen niet in een magnetisch veld uitlijnen en vertoont het daarom geen magnetische eigenschappen. Dit is de reden waarom boor wordt beschouwd als een niet-magnetisch materiaal.
 Satellietgegevens tonen de ernst van de droogtezomers in 2018 en 2019
Satellietgegevens tonen de ernst van de droogtezomers in 2018 en 2019 Niet genoeg fruit, groenten geteeld om de planeet te voeden, studie onthult
Niet genoeg fruit, groenten geteeld om de planeet te voeden, studie onthult Hoe barrière-eilanden werken
Hoe barrière-eilanden werken  Virusvertraging, vroege ijssmelt-uitdaging Arctische wetenschappelijke missie
Virusvertraging, vroege ijssmelt-uitdaging Arctische wetenschappelijke missie Hoe hebben mensen onze planeten beïnvloed Biodiversiteit op zowel positieve als negatieve manieren?
Hoe hebben mensen onze planeten beïnvloed Biodiversiteit op zowel positieve als negatieve manieren?
Hoofdlijnen
- Haaien vertonen nieuwe veranderingen in hun immuunkankergerelateerde genen
- Wat zijn aldosen en ketosen?
- Hoe een bloeiende legale marihuana-industrie de luchtkwaliteit kan schaden
- Seizoensgebonden afbeeldingen onthullen de wetenschap achter stamcellen
- Onderzoek naar zeevogels aan de westkust laat zien hoe ze op een dag de lucht zouden kunnen delen met windturbines
- Hoe is een kleine bij in Frans-Polynesië terechtgekomen? Acht nieuwe soorten helpen het wetenschappelijke mysterie op te lossen
- Welke klassen van biologische moleculen worden het gemakkelijkst geabsorbeerd en gemetaboliseerd door gist?
- COVID-19-medicijnen blijven aanwezig in afvalwater, kunnen een risico vormen voor in het water levende organismen
- Longorganoïden onthullen hoe ziekteverwekkers menselijk longweefsel infecteren
- Een verrassend resultaat voor vastestoffysici duidt op een ongewoon elektronengedrag
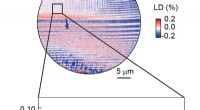
- Onderzoekers ontwikkelen de volgende generatie endoscopietechnologie

- Wetenschappers vinden een nieuw type microscoop uit die door een intacte schedel kan kijken
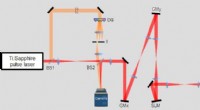
- Baanbrekende ontdekking van inkt kan de productie van nieuwe laser- en opto-elektronische apparaten transformeren

- Op zoek naar onzichtbare axion donkere materie met een nieuwe meercellige haloscoop
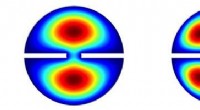
 Boemerangs keren terug met meer inzicht in ruimschoots gebruik
Boemerangs keren terug met meer inzicht in ruimschoots gebruik NASA-satelliet volgt overblijfselen van ex-tropische cycloon Beryl
NASA-satelliet volgt overblijfselen van ex-tropische cycloon Beryl Polaris Star:hoe je de poolster aan de nachtelijke hemel kunt spotten
Polaris Star:hoe je de poolster aan de nachtelijke hemel kunt spotten  Gemiddeld gebruik berekenen
Gemiddeld gebruik berekenen  Japan ziet de Olympische Spelen van 2020 als een herkansing op het technische podium
Japan ziet de Olympische Spelen van 2020 als een herkansing op het technische podium Hoe bereken ik beton voor een elektrische kanaalbank?
Hoe bereken ik beton voor een elektrische kanaalbank?  kroniek van de complexe ecologische veranderingen veroorzaakt door de steeds vluchtigere El Niño – La Niña-cycli
kroniek van de complexe ecologische veranderingen veroorzaakt door de steeds vluchtigere El Niño – La Niña-cycli Raciale vooroordelen erger bij politiemoorden op oudere, mentaal ziek, ongewapende mannen
Raciale vooroordelen erger bij politiemoorden op oudere, mentaal ziek, ongewapende mannen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

