
Wetenschap
Hoe werken handwarmers? Een wetenschappelijke blik
1. Activering :U knipt of schudt de handwarmer om een chemische reactie op gang te brengen.
2. Natriumacetaatkristallisatie :De reactie zet onderkoeld natriumacetaat om in vaste natriumacetaatkristallen.
3. Warmtegeneratie :Bij het kristallisatieproces komt warmte vrij, waardoor de temperatuur van de oplossing en de handwarmer stijgt.
4. IJzerkatalysator :IJzer of ijzeroxide helpt de kristallisatiereactie te versnellen.
5. Exotherme reactie :Het proces is exotherm, wat betekent dat er warmte vrijkomt.
6. Verwarmingsduur :De hitte houdt enkele uren aan, zolang er niet-gereageerd natriumacetaat aanwezig is.
Herbruikbare handwarmers:
1. Nucleatiepunt :Deze handwarmers hebben een metalen schijf die fungeert als kernpunt voor kristallisatie.
2. Buigen :Je buigt of buigt de metalen schijf om de kristallisatiereactie op gang te brengen.
3. Warmteafgifte :Bij de reactie ontstaat warmte, waardoor de temperatuur van de handwarmer stijgt.
4. Koelen :Naarmate de reactie voltooid is, koelt de handwarmer af.
5. Opnieuw koken :Je plaatst de gekoelde handwarmer in kokend water om het natriumacetaat te laten smelten.
6. Herkristallisatie :Het natriumacetaat herkristalliseert als je het uit het water haalt en laat afkoelen.
Handwarmers op gelbasis :
1. Klik op Activering :Je klikt op een metalen schijf of knop om een chemische reactie te starten.
2. Exotherme reactie :Bij de chemische reactie ontstaat warmte via een oxidatieproces.
3. Gelverwarming :De gel in de handwarmer bevat zouten en water, die de warmte absorberen.
4. Warmteverdeling :De gel verdeelt de warmte gelijkmatig over de handwarmer.
5. Duur en opwaarderen :Sommige handwarmers op gelbasis kunnen worden opgeladen door ze te koken voor toekomstig gebruik.
 Experimentele bermudagrassen laten een gevarieerde reactie op droogte zien
Experimentele bermudagrassen laten een gevarieerde reactie op droogte zien  Verschillende soorten weersomstandigheden
Verschillende soorten weersomstandigheden We hadden gisteren een deal nodig:deadline verstrijkt zonder deal om Colorado River te redden. Wat nu?
We hadden gisteren een deal nodig:deadline verstrijkt zonder deal om Colorado River te redden. Wat nu? Waarom smolten gashydraten aan het einde van de laatste ijstijd?
Waarom smolten gashydraten aan het einde van de laatste ijstijd? Nieuwe studie helpt verklaren hoe vuilvlekken zich vormen in de oceanen van de wereld
Nieuwe studie helpt verklaren hoe vuilvlekken zich vormen in de oceanen van de wereld
Hoofdlijnen
- Metafase: wat gebeurt er in dit stadium van mitose en meiose?
- Hoge verwachtingen van Australische poging om pandawelpen te fokken
- Platte gezichten en moeite met ademhalen:hoe huisdiertrends de diergezondheid hebben geschaad – en wat we eraan kunnen doen
- Uit herbebossingsonderzoek blijkt dat slechts enkele boomsoorten een eeuw van snelle klimaatverandering kunnen overleven
- Hoe insecten hun vleugels beheersen:de mysterieuze mechanica van insectenvluchten
- Onkruidverdelger glyfosaat, controversieel maar nog steeds het meest gebruikt
- Wat organiseert het genoom in de kern?
- Genoomonderzoek daagt eerder begrip van de oorsprong van fotosynthese uit
- Wetenschap komt dichter bij het verklaren van de boze dronkaard
- Hoe worden microben aangetrokken door een olieramp?

- Veelzijdig LED-bestralingssysteem:van desinfectie tot medische behandelingen

- Het stabiliseren van meerlaagse stromen kan het transport van zware oliën verbeteren

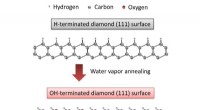
- Onthardingstechniek met waterdamp op diamantoppervlakken voor stroomapparatuur van de volgende generatie
- Onderzoekers maken schakelbare spiegels van vloeibaar metaal

 Hoe lang duurt het voordat een orkaan door het land reist?
Hoe lang duurt het voordat een orkaan door het land reist?  Koel blijven met een zwarte halfgeleider
Koel blijven met een zwarte halfgeleider Synthetisch suède geeft high-end auto's een luxe gevoel
Synthetisch suède geeft high-end auto's een luxe gevoel Bezorgd over klimaatverandering? Plant een overwinningstuin
Bezorgd over klimaatverandering? Plant een overwinningstuin Wetenschappers onderzoeken mysterieus smelten van aardkorst in het westen van Noord-Amerika
Wetenschappers onderzoeken mysterieus smelten van aardkorst in het westen van Noord-Amerika Squishy hydrogels kunnen het ticket zijn voor het bestuderen van biologische effecten van nanodeeltjes
Squishy hydrogels kunnen het ticket zijn voor het bestuderen van biologische effecten van nanodeeltjes Satelliet ziet tropische depressie Greg als een spookachtige werveling van wolken
Satelliet ziet tropische depressie Greg als een spookachtige werveling van wolken Origami inspireert onderzoek naar materialen die zichzelf assembleren bij blootstelling aan licht (met video)
Origami inspireert onderzoek naar materialen die zichzelf assembleren bij blootstelling aan licht (met video)
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

