
Wetenschap
Aanwijzingen uitstippelen voor de toekomst van betrouwbare modellen voor bloedstollingsmoleculen
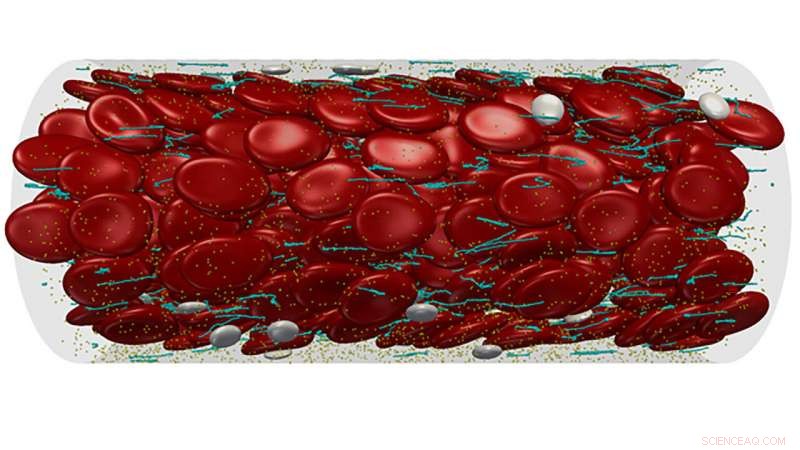
Onderzoekers beoordelen recent werk over het begrijpen van het gedrag van con Willebrand-factor in APL Bioengineering, het schilderen van een portret van vWF, en door de vooruitgang in het veld te benadrukken, de auteurs bieden veelbelovende mogelijkheden voor therapieën bij het beheersen van deze eiwitten. Multischaalmodellering van complexe bloedstroom door een microvat. Krediet:Zixiang Liu
Bloedstolsels zijn al lang betrokken bij hartaanvallen en beroertes, samen goed voor bijna de helft van de sterfgevallen per jaar in de Verenigde Staten. Hoewel de rol van één sleuteleiwit in het proces, genaamd von Willebrand-factor, is opgericht, een betrouwbaar model om te voorspellen hoe vWF zich in bloedvaten verzamelt, blijft ongrijpbaar.
Onderzoekers van het Georgia Institute of Technology publiceerden een recensie van recent werk over het begrijpen van het gedrag van vWF in APL Bio-engineering . Het papier schildert een portret van vWF, die zich ontrolt onder de schuifspanning van de bloedstroom om netten te vormen die voorbijgaande bloedplaatjes opvangen, die dan een bloedstolsel vormen, een trombus genoemd. Door de vooruitgang in het veld te benadrukken, de auteurs bieden veelbelovende mogelijkheden voor therapieën om deze eiwitten onder controle te houden.
"De trombus moet de bloedstroom blokkeren als hij afsluit, zoals proberen je duim aan het einde van een tuinslang te gebruiken en dan alle stroming stoppen met wat modder, " zei David Ku, een auteur op papier. "Dit is extreem moeilijk om te bereiken, dus trombose vereist de snelste, sterkste banden in de hele biologie."
Een uitdaging is dat veel van de huidige experimentele modellen alleen gebeurtenissen op de schaal van microns per seconde of zo kunnen afbeelden. vWF-eiwitten, echter, zijn ongeveer een duizendste van die grootte, en hun interacties vinden plaats in een duizendste van die tijd.
Er is een verscheidenheid aan computermodellen voorgesteld om de kloof van microschaal naar nanoschaal bij stolselvorming te overbruggen, variërend van simulaties op basis van de tijd die nodig is om stolsels te vormen tot rekenintensieve modellen die nabootsen hoe bloedplaatjes, vWF en cellen interageren allemaal in de bloedbaan. De paper roept onderzoekers uit de hele biologie op, informatica en andere gebieden om samen te werken om een verbeterd model te bouwen.
Naast het richten op bloedplaatjesaggregatie en high-shear omgevingen die vWF uitrekken, een mogelijke therapie is het versterken van de activiteit van een ander eiwit, ADAMTS13, die vWF splitst en ervoor zorgt dat het geen stolsels kan vormen. Hoewel onderzoek naar muismodellen veelbelovend is, er is nog veel werk nodig om te bepalen of ADAMTS13-therapieën veilig of effectief zijn voor mensen.
Ku's eigen onderzoek wees op negatief geladen nanodeeltjes waarvan computationele modellering heeft aangetoond dat ze vWF in zijn opgerolde niet-reactieve toestand kunnen houden. De groep ontdekte dat de nanodeeltjes verminderen hoe snel bloedvaten verstopt raken en onderzoeken hoe dit proces kan worden verklaard en geoptimaliseerd.
Ku zei dat hij hoopt dat het artikel anderen zal inspireren om dieper in te gaan op nieuwe manieren om de stolselvormende vWF te meten en te begrijpen.
 Onderzoekers ontwerpen katalysatoren voor dinucleaire locaties en onthullen het onderliggende mechanisme
Onderzoekers ontwerpen katalysatoren voor dinucleaire locaties en onthullen het onderliggende mechanisme Nieuwe stoffen met antivirale eigenschappen
Nieuwe stoffen met antivirale eigenschappen Verwijdering van boorzuur
Verwijdering van boorzuur  Een scanning transmissie-röntgenmicroscoop voor analyse van chemische toestanden van lithium
Een scanning transmissie-röntgenmicroscoop voor analyse van chemische toestanden van lithium Nieuw elektrodemateriaal ontwikkeld om de laadcapaciteit van lithiumbatterijen te vergroten
Nieuw elektrodemateriaal ontwikkeld om de laadcapaciteit van lithiumbatterijen te vergroten
 Typen meteorologie
Typen meteorologie Aardbevingsvoorspellingen komen een stap dichter bij de realiteit
Aardbevingsvoorspellingen komen een stap dichter bij de realiteit Modellen van de volgende generatie die het effect van klimaatverandering op orkanen onthullen
Modellen van de volgende generatie die het effect van klimaatverandering op orkanen onthullen Bevroren in de tijd:gletsjerarcheologie op het dak van Noorwegen
Bevroren in de tijd:gletsjerarcheologie op het dak van Noorwegen NASA vindt weinig kracht meer in tropische cycloon Herold
NASA vindt weinig kracht meer in tropische cycloon Herold
Hoofdlijnen
- Genoomanalyse van vroege plantenafstamming werpt licht op hoe planten leerden te gedijen op het land
- Wat zijn de functies van mRNA & tRNA?
- Panspermia:zorgden buitenaardse zaden ervoor dat het leven op aarde explodeerde?
- Stiekeme mannetjes nemen vrouwelijke hersens aan om grote bruten voor de gek te houden
- Vleugelstructuur van vitaal belang bij het produceren van een reeks tonen bij paringsoproepen van bush-cricket
- Hoe een tRNA-sequentie uit een DNA-sequentie te krijgen
- De microbiologische kunst van het maken van een betere worst
- Hoe neemt een slijmvorm beslissingen zonder hersenen?
- Wat is de functie van de pellet?
- Een gewicht-sterkte-verhouding berekenen

- Nieuwe metingen suggereren antineutrino anomalie gevoed door modelleringsfout

- Een nieuw soort kwantumcomputer

- Innovatief schakelmechanisme verbetert ultrasnelle controle van microlasers

- De realisatie van topologisch beschermde vallei-afhankelijke kwantumfotonische chips

 Apple roept sommige MacBook Pro-laptops terug vanwege brandgevaar
Apple roept sommige MacBook Pro-laptops terug vanwege brandgevaar Doorbraak in Japan kan weerswaarschuwingen verbeteren
Doorbraak in Japan kan weerswaarschuwingen verbeteren Afrika heeft betere wetenschappelijke capaciteit nodig om milieu-uitdagingen aan te gaan
Afrika heeft betere wetenschappelijke capaciteit nodig om milieu-uitdagingen aan te gaan Een verbeterde op ruthenium gebaseerde katalysator voor de synthese van primaire amines
Een verbeterde op ruthenium gebaseerde katalysator voor de synthese van primaire amines Mensgericht ontwerp toepassen op stemplaatsen
Mensgericht ontwerp toepassen op stemplaatsen Nieuwe techniek verbindt meerwandige koolstofnanobuisjes
Nieuwe techniek verbindt meerwandige koolstofnanobuisjes Een kijkje nemen onder de motorkap van topologische isolatoren
Een kijkje nemen onder de motorkap van topologische isolatoren Team benadrukt het werk aan het afstemmen van blokpolymeren voor nanogestructureerde systemen
Team benadrukt het werk aan het afstemmen van blokpolymeren voor nanogestructureerde systemen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

