
Wetenschap
Hoe u een hoogwaardige elektrolytoplossing voor batterijen kunt bereiden
Door Sean Lancaster
Bijgewerkt op 24 maart 2022
Batterijen zijn afhankelijk van twee halfcelreacties die met elkaar verbonden zijn door een zoutbrug en ondergedompeld zijn in een elektrolytoplossing. De loodzuuraccu, een belangrijk onderdeel van de aandrijfsystemen van auto's, maakt gebruik van halfcellen van looddioxide en waterstof. De elektrolyt, meestal een mengsel van zwavelzuur en water, levert de sulfaationen die nodig zijn voor de ontwikkeling van zuurstof en dient als ladingsdrager tussen de elektroden.
Stap 1:gebruik zuiver water
Vul een bekerglas ongeveer halfvol met gedestilleerd water. Gedestilleerd water minimaliseert verontreinigingen die het ionentransport kunnen verstoren. Sporen van lood in leidingwater kunnen bijvoorbeeld neerslaan als het wordt gemengd met NaCl, waardoor de geleidbaarheid van de oplossing verandert.
Stap 2:Selecteer de juiste elektrolyt
Kies een elektrolyt die de chemie van de halfcellen van uw batterij aanvult. Als het om koper gaat, zijn CuCO₃ of CuCl₂ geschikt omdat ze Cu²⁺-ionen leveren. Over het algemeen wordt de voorkeur gegeven aan een sterk zuur, een sterke base of hun zouten, zoals H₂SO₄, NaOH of Na₂SO₄, vanwege hun hoge dissociatiesnelheid en efficiënt ladingstransport.
Stap 3:Bepaal de concentratie
Meet voldoende elektrolyt om een concentratie van ongeveer 1M te bereiken. Concentraties onder deze drempel kunnen de celprestaties beperken, terwijl een te hoge concentratie overmatige viscositeit of corrosieve schade kan veroorzaken.
Stap 4:Mengen en roeren
Giet de gemeten elektrolyt in het bekerglas met gedestilleerd water. Roer grondig met een schone staaf tot de oplossing homogeen is. Dit zorgt voor een uniforme ionenverdeling en optimale geleiding.
Benodigde materialen
- Beker
- Sterk zuur, base of zout (bijv. H₂SO₄, NaOH, Na₂SO₄)
- Gedestilleerd water
- Roerstaaf
 Het berekenen van de mollen die nodig zijn voor een chemische reactie:een praktische gids voor stoichiometrie
Het berekenen van de mollen die nodig zijn voor een chemische reactie:een praktische gids voor stoichiometrie  Door SwRI ontwikkeld mobiel systeem om gevaarlijke chemische oorlogsmiddelen ter plaatse te vernietigen
Door SwRI ontwikkeld mobiel systeem om gevaarlijke chemische oorlogsmiddelen ter plaatse te vernietigen Wat de binaire ionische samengestelde naam voor Nabr?
Wat de binaire ionische samengestelde naam voor Nabr?  Welke stoffen bevatten een niet-polaire covalente binding mgf2 nacl nh3 h2o n2?
Welke stoffen bevatten een niet-polaire covalente binding mgf2 nacl nh3 h2o n2?  Welke vergelijking is een voorbeeld van een dubbele verplaatsingsreactie?
Welke vergelijking is een voorbeeld van een dubbele verplaatsingsreactie?
Hoofdlijnen
- Kunnen bacteriën agar verteren?
- 10 belangrijkste eigenschappen die levende organismen definiëren
- Wat zijn de belangrijke bijdragen van Francesco Redi aan de biologie?
- Wat betekent het als levende dingen zich voortplanten?
- Wat is de relatie tussen cellenweefselsorganen en orgaansystemen?
- Wat is een gen en wat doet het?
- Welke drie belangrijke functies presteert water in cellen?
- Wat kan in het echte leven worden vergeleken met de nucleolus?
- Wat is het verschil tussen een gen en eigenschap?
- Veranderingen in suikerachtige moleculen aan het oppervlak helpen kanker uitzaaien

- Wetenschappers ontwikkelen breedspectrumremmers van het griepvirus
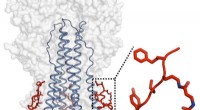
- Structurele inzichten in kleine bacteriële harpoenen
- Onderzoekers observeren het schakelen van Ras-eiwit in detail

- Herontworpen enzym kan schade door ruggenmergletsel en beroerte helpen terugdraaien
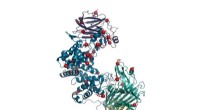
 Hoe hagedissen hun staarten regenereren:onderzoekers ontdekken een genetisch 'recept'
Hoe hagedissen hun staarten regenereren:onderzoekers ontdekken een genetisch 'recept'  Klimaatverandering zal miljoenen mensen verdrijven. Waar zullen ze heen gaan?
Klimaatverandering zal miljoenen mensen verdrijven. Waar zullen ze heen gaan? Hoe bomen water beheren in droge omgevingen
Hoe bomen water beheren in droge omgevingen  Wat is de energietransformatie van een flatshlight?
Wat is de energietransformatie van een flatshlight?  Wat is compound voor AII3?
Wat is compound voor AII3?  Heeft Mercurius een witte plek?
Heeft Mercurius een witte plek?  Wat is een meeteenheid voor alle vormen energie?
Wat is een meeteenheid voor alle vormen energie?  Facebook verdedigt het delen van gegevens na nieuw rapport over partnerdeals
Facebook verdedigt het delen van gegevens na nieuw rapport over partnerdeals
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

