
Wetenschap
Het berekenen van de mollen die nodig zijn voor een chemische reactie:een praktische gids voor stoichiometrie
Door Jack Brubaker – Bijgewerkt 30 augustus 2022
In elk laboratorium voeren scheikundigen nauwkeurige berekeningen uit om de exacte hoeveelheden reactanten en producten te bepalen die nodig zijn voor een bepaalde reactie. Deze discipline, bekend als stoichiometrie, is gebaseerd op het concept van de mol:een fundamentele eenheid die 6,022×10 23 vertegenwoordigt. formule-eenheden van een stof. De mol is zo gedefinieerd dat één mol van een verbinding precies het formulegewicht in grammen weegt, waarbij het formulegewicht de som is van de atoomgewichten van alle atomen in de molecuulformule. Natriumchloride (NaCl) heeft bijvoorbeeld een formulegewicht van 58,44 gmol -1 , wat betekent dat 58,44 g NaCl 6,022×10 23 bevat formule-eenheden.
Stap 1:Schrijf een evenwichtige chemische vergelijking
Begin met het opstellen van een evenwichtige vergelijking voor de reactie van interesse. Een gebalanceerde vergelijking bevat hetzelfde aantal van elk type atoom aan beide zijden van de pijl. Bijvoorbeeld de reactie tussen calciumhydroxide (Ca(OH)2 ) en zoutzuur (HCl) wordt geschreven als:
Ca(OH)2 + HCl → CaCl2 + H2 O
Deze versie is onevenwichtig:de linkerkant heeft twee zuurstofatomen en één chlooratoom, terwijl de rechterkant twee chlooratomen en één zuurstofatoom heeft. De correct uitgebalanceerde vergelijking is:
Ca(OH)2 + 2HCl → CaCl2 + 2H2 O
Nu verschijnt elk element aan beide kanten in gelijke aantallen.
Stap 2:Bepaal het gewicht van formules
Bereken vervolgens het formulegewicht van elke verbinding in de uitgebalanceerde vergelijking. Het formulegewicht wordt verkregen door de atoomgewichten van alle aanwezige atomen op te tellen. Bijvoorbeeld calciumchloride (CaCl2 ) bevat één calciumatoom (40,08 gmol -1 ) en twee chlooratomen (35,45gmol -1 elk), wat oplevert:
(1×40,08) + (2×35,45) =100,98gmol -1
Stap 3:Converteer bekende massa naar mol
Als u de massa van één reactant of product kent, converteert u die massa naar mol door te delen door het formulegewicht. Stel dat u, met behulp van de bovenstaande uitgebalanceerde reactie, 10 g calciumhydroxide heeft. Het formulegewicht van Ca(OH)2 bedraagt 74,10 gmol -1 , dus het aantal mol Ca(OH)2 aanwezig zijn:
10g ÷ 74,10 gmol -1 =0,135mol (≈0,13mol)
Stap 4:Pas de stoichiometrische verhouding toe
Gebruik de coëfficiënten uit de uitgebalanceerde vergelijking om de bekende mollen te relateren aan de onbekende mollen. In Ca(OH)2 + 2HCl → CaCl2 + 2H2 O, de stoichiometrische verhouding van HCl tot Ca(OH)2 bedraagt 2:1. Daarom:
0,135molCa(OH)2 ×(2molHCl·1molCa(OH)2 ) =0,270 molHCl
Er is dus 0,270 mol HCl nodig om volledig te reageren met 10 g Ca(OH)2 .
Benodigde materialen
- Periodiek systeem der elementen (voor atoomgewichten)
- Wetenschappelijke rekenmachine (voor delen en vermenigvuldigen)
Door deze systematische stappen te volgen, kunt u nauwkeurig de molhoeveelheden bepalen die nodig zijn voor elke chemische reactie, waardoor u verzekerd bent van nauwkeurige stoichiometrische berekeningen in het laboratorium.
 Wetenschappers modelleren nauwkeurig de werking van aerosolen op wolken
Wetenschappers modelleren nauwkeurig de werking van aerosolen op wolken Biotische factoren van het regenwoud
Biotische factoren van het regenwoud Wat is een proces waarbij een ecosysteem zichzelf kan vernieuwen?
Wat is een proces waarbij een ecosysteem zichzelf kan vernieuwen?  Wetenschappelijk boren ontrafelt het historische mysterie rond de vulkanische archipel van Santorini
Wetenschappelijk boren ontrafelt het historische mysterie rond de vulkanische archipel van Santorini  Hoe sloppenwijken veerkrachtiger kunnen worden tegen de klimaatverandering
Hoe sloppenwijken veerkrachtiger kunnen worden tegen de klimaatverandering
Hoofdlijnen
- Hoe bleek de celtheorie verkeerd?
- Welk organisme hangt volledig af van een ander leven voor bestaan op een manier die het andere organisme schaadt?
- Wat eten paddestoel?
- Planten en algen worden hoe genoemd?
- Wat vindt alleen plaats in het reproductieve weefsel van een organisme en tijdens het doorloopt een enkele cel twee divisies?
- Voor melkveehouders, waar blijft de tijd?
- Wat is evolutie van ontwikkelingsadministratie?
- Wat zijn enkele veel voorkomende toepassingen van gist?
- Wat is codominant genotype?
- Wetenschappers ontrafelen de werkingsprincipes van een veelbelovend materiaal voor het snel opladen van batterijen
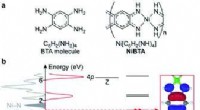
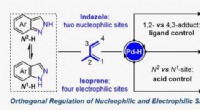
- Orthogonale regulatiestrategie biedt nieuwe kansen voor opbouw van moleculaire complexiteit
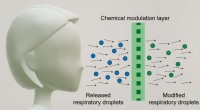
- Gezichtsmasker is bedoeld om het virus te deactiveren om anderen te beschermen
- Baanbrekende chemiebenadering kan leiden tot robuustere zachte elektronica

- Door ontwerp:van afval naar de volgende generatie koolstofvezel

 Met nieuwe algoritmen kunnen datawetenschappers in dagen bereiken wat ooit maanden duurde
Met nieuwe algoritmen kunnen datawetenschappers in dagen bereiken wat ooit maanden duurde  Trek 20% af op een rekenmachine:stapsgewijze handleiding
Trek 20% af op een rekenmachine:stapsgewijze handleiding  Waar is de onderste laag mantel uit samengesteld?
Waar is de onderste laag mantel uit samengesteld?  Heb je batterijen? Een stroomstoring blokkeert een gigantische technologieshow in Las Vegas
Heb je batterijen? Een stroomstoring blokkeert een gigantische technologieshow in Las Vegas  Hoe vormden de afzettingen van aardes zich?
Hoe vormden de afzettingen van aardes zich?  Wat is de pH van ammoniumnitraat?
Wat is de pH van ammoniumnitraat?  Wetenschappers ontwikkelen een goedkopere methode die kan helpen bij het maken van brandstoffen uit planten
Wetenschappers ontwikkelen een goedkopere methode die kan helpen bij het maken van brandstoffen uit planten Wat is de evolutie van de staat?
Wat is de evolutie van de staat?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

