
Wetenschap
Hard versus zacht water:belangrijkste verschillen en hoe deze uw leven beïnvloeden
Door Rosann Kozlowski Bijgewerkt op 24 maart 2022
pinkomelet/iStock/GettyImages
Water kan soms worden omschreven als hard water en zacht water. Het onderscheid berust op de hoeveelheid opgeloste mineralen in het water. Hard water bevat een grote hoeveelheid mineralen, en zacht water weinig tot geen.
Hard water en zacht water:oorsprong
Hard water en zacht water:oorsprong
Water verzamelt opgeloste vaste stoffen terwijl het door rotsen en andere substraten beweegt, zoals kalksteen, gips of dolomiet. Calcium en magnesium zijn bijzonder oplosbaar in water, en als deze natuurlijk voorkomende mineralen zich binnen het geografische gebied bevinden, zullen de bewoners rond de waterbron hard water hebben. .
In de Verenigde Staten hebben de gebieden aan de oostkust over het algemeen zacht water, en die in het zuidwesten hard water. Regenwater wordt als zacht beschouwd, omdat het niet zoals grondwater door bodemsubstanties is gesijpeld.
Hard water en zacht water:niveaus
Hard water en zacht
Water:Niveaus
De kenmerken van hard water en zacht water worden bepaald door de hoeveelheid mineralen in water, gemeten in milligram per liter of in granen per gallon. De hardheid hangt ook af van de pH en temperatuur van het water.
De American National Standards definiëren dat zacht water minder dan 17,1 mg/l bevat; de volgende niveaus kunnen echter worden gebruikt om de waterhardheid te benaderen:
- Zacht:0 – 60 mg/L
- Redelijk moeilijk:61
– 120 mg/L* Hard:121 – 180 mg/L
- Zeer hard:181 mg/L en hoger
Chemische eigenschappen van hardwater
Chemische eigenschappen van hard
Water
Veel voorkomende oorzaken van de waterhardheid zijn calcium, Ca en magnesium, Mg. Beide elementen zijn aardalkalimetalen die voorkomen in Groep 2 van het periodiek systeem. De elementen in de Groep 2-kolom hebben een lading van 2+ en verliezen twee elektronen om kationen te vormen, zoals Ca2+ en Mg2+. Deze kationen lossen gemakkelijk op in water.
Calciumcarbonaat CaCO3 is een veel voorkomende stof bij gesteentevorming, vooral van kalksteen, een soort sedimentair gesteente en dolomiet, CaMg(CO3)2, ook een sedimentair gesteente. Calciumcarbonaat wordt ook aangetroffen in de schelpen van mariene organismen en eieren.
Wanneer regenwater met opgelost kooldioxide, CO2, door calciumcarbonaat filtert, lossen de calciumionen op in het water. De volgende chemische vergelijking beschrijft dit proces:
CaCO3(s) + H20(l) + CO2(aq) → Ca2+(aq) + 2HCO3-
Waar het calciumcarbonaat, CaCO3, Ca2+ en bicarbonaat, HCO3-, vormt in aanwezigheid van water en koolstofdioxide.
Soorten hard water
Soorten hard water
De eigenschappen van hard water worden beschreven als tijdelijk en permanent . Tijdelijk hard water bevat bicarbonaat, HCO3-. Permanent hard water bevat bicarbonaationen met andere ionen zoals sulfaat, SO42-. Door koken worden de permanente verhardende soorten niet neergeslagen en zou natriumcarbonaat, Na2CO3, moeten worden toegevoegd.
Eigenschappen van hard water:vorming van neerslag
Eigenschappen van hard water:Vorming
Neerslag
Wanneer hard water wordt verwarmd, laat het vaak een laagje achter op potten of containers. Merk op dat de vergelijking voor dit neerslag het omgekeerde is voor de Ca2+-ionen die oplossen in een waterige oplossing:
Ca2+(aq) + 2HCO3- (aq) → CaCO3(s) + H20 (l) + CO2(aq)
Het calciumcarbonaatneerslag, CaCO3, wordt kalkaanslag genoemd. Hoewel het frustrerend is om schoon te maken, is het geen probleem voor de gezondheid.
Het neerslag kan zich in de loop van de tijd opbouwen; Dit kan echter de levensduur van apparaten zoals vaatwassers en wasmachines en eventuele leidingen beïnvloeden. De opeenhoping vernauwt de ruimte waar water kan stromen, en apparaten en leidingen moeten worden vervangen.
Eigenschappen van hard water:Interferentie met oppervlakteactieve stoffen
Eigenschappen van hard water:
Interferentie met oppervlakteactieve stoffen
Zoals hierboven vermeld bevat hard water opgeloste mineralen die voor consumenten problemen kunnen veroorzaken door afzettingen in sanitair en apparaten achter te laten. Hard water heeft ook invloed op de effectiviteit van veel huishoudelijke schoonmaakmiddelen.
De Ca2+- en Mg2+-ionen verstoren de oppervlakteactieve eigenschappen van **zeep. ** Een oppervlakteactieve stof verlaagt de oppervlaktespanning van water, waardoor het contact kan houden met een vast oppervlak, zoals kleding of een wastafel in de badkamer. De ionen verstoren het proces van de oppervlakteactieve stof, en hiervoor is vaak extra was- of schoonmaakmiddel nodig om een taak te voltooien.
De mineralen in hard water vormen samen met zeep een kleverige of wazige film op serviesgoed en in badkuipen, douches en gootstenen. Deze film kan ook kleding, huid en haar bedekken, waardoor kleding er smerig uitziet en een droge of geïrriteerde huid of haar ontstaat dat dof en onhandelbaar is.
Voordelen van hard water en zacht water
Hard water en zacht water
Voordelen
Hard water heeft een bijkomend gezondheidsvoordeel. Calcium en magnesium zijn belangrijke mineralen die het lichaam nodig heeft voor de groei en functie van botten en spieren. Deze mineralen reguleren ook de bloeddruk en de werking van enzymen. Het consumeren van hard water kan een bron van deze mineralen zijn.
Zacht water heeft niet de negatieve effecten van minerale afzettingen op huishoudelijke apparaten en afvoerleidingen. Het mist de minerale smaak van hard water en laat geen resten achter op de huid, de vaat of andere oppervlakken.
Methoden voor het verzachten van hard water
Methoden voor het verzachten van hard water
Een huishoudelijke waterontharder werkt door middel van ionenuitwisseling. Wanneer het harde water door een ionenwisselaar wordt geleid, stroomt het door lagen polymeer (plastic) kralen die covalent gebonden zijn aan aniongroepen, zoals:
- –COO-
- natrium
- Na+
- of kalium
- K+ kationen
Terwijl het water langs deze kralen stroomt, verdringen de calcium- en magnesiumionen de natrium- of kaliumionen.
Waterontharders:voordelen
Waterontharders:voordelen
De voordelen van waterontharders zijn schonere was, apparaten die langer meegaan en geen plakkerige zeepophoping. Consumenten gebruiken minder wasmiddel en andere soorten schoonmaak- en wasmiddelen. Kleding ziet er helderder uit en wastafels, badkuipen en douches behoeven minder schoonmaak.
Watertoestellen zoals boilers, waterverwarmers en vaatwassers werken doorgaans efficiënter en hebben minder onderhoud nodig, omdat zacht water geen kalkaanslag in leidingen en sanitaire voorzieningen veroorzaakt. Gebruikers van zacht water melden vaak dat het haar en de huid minder droog en schilferig aanvoelen.
Waterontharders:nadelen
Waterontharders:nadelen
De nadelen van waterontharders zijn onder meer de hoge kosten en inspanningen die gepaard gaan met het onderhouden van een wateronthardingssysteem. Een waterontharder en de installatie ervan kunnen duizenden dollars kosten, en er moet regelmatig zout aan de waterontharder worden toegevoegd.
Waterontharders zijn waterintensief tijdens het regeneratieproces en gebruiken tot 25 liter water per dag. Het doorspoelen van waterontharders met een zoutoplossing kan negatieve gevolgen hebben voor het milieu. Dit water, met zijn hoge natriumgehalte, wordt niet aanbevolen voor het bewateren van planten, gazons of tuinen.
Wat de gezondheid betreft bevat onthard water meer natrium dan hard water, en dit kan problematisch zijn voor mensen die hun zoutinname via de voeding moeten beperken. Omdat veel calcium en magnesium zijn verwijderd, biedt zacht water geen bron voor deze mineralen in de voeding.
 Nieuw onderzoek vindt dat tornado's van de grond af worden gevormd, in tegenstelling tot de populaire gedachte
Nieuw onderzoek vindt dat tornado's van de grond af worden gevormd, in tegenstelling tot de populaire gedachte Rifvissen erven tolerantie voor opwarmende oceanen
Rifvissen erven tolerantie voor opwarmende oceanen Economie van bosbiomassa werpt hindernissen op voor plattelandsontwikkeling
Economie van bosbiomassa werpt hindernissen op voor plattelandsontwikkeling Naar huis bellen? Ily vindt de vaste lijn slimmer en gebruiksvriendelijker
Naar huis bellen? Ily vindt de vaste lijn slimmer en gebruiksvriendelijker  Klimaatverandering verergert honger wereldwijd:VN
Klimaatverandering verergert honger wereldwijd:VN
Hoofdlijnen
- Hoe interageren abiotische en biotische factoren in een ecosysteem?
- Welk orgaan produceert enzymenhormonen en een alkalische vloeistof?
- In eukaryoten waar is actieve transcriptie over het algemeen aan geassocieerd?
- Waar of onwaar, alle levende dingen kunnen zich voortplanten?
- Microraptor:de kleine dinosaurus met vier vleugels die wetenschappers schokte
- Aardbeien zijn kleiner als bijen pesticiden binnenkrijgen, zo blijkt uit onderzoek
- Hoe zijn de verschillende vormen van een gen genoemd?
- Wat voor soort organisme is broodvorm?
- Kunnen menselijke lichaamscellen zich aseksueel voortplanten?
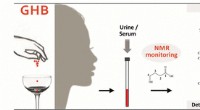
- De detectie van een date rape drug verbeteren
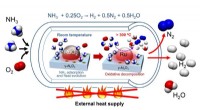
- Ontdekking van een eenvoudig proces voor H2-productie met ammoniak als drager
- Chemici ontwikkelen nieuwe methode om eiwitten te identificeren

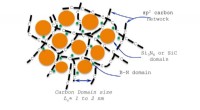
- Ingenieur patenteert waterachtig polymeer om keramiek op hoge temperatuur te maken
- Wetenschappers verbeteren een fotosynthetisch enzym door fluoroforen toe te voegen

 Is hormoon geen product van biotechnologie?
Is hormoon geen product van biotechnologie?  Hoe het heelal wordt weerkaatst in de buurt van zwarte gaten
Hoe het heelal wordt weerkaatst in de buurt van zwarte gaten Hoe lockdown-afspeellijsten werden gebruikt om emoties te uiten tijdens de pandemie
Hoe lockdown-afspeellijsten werden gebruikt om emoties te uiten tijdens de pandemie Onderzoek van bergen afgebeeld in Tableau Physique onthult fouten, impact van klimaatverandering
Onderzoek van bergen afgebeeld in Tableau Physique onthult fouten, impact van klimaatverandering Verbeterde verwering van rotsen kan atmosferische CO2 met beperkt effect verminderen
Verbeterde verwering van rotsen kan atmosferische CO2 met beperkt effect verminderen Anders omgaan met rampen is cruciaal voor kuststeden
Anders omgaan met rampen is cruciaal voor kuststeden Is het eten van een appelkinectische of potentiële energie?
Is het eten van een appelkinectische of potentiële energie?  Hoe een over het hoofd gezien onderzoek van meer dan een eeuw geleden de Colorado River-crisis heeft aangewakkerd
Hoe een over het hoofd gezien onderzoek van meer dan een eeuw geleden de Colorado River-crisis heeft aangewakkerd
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

