
Wetenschap
Elementen vergelijkbaar met chloor:eigenschappen en reactiviteit
1. Fluor (F) :Fluor is het lichtste halogeen en het meest reactieve niet-metaal. Het deelt veel eigenschappen met chloor, zoals het sterke oxiderende vermogen, de neiging om diatomische moleculen (F2) te vormen en het vermogen om ionische verbindingen met metalen te vormen.
2. Broom (Br) :Broom bevindt zich onder chloor in het periodiek systeem en is bij kamertemperatuur een roodbruine vloeistof. Het heeft vergelijkbare chemische eigenschappen als chloor, vormt diatomische moleculen (Br2) en vertoont reactiviteit met metalen en andere elementen.
3. Jodium (I) :Jodium is bij kamertemperatuur een vaste stof met een donkergrijs, bijna zwart uiterlijk. Het heeft vergelijkbare chemische eigenschappen als chloor, waaronder het vermogen om diatomische moleculen (I2) te vormen en de reactiviteit met metalen. Jodium is echter minder reactief dan chloor.
Belangrijkste overeenkomsten:
* Elektronenconfiguratie: Alle halogenen hebben 7 elektronen in hun buitenste schil, waardoor ze vergelijkbare chemische reactiviteiten hebben.
* Oxiderende kracht: Halogenen zijn sterke oxidatiemiddelen, wat betekent dat ze gemakkelijk elektronen opnemen.
* Vorming van diatomische moleculen: Alle halogenen bestaan als tweeatomige moleculen in hun elementaire toestand (F2, Cl2, Br2, I2).
* Vorming van ionische verbindingen: Halogenen vormen gemakkelijk ionische verbindingen met metalen door elektronen te accepteren om een stabiel octet te bereiken.
Belangrijke opmerking: Hoewel deze elementen veel overeenkomsten vertonen, kunnen hun eigenschappen in intensiteit variëren als gevolg van verschillen in elektronegativiteit, atomaire grootte en andere factoren.
 Ontbossing van het Amazonebekken kan verre regenwouden verstoren door een klimaatverbinding op afstand
Ontbossing van het Amazonebekken kan verre regenwouden verstoren door een klimaatverbinding op afstand Is het olielek gestopt? Wat we weten over de oorsprong van de massale lekkage in Orange County?
Is het olielek gestopt? Wat we weten over de oorsprong van de massale lekkage in Orange County? Watercrisis grijpt Amerikaanse stad in de greep na loodbesmetting
Watercrisis grijpt Amerikaanse stad in de greep na loodbesmetting Wat kan een geschikte slogan zijn voor naaldbos?
Wat kan een geschikte slogan zijn voor naaldbos?  De impact van toerisme op de duurzaamheid van een vergrijzende gemeenschap in Japan
De impact van toerisme op de duurzaamheid van een vergrijzende gemeenschap in Japan
Hoofdlijnen
- Welk element is het hoofd van het leven op basis van koolstoffamilies?
- Wat zijn de twee categorieën van klieren op basis van hun methode secretie?
- De wereldberoemde Romeinse baden kunnen wetenschappers helpen de uitdaging van antibioticaresistentie het hoofd te bieden
- Welke organismen zijn eencellige organismen?
- Recombinant DNA begrijpen:het voorbeeld van een menselijk groeihormoonplasmide
- Wat is herpescomplex?
- Is ademhaling de exacte omkering van biochemische paden fotosynthese?
- Is de amoeba abiotisch of biotisch?
- Wat vormt een nucleotide?
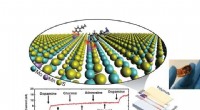
- Zeer gevoelige dopaminedetector maakt gebruik van 2D-materialen
- Het berekenen van pKa-waarden:een praktische gids voor chemici

- Een multidimensionaal beeld van SARS-CoV-2

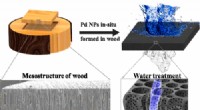
- Houtfilter verwijdert giftige kleurstof uit water
- Het uitlaatgas van een elektriciteitscentrale kan worden teruggewonnen en gebruikt als grondstof voor reactie

 Tesla zegt autobrand in Shanghai veroorzaakt door defecte batterijmodule
Tesla zegt autobrand in Shanghai veroorzaakt door defecte batterijmodule Wat zijn drie manieren waarop een atoom stabiliteit kan krijgen?
Wat zijn drie manieren waarop een atoom stabiliteit kan krijgen?  We hebben helemaal verkeerd nagedacht over hoe ijs zich vormt in cirruswolken
We hebben helemaal verkeerd nagedacht over hoe ijs zich vormt in cirruswolken Grote hoeveelheid calciumcarbonaat is typisch het type grond dat wordt genoemd?
Grote hoeveelheid calciumcarbonaat is typisch het type grond dat wordt genoemd?  COVID-19 een gouden kans voor terreurorganisaties om hun propaganda te intensiveren
COVID-19 een gouden kans voor terreurorganisaties om hun propaganda te intensiveren Hoe vind je het aantal atomen in 6.21 mol mg?
Hoe vind je het aantal atomen in 6.21 mol mg?  Flexibele nanosensoren voor draagbare apparaten
Flexibele nanosensoren voor draagbare apparaten Balansvergelijking voor H2O2 H2O + O2?
Balansvergelijking voor H2O2 H2O + O2?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

