
Wetenschap
Hoe suiker het vriespunt van water verlaagt – een wetenschappelijke verklaring
Door Claire Gillespie, bijgewerkt op 24 maart 2022
Allexxandar/iStock/GettyImages
Vriespunt
De temperatuur waarbij een vloeistof in een vaste stof verandert, wordt het vriespunt genoemd. Voor zuiver water is dit 32°F (0°C). Bij deze temperatuur zijn watermoleculen en ijsmoleculen in dynamisch evenwicht:water bevriest terwijl ijs met dezelfde snelheid smelt.
Watermoleculen
Een watermolecuul bestaat uit één zuurstofatoom en twee waterstofatomen. Wanneer de temperatuur daalt, neemt de kinetische energie van deze moleculen af, waardoor ze waterstofbruggen kunnen vormen die een kristallijn rooster creëren dat bekend staat als ijs.
Suiker aan water toevoegen
Wanneer suiker (sucrose) oplost in water, raken de suikermoleculen verspreid door het oplosmiddel. Ze verstoren het vermogen van watermoleculen om zich te voegen in de reguliere waterstofgebonden structuur die nodig is voor ijsvorming. De suikermoleculen nemen ruimte in die anders beschikbaar zou zijn voor water, waardoor de oplossing effectief wordt ‘verdrongen’.
Vriespuntdaling
Omdat suikerdeeltjes in de vloeibare fase blijven, verlagen ze het chemische potentieel van de oplossing. Dit fenomeen, bekend als vriespuntverlaging, betekent dat het mengsel moet worden afgekoeld tot onder 0°C voordat er zich ijs kan vormen. De omvang van de depressie hangt af van de suikerconcentratie:een grotere hoeveelheid opgeloste suiker leidt tot een grotere daling van de vriestemperatuur.
In de praktijk is dit de reden waarom suikerhoudende dranken en desserts vloeibaar blijven bij temperaturen waarbij gewoon water zou bevriezen. Het principe wordt veel toegepast bij het bewaren van voedsel en bij het maken van ijsbasissen die de gewenste textuur behouden.
 Van flatscreen-tv's tot uw smartphone:het element borium verdient meer aandacht
Van flatscreen-tv's tot uw smartphone:het element borium verdient meer aandacht Wat is de ionische vergelijking voor fosforzuur en bariumhydroxide?
Wat is de ionische vergelijking voor fosforzuur en bariumhydroxide?  Wanneer gemengd met water, creëert rioolwater een oplossing of mechanisch mengsel?
Wanneer gemengd met water, creëert rioolwater een oplossing of mechanisch mengsel?  Hoeveel mengsels zijn er in de wereld?
Hoeveel mengsels zijn er in de wereld?  Wat werd er gedaan voordat Dynamite werd uitgevonden?
Wat werd er gedaan voordat Dynamite werd uitgevonden?
Hoofdlijnen
- De beste manier om de effecten van genen en milieu in onderzoek te scheiden is?
- Wordt een vis als eencellig of multicellulair beschouwd?
- Hoe maak je een hypothese over het effect van een onjuiste mitotische verdeling op nieuwe geproduceerde cellen?
- Wat doet Mitochondrion in de dierencel?
- Welke microbe bestaat uit levende cel?
- Moet wetenschapper in een goed experiment de hyothese leegmaken?
- Welke ziekte omvat de afbraak van luchtzakken?
- Hoe orchideeën werken
- Hoeveel genen hebben mensen ongeveer?
- Een duurzamere manier om metalen te raffineren

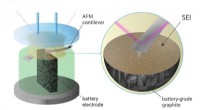
- Wetenschappers krijgen een voorproefje van een belangrijk proces in de levensduur van de batterij
- Duidelijk, geleidende coating kan geavanceerde zonnecellen beschermen, aanraakschermen

- Wat zeekomkommers ons kunnen leren over zelfverdediging

- Onderzoekers ontwikkelen een nieuwe manier om belangrijke biologische processen te bestuderen

 Wie heeft eerst sterrenbeelden opgenomen?
Wie heeft eerst sterrenbeelden opgenomen?  Dringende noodzaak voor het VK en zijn bondgenoten om duidelijk te maken hoe ze militair zullen reageren op dreigende gewapende aanvallen, zegt onderzoek
Dringende noodzaak voor het VK en zijn bondgenoten om duidelijk te maken hoe ze militair zullen reageren op dreigende gewapende aanvallen, zegt onderzoek Vrouwen op Tinder geven de voorkeur aan hoogopgeleide mannen
Vrouwen op Tinder geven de voorkeur aan hoogopgeleide mannen Welke fysieke eigenschappen kunnen in aantallen worden uitgedrukt?
Welke fysieke eigenschappen kunnen in aantallen worden uitgedrukt?  De plantenbiomen die worden gevonden onder de zeeën die worden genoemd?
De plantenbiomen die worden gevonden onder de zeeën die worden genoemd?  Onderzoeken hoe El Niño de neerslag over het Antarctisch Schiereiland en West-Antarctica beïnvloedt
Onderzoeken hoe El Niño de neerslag over het Antarctisch Schiereiland en West-Antarctica beïnvloedt  Wat bepaalt de grootte van de ster?
Wat bepaalt de grootte van de ster?  4,6-magnitude aardbeving rammelt Hawaiis Big Island
4,6-magnitude aardbeving rammelt Hawaiis Big Island
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

