
Wetenschap
Van der Waalskrachten:de verborgen lijm die moleculen bij elkaar houdt
kenzaza/iStock/GettyImages
Van der Waals-krachten vormen elektrostatische bindingen tussen moleculen. Deze intermoleculaire interacties – dipool-dipool, dipool-geïnduceerde en London-dispersie – houden vloeistoffen en vaste stoffen bij elkaar en beïnvloeden eigenschappen zoals oppervlaktespanning en kristalstructuur. Hoewel ze zwakker zijn dan covalente bindingen, bepalen ze op beslissende wijze het gedrag van veel materialen.
TL;DR
Van der Waals-krachten zijn zwakke elektrostatische interacties die moleculen binden. Van sterk naar zwak:dipool-dipool, dipool-geïnduceerd en Londense dispersie. Waterstofbruggen, een gespecialiseerde dipool-dipool-interactie, zijn bijzonder krachtig en bepalen belangrijke fysieke eigenschappen.
Soorten Van der Waals-krachten
1. Dipool-dipoolkrachten – Polaire moleculen met permanente positieve en negatieve uiteinden trekken elkaar aan, waardoor een stabiele elektrostatische binding ontstaat.
2. Door dipool geïnduceerde dipoolkrachten – Een polair molecuul induceert een tijdelijke dipool in een naburig niet-polair molecuul; de resulterende aantrekkingskracht is zwakker dan een echte dipool-dipoolbinding.
3. Londense verspreidingskrachten – Zelfs niet-polaire moleculen ervaren vluchtige verschuivingen in de elektronendichtheid, waardoor tijdelijke dipolen ontstaan die elkaar aantrekken. Deze krachten worden sterker in grotere moleculen met meer gedelokaliseerde elektronen.
Wanneer een waterstofatoom is gebonden aan een zeer elektronegatief element (F, O, N), wordt de resulterende sterke dipool-dipool-aantrekking een waterstofbinding genoemd. , een hoeksteen van de unieke eigenschappen van water.
Hoe de krachten van Van der Waals materialen beïnvloeden
In gassen liggen de moleculen ver uit elkaar en zijn ze te energetisch voor de Van der Waals-krachten om er toe te doen. In vloeistoffen blijven moleculen mobiel, waarbij ze herhaaldelijk zwakke bindingen vormen en verbreken, waardoor ze kunnen stromen terwijl ze nog steeds oppervlaktespanning en viscositeit vertonen. In vaste stoffen houdt de verminderde kinetische energie moleculen op hun plaats, en het cumulatieve effect van Van der Waals-interacties, naast ionische of metallische bindingen, definieert kristalroosters, glasachtige structuren en polymeerflexibiliteit.
Terwijl covalente bindingen de chemische identiteit dicteren, bepalen de krachten van Van der Waals dus het fysieke karakter (dichtheid, smeltpunt, hardheid) van het materiaal.
 Wat wordt er gevormd als HCO3- als bronsbasis fungeert?
Wat wordt er gevormd als HCO3- als bronsbasis fungeert?  Chemische synthese:nieuwe strategie voor het bewerken van skeletten op pyridines
Chemische synthese:nieuwe strategie voor het bewerken van skeletten op pyridines  Verbetering van de gevoeligheid voor analyse van ionische opgeloste stoffen
Verbetering van de gevoeligheid voor analyse van ionische opgeloste stoffen Wat is geconjugeerd zuur van ho?
Wat is geconjugeerd zuur van ho?  Fluor versus jodium:verschillen in reactiviteit begrijpen
Fluor versus jodium:verschillen in reactiviteit begrijpen
 Voedingsrijk menselijk afval klaar om de landbouw te ondersteunen, economie verbeteren
Voedingsrijk menselijk afval klaar om de landbouw te ondersteunen, economie verbeteren Zou het mogelijk zijn geweest om de vulkaanuitbarsting in Nieuw-Zeeland te voorspellen?
Zou het mogelijk zijn geweest om de vulkaanuitbarsting in Nieuw-Zeeland te voorspellen? Vroeg waarschuwingssysteem voor aardbevingen breidt zich uit naar Oregon, Washington
Vroeg waarschuwingssysteem voor aardbevingen breidt zich uit naar Oregon, Washington Toekomstige weersvoorspelling - het zit allemaal in de MRI van wolken
Toekomstige weersvoorspelling - het zit allemaal in de MRI van wolken NASA's CloudSat beëindigt de missie door in het hart van de wolken te turen
NASA's CloudSat beëindigt de missie door in het hart van de wolken te turen
Hoofdlijnen
- Wat is het nieuwe in de biologie?
- Een organisme heeft een diploïd aantal van 102 Wat is het haploïde aantal organismen?
- Stuctuur van een celmembraan
- Wat is een levend organisme dat zijn eigen voedsel maakt?
- Hoe overleef je een massale uitsterving?
- Hoe zijn bacteriën en plantencellen gelijk?
- Hoe wordt het individu geproduceerd door aseksuele reproductie?
- Welke voedingsmiddelen maken planten?
- Wat is het membraan ATPase en wat doet het?
- Zetmeel versus glycogeen:hoe planten en dieren koolhydraten opslaan

- Een duidelijk beeld schetsen van hoe stikstofoxiden worden gevormd

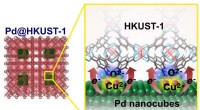
- Elektronische grensvlaktoestand die de waterstofopslagcapaciteit in Pd-MOF-materialen verbetert
- Onderzoekers ontdekken een nieuwe fase in blokcopolymeren

- Gezamenlijk onderzoek kan leiden tot verbeteringen in de productie van koolstofvezels

 Zijn zenuwengroepen cellen die samenwerken?
Zijn zenuwengroepen cellen die samenwerken?  Hoe heet het roodachtige bruine gas?
Hoe heet het roodachtige bruine gas?  Hoe kwantumeffecten de kunstmatige intelligentie kunnen verbeteren
Hoe kwantumeffecten de kunstmatige intelligentie kunnen verbeteren  Wat is atoomnummer?
Wat is atoomnummer?  Experiment gebruikt slimme stadsverlichting om uitstoot van straatverlichting te meten
Experiment gebruikt slimme stadsverlichting om uitstoot van straatverlichting te meten Wat is de uiteindelijke waterstofacceptor in elektrontransport en waar kwam het vandaan?
Wat is de uiteindelijke waterstofacceptor in elektrontransport en waar kwam het vandaan?  Meer dan de helft van alle sterren zijn enkele sterren?
Meer dan de helft van alle sterren zijn enkele sterren?  Vast materiaal dat zichtbare lichtfotonen 'opwaardeert' naar UV zou de manier waarop we zonlicht gebruiken kunnen veranderen
Vast materiaal dat zichtbare lichtfotonen 'opwaardeert' naar UV zou de manier waarop we zonlicht gebruiken kunnen veranderen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

