
Wetenschap
Wat bepaalt de sterkte van een zuur? Een duidelijke gids voor protondissociatie
Foto:iStock/GettyImages
Het bepalende kenmerk van een zuur is het gedrag van zijn waterstofatomen wanneer opgelost in water. Een sterk zuur geeft de meeste, zo niet alle, waterstofatomen vrij als vrije protonen, die zich onmiddellijk binden aan watermoleculen om hydroniumionen (H₃O⁺) te vormen. Het resterende deel van het zuurmolecuul wordt de geconjugeerde base, die een negatieve lading draagt. De mate waarin deze dissociatie plaatsvindt, bepaalt de sterkte van het zuur.
TL;DR
Sterke zuren ioniseren volledig, produceren hydroniumionen en laten de geconjugeerde base achter als een negatief ion. Zwakke zuren blijven grotendeels ongedissocieerd, waarbij slechts een klein deel protonen vrijgeeft. De balans tussen deze soorten geeft zuren hun karakteristieke gedrag.
Sterke zuren en hun dissociatie
De meest voorkomende sterke zuren zijn zoutzuur (HCl) en zwavelzuur (H₂SO₄). In zoutzuur is de H-Cl-binding zo zwak dat elk waterstofatoom loskomt wanneer het zuur oplost. Het vrijgekomen proton wordt een hydroniumion, terwijl het chloride-ion een lading van –1 heeft.
In zwavelzuur zijn beide waterstofatomen op vergelijkbare wijze zwak gebonden. Bij ontbinding vormen de twee protonen twee hydroniumionen, en de resterende SO₄²⁻-eenheid heeft een lading van –2. Vanwege deze volledige dissociatie zijn beide zuren zeer effectief in het protoneren van andere stoffen.
Sterke basen en hun dissociatie
Sterke basen gedragen zich precies andersom:ze geven hydroxide-ionen (OH⁻) af in plaats van protonen. Natriumhydroxide (NaOH) en calciumhydroxide (Ca(OH)₂) zijn klassieke voorbeelden. Elk molecuul splitst zich volledig in water, waardoor een hoge concentratie OH⁻ ontstaat die de oplossing een basaal karakter geeft.
Neutralisatie van sterke zuren en basen
Wanneer een sterk zuur en een sterke base elkaar ontmoeten, paren hun ionen volledig. De H⁺ uit het zuur combineert met de OH⁻ uit de base om water te vormen, terwijl de resterende ionen zich samenvoegen tot een neutraal zout. Door NaOH aan HCl toe te voegen, ontstaat bijvoorbeeld water en natriumchloride (NaCl), een stabiel, neutraal zout. De volledigheid van de ionisatie zorgt ervoor dat deze reacties onder normale omstandigheden kunnen worden voltooid.
 Vooruitgang in jacht op onbekende verbindingen in drinkwater
Vooruitgang in jacht op onbekende verbindingen in drinkwater Formulegewicht versus molaire massa:de relatie begrijpen
Formulegewicht versus molaire massa:de relatie begrijpen  Welke twee subatomaire deeltjes zijn in gelijke aantallen per atoom aanwezig?
Welke twee subatomaire deeltjes zijn in gelijke aantallen per atoom aanwezig?  Nieuwe katalytische benadering voor toegang tot belangrijke intermediaire carbokation
Nieuwe katalytische benadering voor toegang tot belangrijke intermediaire carbokation Wat is het vriespunt van een stof?
Wat is het vriespunt van een stof?
Hoofdlijnen
- Wat zijn de organen in het lichaam?
- Wat is de rol van bacteriën binnen een voedselweb?
- Wat is een kenmerk van een hypothese?
- Wat is de definitie van eubacteriën?
- DNA versus RNA: wat zijn de overeenkomsten en verschillen? (met diagram)
- Waarom vogels van een veer samen leken
- Wat de eerste paar cellen die vormen omdat ze elk type cel kunnen worden?
- Hoe kan een mutatie het gen veranderen?
- Gemanipuleerde bacteriën zijn veelbelovend voor een duurzame biobrandstofindustrie, zeggen onderzoekers
- Nobelweek gaat door met Scheikundeprijs

- Siliconen verkregen bij lage temperaturen met behulp van lucht

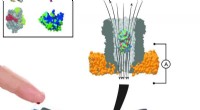
- Nieuwe methode meet enkele moleculen uit nanoliter bloed in realtime
- Hoe u de reactie-enthalpie nauwkeurig kunt berekenen

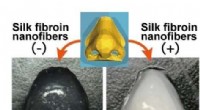
- Zijdevezels verbeteren bioinkt voor 3D-geprinte kunstmatige weefsels en organen
 Welk oxide kan worden gereduceerd tot het metaal met koolstof?
Welk oxide kan worden gereduceerd tot het metaal met koolstof?  Worden er kristallen gevormd uit mineralen opgelost in vloeistoffen?
Worden er kristallen gevormd uit mineralen opgelost in vloeistoffen?  Leven op land vereiste die planten?
Leven op land vereiste die planten?  Nieuw boormateriaal met hoge hardheid gecreëerd door chemische dampafzetting in plasma
Nieuw boormateriaal met hoge hardheid gecreëerd door chemische dampafzetting in plasma Nieuwe vliegende robot bootst snelle insectenvlucht na
Nieuwe vliegende robot bootst snelle insectenvlucht na Hoe verschillen obligate aeroben en anaëroben?
Hoe verschillen obligate aeroben en anaëroben?  Wat is erosieoppervlak?
Wat is erosieoppervlak?  Wat is de reactiviteit van Americium?
Wat is de reactiviteit van Americium?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

